
| 甲 | 乙 | 丙 | |
| 所含元素 | C、H | C、H、F | C、H、F |
| 所含電子數 | 26 | ||
| 結構特點 | 飽和有機物 | ||
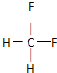 .下列關于乙的敘述正確的是D.
.下列關于乙的敘述正確的是D.分析 (1)化合物甲只含C、H兩種元素,為飽和有機物,應為烷烴,分子式符合CnH2n+2,分子中含有26個電子,則有6n+2n+2=26,n=3,則甲為C3H8;
(2)乙分子中C、H、F原子個數比為l:2:2,分子中含有26個電子,應為CH2F2,電子數為26,符合;聯系甲烷的空間結構判斷CH2F2的結構特點及具有的性質;
(3)將甲、乙按物質的量之比1:1混合所得混合物的平均摩爾質量等于丙的摩爾質量,丙的相對分子質量為:$\frac{44+52}{2}$=48,且分子中含有26個電子,應為C2H5F.
解答 解:(1)化合物甲只含C、H兩種元素,且為飽和有機物,則甲應為烷烴,分子式符合CnH2n+2,分子中含有26個電子,則有6n+2n+2=26,n=3,則甲為C3H8,若甲分子中有兩個H原子被F原子代替,所得產物可能有CH3CH2CHF2、CH3CF2CH3、CH2FCHFCH3、CH2FCH2CH2F共4種,
故答案為:C3H8;4;
(2)乙分子中C、H、F原子個數比為l:2:2,分子中含有26個電子,其分子式為CH2F2,CH2F2為共價化合物,其電子式為: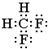 ,將所有共用電子對換成短線即為結構式,則其結構式為:
,將所有共用電子對換成短線即為結構式,則其結構式為: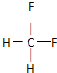 ,
,
A.甲烷為正四面體結構,而CH2F2為四面體形結構,不是正四面體,故A錯誤;
B.其分子中不存在不飽和鍵,不能使溴水褪色,故B錯誤;
C.1mol乙中含有2molH原子,最多能與2mol F2 發生取代反應,故C錯誤;
D.甲烷中所有H都等效,則CH2F2沒有同分異構體,故D正確;
故答案為: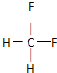 ;D;
;D;
(3)將甲、乙按物質的量之比1:1混合所得混合物的平均摩爾質量等于丙的摩爾質量,丙的相對分子質量為:$\frac{44+52}{2}$=48,且分子中含有26個電子,應為C2H5F,
故答案為:C2H5F.
點評 本題考查有機物分子式、結構簡式的確定,題目難度中等,明確烷烴的通式以及原子的構成為解答該題的關鍵,試題培養了學生的分析、理解能力及靈活應用基礎知識的能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
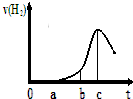 某興趣小組進行“活潑金屬與酸反應”的實驗,將5.4g的鋁片投入500mL 0.5mol•L-1的硫酸溶液中,下圖為反應產生氫氣速率與反應時間的關系圖.
某興趣小組進行“活潑金屬與酸反應”的實驗,將5.4g的鋁片投入500mL 0.5mol•L-1的硫酸溶液中,下圖為反應產生氫氣速率與反應時間的關系圖.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Na2CO3固體溶于1L水中配成溶液,其物質的量濃度為1mol/L | |
| B. | 40g NaOH固體溶于100g水,配成的溶液質量百分比濃度為40% | |
| C. | 22.4L氨氣溶于水配成1L溶液,其物質的量濃度為1mol/L | |
| D. | 1mol NaCl固體溶于水配成1L溶液,其物質的量濃度為1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na、Mg與水反應產生堿和氫氣,Fe與在一定條件下水反應也生成堿和氫氣 | |
| B. | CaC2能水解:CaC2+2H2O═Ca(OH)2+C2H2↑;則Al4C3也能水解:Al4C3+12H2O═4Al(OH)3↓+3CH4↑ | |
| C. | Fe能置換硫酸銅溶液的銅;則Na也能置換硫酸銅溶液的銅 | |
| D. | 工業上電解熔融MgCl2的制取金屬鎂;則也可以用電解熔融AlCl3的制取金屬鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 從上到下氫化物的熔沸點逐漸升高 | |
| B. | 從上到下單質的還原性逐漸減弱 | |
| C. | 從上到下最高價氧化物的水化物酸性逐漸減弱 | |
| D. | 從上到下原子得電子的能力逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
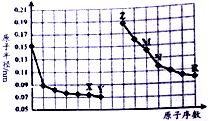
| A. | Y、R兩種元素的氣態氫化物穩定性大小:Y<R | |
| B. | 簡單離子的半徑:X>Z>M | |
| C. | 由X于N兩種元素組成的化合物不能與任何酸反應,但能與強堿反應 | |
| D. | Z單質能從M與R元素構成的鹽溶液中置換出單質M |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com