


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
(14分)
I.我國即將建成自己的載人空間站。載人航天器的生態(tài)系統(tǒng)中,不僅要求分離去除CO2,還要求提供充足的O2。
⑴某種電化學裝置可實現如下轉化:2CO2=2CO+O2,CO可用作燃料。已知該反應的某極反應為:4OH--4e-=O2↑+2H2O,則另一極反應為: 。
⑵有人提出,可以設計某溫度下的反應:2CO=2C+O2(△H>O、△S<O)來消除CO的污染。請你判斷該溫度下上述反應是否能發(fā)生并說明理由是 。
Ⅱ.大氣固氮屬于自然固氮,合成氨是目前人工固氮的主要方法。科學家一直致力“人工固氮”新方法的研究。
⑴有關大氣固氮(以N2+O2 2NO為例)、人工固氮(以N2+3H2
2NH3為例)反應的平衡常數
的值如下表。
| 反應 | N2+02 | N2+3H2 | ||
| 溫度/℃ | 27 | 2000 | 100 | 400 |
| K | 3.84×10-31 | 0.1 | 3.4×109 | 2.0x104 |
下列說法正確的是 。(填字母)
a.大氣固氮與人工固氮都是放熱反應
b.人類模擬大氣固氮無現實意義
c.尋找在常溫下合成氨的高效催化劑是目前人工固氮的新方向
d.在常溫下,人工固氮非常容易進行
⑵已知:N2(g)+3H2(g) 2NH3(g)
=-92.4kJ·mol-1
2H2(g)+02(g)=2H20(1) =-571.6 kJ·mol-1
據報道,在常溫、常壓、光照、催化劑的條件下,N2可以與水反應,則反應 N2(g)+3H20(1)=2NH3(g)+3/2O2(g)的= KJ·mol-1。
⑶某研究小組在673 K、30 MPa下,在體積為的密閉容器中進行反應:N2(g)+3H2(g)
2NH3(g),其(H2)和 (NH3)隨時間變化的關系如圖所示。
①下列敘述正確的是 。(填字母)
A.點a的正反應速率比點b的大
B.點c處反應達到化學平衡狀態(tài)
C.若t3時由673K升至773 K,則 (H2)將增大
②從開始到平衡時反應的平均速率(以H2的濃度變化表示) (H2)= 。
③若開始時 (N2)= (H2),則反應的平衡常數= (用代數式表示)。
查看答案和解析>>
科目:高中化學 來源:2011屆寧夏銀川二中高三第一次模擬考試試題(理綜)化學部分 題型:填空題
(14分)
I.我國即將建成自己的載人空間站。載人航天器的生態(tài)系統(tǒng)中,不僅要求分離去除CO2,還要求提供充足的O2。
⑴某種電化學裝置可實現如下轉化:2CO2=2CO+O2,CO可用作燃料。已知該反應的某極反應為:4OH--4e-=O2↑+2H2O,則另一極反應為: 。
⑵有人提出,可以設計某溫度下的反應:2CO=2C+O2(△H>O、△S<O)來消除CO的污染。請你判斷該溫度下上述反應是否能發(fā)生并說明理由是 。
Ⅱ.大氣固氮屬于自然固氮,合成氨是目前人工固氮的主要方法。科學家一直致力“人工固氮”新方法的研究。
⑴有關大氣固氮(以N2+O2  2NO為例)、人工固氮(以N2+3H2
2NO為例)、人工固氮(以N2+3H2 2NH3為例)反應的平衡常數
2NH3為例)反應的平衡常數 的值如下表。
的值如下表。
| 反應 | N2+02  2NO 2NO | N2+3H2 2NH3 2NH3 | ||
| 溫度/℃ | 27 | 2000 | 100 | 400 |
| K | 3.84×10-31 | 0.1 | 3.4×109 | 2.0x104 |
 2NH3(g)
2NH3(g) 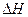 =-92.4kJ·mol-1
=-92.4kJ·mol-1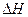 ="-571.6" kJ·mol-1
="-571.6" kJ·mol-1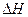 = KJ·mol-1。
= KJ·mol-1。 的密閉容器中進行反應:N2(g)+3H2(g)
的密閉容器中進行反應:N2(g)+3H2(g)  2NH3(g),其
2NH3(g),其 (H2)和
(H2)和 (NH3)隨時間變化的關系如圖所示。
(NH3)隨時間變化的關系如圖所示。
 (H2)將增大
(H2)將增大 (H2)= 。
(H2)= 。 (N2)=
(N2)= (H2),則反應的平衡常數
(H2),則反應的平衡常數 = (用代數式表示)。
= (用代數式表示)。查看答案和解析>>
科目:高中化學 來源:2010-2011學年寧夏高三第一次模擬考試試題(理綜)化學部分 題型:填空題
(14分)

I.我國即將建成自己的載人空間站。載人航天器的生態(tài)系統(tǒng)中,不僅要求分離去除CO2,還要求提供充足的O2。
⑴某種電化學裝置可實現如下轉化:2CO2=2CO+O2,CO可用作燃料。已知該反應的某極反應為:4OH--4e-=O2↑+2H2O,則另一極反應為: 。
⑵有人提出,可以設計某溫度下的反應:2CO=2C+O2(△H>O、△S<O)來消除CO的污染。請你判斷該溫度下上述反應是否能發(fā)生并說明理由是 。
Ⅱ.大氣固氮屬于自然固氮,合成氨是目前人工固氮的主要方法。科學家一直致力“人工固氮”新方法的研究。
⑴有關大氣固氮(以N2+O2  2NO為例)、人工固氮(以N2+3H2
2NO為例)、人工固氮(以N2+3H2  2NH3為例)反應的平衡常數
2NH3為例)反應的平衡常數 的值如下表。
的值如下表。
|
反應 |
N2+02
|
N2+3H2 |
||
|
溫度/℃ |
27 |
2000 |
100 |
400 |
|
K |
3.84×10-31 |
0.1 |
3.4×109 |
2.0x104 |
下列說法正確的是 。(填字母)
a.大氣固氮與人工固氮都是放熱反應
b.人類模擬大氣固氮無現實意義
c.尋找在常溫下合成氨的高效催化劑是目前人工固氮的新方向
d.在常溫下,人工固氮非常容易進行
⑵已知:N2(g)+3H2(g)  2NH3(g)
2NH3(g)  =-92.4kJ·mol-1
=-92.4kJ·mol-1
2H2(g)+02(g)=2H20(1)
 =-571.6 kJ·mol-1
=-571.6 kJ·mol-1
據報道,在常溫、常壓、光照、催化劑的條件下,N2可以與水反應,則反應 N2(g)+3H20(1)=2NH3(g)+3/2O2(g)的 = KJ·mol-1。
= KJ·mol-1。
⑶某研究小組在673 K、30 MPa下,在體積為 的密閉容器中進行反應:N2(g)+3H2(g)
的密閉容器中進行反應:N2(g)+3H2(g)  2NH3(g),其
(H2)和 (NH3)隨時間變化的關系如圖所示。
2NH3(g),其
(H2)和 (NH3)隨時間變化的關系如圖所示。

①下列敘述正確的是 。(填字母)
A.點a的正反應速率比點b的大
B.點c處反應達到化學平衡狀態(tài)
C.若t3時由673 K升至773 K,則 (H2)將增大
②從開始到平衡時反應的平均速率(以H2的濃度變化表示) (H2)= 。
③若開始時 (N2)= (H2),則反應的平衡常數 =
(用代數式表示)。
=
(用代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com