
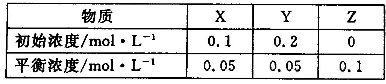
A.該反應可表示為 X+3Y 2Z 2Z |
| B.反應達到平衡時,X的轉化率為50% |
| C.前5min 以Y表示的平均反應速率為υ(Y)=" 0.01" mol·L-1·min-1 |
| D.增大壓強使平衡向生成Z的方向移動 |
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:不詳 題型:單選題
| 物質 | X | Y | Z |
| 初始濃度/mol·L- | 0.1 | 0.2 | 0 |
| 平衡濃度/mol·L- | 0.05 | 0.05 | 0.1 |
 2Z,其平衡常數為1600
2Z,其平衡常數為1600查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
 CO2+H2;在827℃時的平衡常數是100,如果反應開始時,一氧化碳和水蒸氣的濃度都是0.011mol/L,計算:一氧化碳在此反應條件下的平衡轉化率。
CO2+H2;在827℃時的平衡常數是100,如果反應開始時,一氧化碳和水蒸氣的濃度都是0.011mol/L,計算:一氧化碳在此反應條件下的平衡轉化率。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2Z(g)+W(g);ΔH>0。達平衡時,A的體積為1.2aL。下列說法錯誤的是
2Z(g)+W(g);ΔH>0。達平衡時,A的體積為1.2aL。下列說法錯誤的是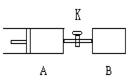
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2AB(g)達到平衡狀態的標志是( )
2AB(g)達到平衡狀態的標志是( )| A.單位時間內生成n mol A2的同時,生成n mol的AB |
| B.容器內的總壓強不隨時間而變化 |
| C.單位時間內生成2n mol AB的同時,生成n mol的B2 |
| D.單位時間內,生成n mol A2的同時,生成n mol的B2 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
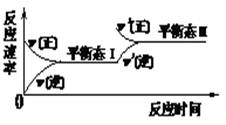
| A.反應達平衡時,正反應速率和逆反應速率相等 |
| B.同一種反應物在平衡態I和平衡態II時濃度不相等 |
| C.該反應達到平衡態I后,減小反應物濃度,平衡發生移動,達到平衡態II |
| D.該反應達到平衡態I后,增大反應物濃度,平衡發生移動,達到平衡態II |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO2(g)+ O2 (g)下列有關說法正確的是
2SO2(g)+ O2 (g)下列有關說法正確的是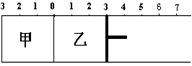
| A.若活塞固定在6處不動,達平衡時甲乙兩容器中的壓強:P乙=P甲 |
| B.若活塞固定在3處不動,達平衡時甲乙兩容器中SO3的濃度: c(SO3)乙>2c(SO3)甲 |
| C.若活塞固定在3處不動,達平衡時甲乙容兩器中SO2的體積分數:ψ(SO2)乙>2ψ(SO2)甲 |
| D.若活塞固定在7處不動,達平衡時兩容器中SO3的物質的量分數相等 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Si(s)+4HCl(g)△H=+236kJ/mol,將一定量反應物通入密閉容器進行以上可逆反應,既能提高SiCl4的轉化率又能縮短達到平衡的時間的是
Si(s)+4HCl(g)△H=+236kJ/mol,將一定量反應物通入密閉容器進行以上可逆反應,既能提高SiCl4的轉化率又能縮短達到平衡的時間的是| A.增大壓強 | B.減小氫氣濃度 | C.升高溫度 | D.加入催化劑 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
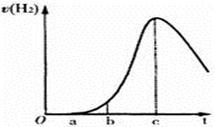
| A.t由0→a段不產生氫氣是因為表面的氧化物隔離了鋁和硫酸溶液 |
| B.t由b→c段產生氫氣的速率增加較快的主要原因之一是溫度升高 |
| C.t=c時反應處平衡狀態 |
| D.t>c產生氫氣的速率降低主要是因為溶液中c(H+)降低 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com