
【題目】已知某校回收的含銀懸濁廢水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,設計從廢水中回收硝酸銀的具體流程如下:
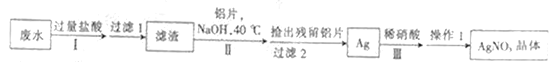
下列說法不正確的是
A. 步驟Ⅱ中發生的主要反應的離子方程:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O
B. 實驗中用鋁粉代替鋁片可以加快反應速率并簡化實驗操作
C. 步驟Ⅲ中若先將Ag氧化為Ag2O,再加入稀硝酸反應有利于環保
D. 操作Ⅰ包括蒸發濃縮、冷卻結晶、過濾、洗滌等
【答案】B
【解析】
含銀懸濁廢水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,加入鹽酸后生成氯化銀沉淀,過濾后,濾渣的主要成分是氯化銀,在氯化銀中加入鋁片、氫氧化鈉溶液后置換出銀,然后用硝酸溶解得到硝酸銀溶液,經過蒸發濃縮、冷卻結晶、過濾、洗滌得到硝酸銀晶體,據此分析解答。
A、步驟Ⅱ中主要發生鋁、氫氧化鈉溶液與氯化銀的置換反應,發生的主要反應的離子方程式為:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O,故A正確;
B、若實驗中用鋁粉代替鋁片可以加快反應速率,但置換出的銀中混入了鋁粉,還需要分離提純,沒有簡化實驗操作,故B錯誤;
C、銀與稀硝酸反應會生成NO,污染環境,若先將Ag氧化為Ag2O,再加入稀硝酸反應,可以防止NO的生成,有利于環保,故C正確;
D、操作Ⅰ是從硝酸銀溶液中獲得硝酸銀晶體,需要經過蒸發濃縮、冷卻結晶、過濾、洗滌等,故D正確;
故選B。


科目:高中化學 來源: 題型:
【題目】三苯甲醇是有機合成中間體。實驗室用格氏試劑![]() )與二苯酮反應制備三苯甲醇。已知:①格氏試劑非常活潑,易與水、氧氣、二氧化碳等物質反應;
)與二苯酮反應制備三苯甲醇。已知:①格氏試劑非常活潑,易與水、氧氣、二氧化碳等物質反應;
②![]()
③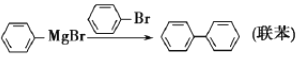
④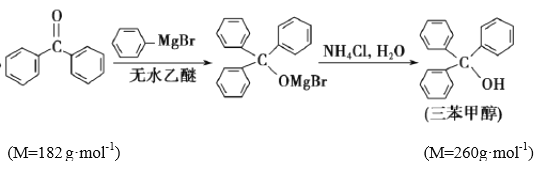
實驗過程如下
①實驗裝置如圖1所示。
a.合成格氏試劑:向三頸燒瓶中加入0.75g鎂屑和少量碘(引發劑),連接好裝置,在恒壓漏斗中加入3.20mL(0.03mol)溴苯和15.00mL乙醚混勻,開始緩慢滴加混合液,滴完后待用。
b.制備三苯甲醇:將5.50g二苯與15.00mL乙醚在恒壓漏斗中混勻,滴入三頸燒瓶。40℃左右水溶回流0.5h,加入20.00mL包和氯化銨溶液,使晶體析出。
②提純:圖2是簡易水蒸氣蒸餾裝置,用該裝置進行提純,最后冷卻抽濾
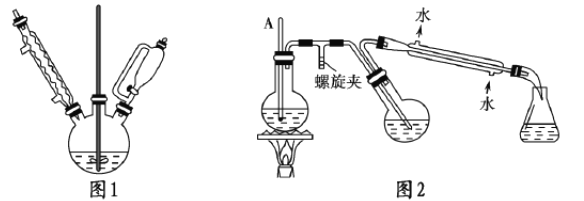
(1)圖1實驗中,實驗裝置有缺陷,應在球形冷凝管上連接____________裝置
(2)①合成格氏試劑過程中,低沸點乙醚的作用是____________________;
②合成格氏試劑過程中,如果混合液滴加過快將導致格氏試劑產率下降,其原因是______;
(3)提純過程中發現A中液面上升,此時應立即進行的操作是_______;
(4)①反應結束后獲得三苯甲醇晶體的操作為_______、過濾、洗滌______;
A.蒸發結晶 B.冷卻結晶 C.高溫烘干 D.濾紙吸干
②下列抽濾操作或說法正確的是_______
A.用蒸餾水潤濕濾紙,微開水龍頭,抽氣使濾紙緊貼在漏斗瓷板上
B.用傾析法轉移溶液,開大水龍頭,待溶液快流盡時再轉移沉淀
C.注意吸濾瓶內液面高度,當接近支管口位置時,撥掉橡皮管,濾液從支管口倒出
D.用抽濾洗滌沉淀時,應開大水龍頭,使洗滌劑快速通過沉淀物,以減少沉淀物損失
E.抽濾不宜用于過濾膠狀成劇粒太小的沉淀
(5)用移液管量取20.00mL飽和氯化較溶液,吸取液體時,左手______,右手持移液管;
(6)通過稱量得到產物4.00g,則本實驗產率為__________(精確到0.1%)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用勒夏特列原理解釋的是
A. 實驗室中常用排飽和食鹽水的方法收集Cl2
B. 對CO(g)+NO2(g)![]() CO2(g)+NO(g),平衡體系增大壓強可使顏色變深
CO2(g)+NO(g),平衡體系增大壓強可使顏色變深
C. 升高溫度能夠促進水的電離
D. 在含有Fe(SCN)3的紅色溶液中加少量鐵粉,振蕩靜置,溶液顏色變淺
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金剛烷(C10H16)的結構如圖1所示,它可以看成四個等同的六元環組成的空間構型。立方烷(C8H8)的結構如圖2所示。其中金剛烷的二氯代物和立方烷的六氯代物的同分異構體分別是 ( )
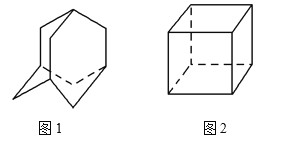
A. 4種和1種 B. 5種和3種
C. 6種和3種 D. 6種和4種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。現有Ca(OH)2溶液,向其溶液中逐漸通入CO2。則下列四個圖中,能比較準確地反映出溶液的導電能力和通入CO2氣體量的關系的是(x軸表示CO2通入的量,y軸表示導電能力)
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇(BaTiO3)主要用于電子陶瓷、PTC熱敏電阻、電容器等多種電子元器件的配制中。某工廠以重晶石(主要含BaSO4)為原料生產鈦酸鋇的工藝流程如圖:

回答下列問題:
(1)利用焰色反應的原理可定性鑒別某些金屬鹽。灼燒鈦酸鋇樣品時,鋇的焰色為______(填標號)。
A.磚紅色 B.黃綠色 C.紫色 D.黃色
(2)用Na2CO3溶液浸泡重晶石(雜質不與Na2CO3反應),能將BaSO4轉化為BaCO3,此反應的平衡常數K=_________。(已知Kap(BaSO4)=1.2×10-10、Kap(BaCO3)=2.4×10-9)。
(3)流程中“混合”溶液中的鈦元素在不同pH時主要以Ti(OH)+、TiOC2O4、TiO(C2O4)23-這三種形式存在(變化曲線如圖所示)。實際制備工藝中,先用氨水調節混合溶液的pH在______,再進行“沉淀”,寫出該條件下生成草酸氧鈦鋇晶體的離子方程式:__________。
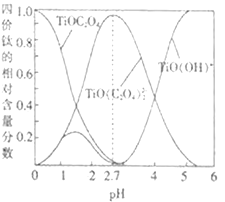
(4)檢驗草酸氧鈦鋇晶體是否洗滌干凈的操作是_________。
(5)隔絕空氣煅燒草酸氧鈦鋇晶體得到BaTiO3的同時,還能得到氣體產物有H2O(g)、________;
(6)BaTiO3成品中C2O42-的含量可以用“氧化還原滴定法”測得。稱取m g樣品,置于燒杯中,加入50mL0.2 mol·L-1酸性高錳酸鉀溶液充分反應后配制成100mL溶液,取20mL該溶液于錐形瓶中用0.1 mol·L-1的硫酸亞鐵溶液進行滴定,滴定達到終點的標志是__________,重復滴定3次,平均每次消耗硫酸亞鐵溶液的體積為20mL,則BaTiO3成品中C2O42-的質量分數為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.Fe(OH)3膠體可使水中懸浮物凝聚沉淀,是城市飲用水處理新技術。
(1)實驗室如何制取Fe(OH)3膠體,請簡述操作___,相應的化學方程式是____。
(2)向Fe(OH)3膠體中逐滴加入硅酸膠體,逐漸出現紅褐色沉淀,出現該現象的原因是____。
(3)除去膠體中混有的FeCl3和HCl的方法是___,如何驗證膠體已凈化完全,請簡述方法___。
Ⅱ.已知某“84消毒液”瓶體部分標簽如圖所示,該“84消毒液”通常稀釋100倍(體積之比)后使用。請回答下列問題:

(1)該“84消毒液”的物質的量濃度約為____mol·L-1(保留小數點后一位)。
(2)某同學取100 mL該“84消毒液”,稀釋后用于消毒,稀釋后的溶液中c(Na+)=____mol·L-1。
(3)該同學參閱該“84消毒液”的配方,欲用NaClO固體配制480mL含NaClO質量分數為25%的消毒液。下面操作造成所配溶液濃度偏高的是___(填序號)。
A.容量瓶用蒸餾水洗滌后未進行干燥處理,底部有少量水殘留
B.向容量瓶加水定容時眼睛俯視液面
C.燒杯溶解固體后,用蒸餾水潤洗2-3次,將部分洗滌液轉入容量瓶中
D.定容搖勻后發現液面低于刻度線,又加蒸餾水至刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,縱坐標表示導電能力,橫坐標表示所加溶液的量,以下各組反應,符合該圖的是( )
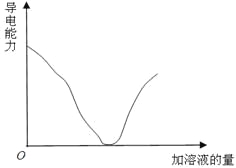
A.Ba(OH)2溶液中滴加稀H2SO4B.NaOH溶液中滴加稀HCl
C.CH3COOH溶液中滴加KOH溶液D.Cu(OH)2懸濁液中滴加HNO3溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com