
| A. | 磁性氧化鐵溶于鹽酸:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 淀粉碘化鉀溶液在空氣中變藍:4I-+O2+2H2O=2I2+4OH- | |
| C. | Na2O2與H2O反應制備O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| D. | 氯氣溶于水制備次氯酸:Cl2+H2O=2H++Cl-+ClO- |
分析 A.磁性氧化鐵為四氧化三鐵,不是氧化鐵,四氧化三鐵與鹽酸反應生成氯化鐵、氯化亞鐵和水;
B.碘離子被空氣中的氧氣氧化成碘單質,碘單質遇到淀粉顯示藍色;
C.2mol過氧化鈉與水反應生成1mol氧氣,該反應不滿足電子守恒;
D.次氯酸為弱電解質,離子方程式中次氯酸不能拆開.
解答 解:A.磁性氧化鐵的化學式為四氧化三鐵,將磁性氧化鐵溶于鹽酸的離子反應為:Fe3O4+8H+=2Fe3++Fe2++4H2O,故A錯誤;
B.淀粉碘化鉀溶液在空氣中,碘離子被氧氣氧化成碘單質,碘單質遇到淀粉變藍,反應的離子方程式為:4I-+O2+2H2O=2I2+4OH-,故B正確;
C.Na2O2與H2O反應制備O2,離子方程式必須滿足電子守恒,正確的離子方程式為:2Na2O2+2H2O=4Na++4OH-+O2↑,故C錯誤;
D.氯氣溶于水制備次氯酸,次氯酸需要保留分子式,正確的離子方程式為:Cl2+H2O=H++Cl-+HClO,故D錯誤;
故選B.
點評 本題考查了離子方程式的書寫判斷,為中等難度的試題,注意掌握離子方程式的書寫原則,明確離子方程式正誤判斷常用方法:檢查反應物、生成物是否正確,檢查各物質拆分是否正確,如難溶物、弱電解質等需要保留化學式,檢查是否符合守恒關系(如:質量守恒和電荷守恒等).


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 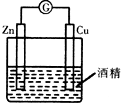 形成原電池 | B. | 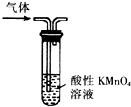 除去乙烯中混有的SO2 | ||
| C. | 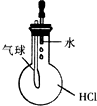 驗證HCl氣體在水中的溶解性 | D. | 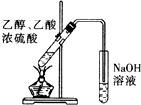 實驗室制取乙酸乙酯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ①②④ | C. | ①④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應屬于置換反應 | |
| B. | 該反應利用了KClO3的強氧化性 | |
| C. | 氧化劑與還原劑的物質的量之比為1:6 | |
| D. | 該反應中有5mo1電子轉移時,則一定生成67.2L Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
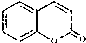 )是一種用途廣泛的香料,其合成路線如圖:
)是一種用途廣泛的香料,其合成路線如圖: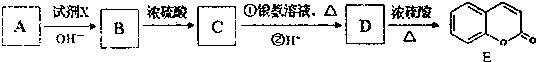
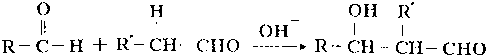
 ;
;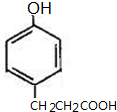 、
、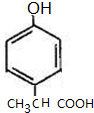 (寫出一種即可).
(寫出一種即可).查看答案和解析>>
科目:高中化學 來源: 題型:多選題
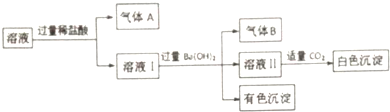
| A. | 氣體A一定沒有CO2,氣體B一定是NH3 | |
| B. | 有色沉淀一定是混合物 | |
| C. | Na+可能存在于該溶液中 | |
| D. | 白色沉淀中一定沒有Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
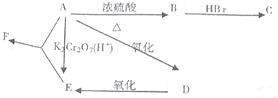
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com