
分析 濃硫酸物質的量濃度=$\frac{1000ρω}{M}$,根據溶液稀釋前后溶質的物質的量不變計算濃硫酸體積,量筒的規格應該等于或稍大于量取溶液體積.
解答 解:濃硫酸物質的量濃度=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,濃硫酸體積=$\frac{1.5mol/L×0.1L}{18.4mol/L}$=8.2mL,量筒的規格應該等于或稍大于量取溶液體積,所以應該選取10mL量筒,
故答案為:10mL;8.2.
點評 本題考查物質的量有關計算,為高頻考點,側重考查學生計算能力,正確計算濃硫酸濃度是解本題關鍵,易錯點是量筒規格的選取,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
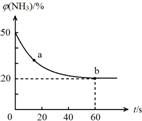 合理應用和處理氮的化合物,在生產生活中有重要意義.
合理應用和處理氮的化合物,在生產生活中有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl屬于共價化合物,溶于水能電離出H+和Cl- | |
| B. | NaOH是離子化合物,該物質中只含離子鍵 | |
| C. | HI氣體受熱分解的過程中,只需克服分子間作用力 | |
| D. | 石英和干冰均為原子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
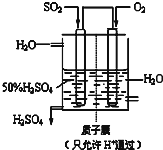 工業上為了測定輝銅礦(主要成分是Cu2S)中Cu2S的質量分數,設計了如圖裝置.實驗時按如下步驟操作:
工業上為了測定輝銅礦(主要成分是Cu2S)中Cu2S的質量分數,設計了如圖裝置.實驗時按如下步驟操作: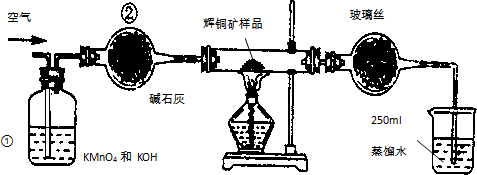
| 滴定 次數 | 待測溶液的 體積/mL | 標準溶液的體積 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 用鉛蓄電池電解苦鹵水(含C1-、Br-、Na+、Mg2+)的裝置如圖所示(a、b為石墨電極).下列說法中正確的是( )
用鉛蓄電池電解苦鹵水(含C1-、Br-、Na+、Mg2+)的裝置如圖所示(a、b為石墨電極).下列說法中正確的是( )| A. | 鉛蓄電池放電時,該電池兩極質量均減小 | |
| B. | 鉛蓄電池充電時,B極應與外電源負極相連 | |
| C. | 電解苦鹵水時,a電極首先放電的是Cl-而不是Br-,因為Cl-的還原性強于Br- | |
| D. | 當b極產生0.01 mol 氣體時,鉛蓄電池中消耗0.02 molH2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

| 離子 | Fe3+ | AP+ | ZrO2+ |
| 開始沉淀pH | 1.9 | 3.3 | 6.2 |
| 完仝沉淀pH | 3.2 | 5.2 | 8.0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com