

分析 (1)猜測硫酸亞鐵加熱可能發生反應,硫酸鹽$\stackrel{△}{→}$金屬氧化物+SO2↑+SO3↑+O2↑,則固體受熱分解連接順序為試管中加熱,根據氣體的制備和收集按照發生裝置→除雜裝置→干燥氣體→氣體吸收裝置→排水→測量裝置來組裝實驗儀器;
(2)加熱硫酸亞鐵生成三氧化硫和氧氣、二氧化硫、和氧化鐵,因為裝置F總質量在實驗結束時增加了0.16g,且其溶液中只有一種溶質,所以三氧化硫通入飽和亞硫酸氫鈉中發生反應生成硫酸氫鈉和二氧化硫;
(3)裝置C堿石灰吸收二氧化硫;
(4)測定氣體體積時,應裝置內氣體的溫度應恢復到室溫,調節量筒使其液面與E裝置中的液面持平,視線與液體的凹液面相平;
(5)1molSO3與1molSO2的質量差為16g,裝置F總質量在實驗結束時增加了0.16g,說明反應生成的SO3物質的量是0.01mol;最后測出量筒中水的體積后,折算成排水的氣體,在標準狀況下的體積為112mL即為氧氣體積,故得到氧氣0.005ml;6.08 g無水FeSO4的物質的量是$\frac{6.08g}{152g/mol}$=0.04mol,利用鐵元素守恒得生成Fe2O3的物質的量是0.02mol;通過質量守恒即可計算生成SO2的物質的量是0.03mol.
解答 解:(1)氣體的制備和收集按照發生裝置→除雜裝置→干燥氣體→氣體吸收裝置→排水→測量裝置來安裝實驗儀器,按從左至右的方向,先制備氣體,通過亞硫酸氫鈉吸收三氧化硫,再通過濃硫酸干燥二氧化硫氣體和氧氣,通過堿石灰吸收二氧化硫稱量計算,最后利用排水量氣法測定氧氣的體積,各儀器接口連接順序為:①⑨⑩⑥⑤③④⑧⑦②;
故答案為:⑥⑤、⑧⑦;
(2)加熱硫酸亞鐵生成三氧化硫和氧氣、二氧化硫、和氧化鐵,因為裝置F總質量在實驗結束時增加了0.16g,且其溶液中只有一種溶質,所以三氧化硫通入飽和亞硫酸氫鈉中發生反應生成硫酸氫鈉和二氧化硫,方程式為:SO3+NaHSO3=NaHSO4+SO2↑,所以亞硫酸氫鈉的作用是吸收SO3并且產生等物質的量的SO2氣體,故答案為:產生等物質的量的SO2氣體;
(3)氣體通過D裝置后還剩二氧化硫和氧氣,通過堿石灰吸收二氧化硫稱量計算,所以裝置C的作用是:吸收SO2氣體,故答案為:吸收SO2氣體;
(4)測定氣體體積時,應裝置內氣體的溫度應恢復到室溫,調節量筒使其液面與E裝置中的液面持平,由于量筒中液面是凹液面,所以讀量筒中液體體積時,視線與液體的凹液面相平,否則會造成誤差,
故答案為:與凹液面最低點保持水平相切;
(5)因為裝置F中發生方程式為:SO3+NaHSO3=NaHSO4+SO2↑,則1molSO3與1molSO2的質量差為16g,裝置F總質量在實驗結束時增加了0.16g,說明反應生成的SO3物質的量是0.01mol;最后測出量筒中水的體積后,折算成排水的氣體,在標準狀況下的體積為112mL即為氧氣體積,故得到氧氣0.005ml;6.08 g無水FeSO4的物質的量是$\frac{6.08g}{152g/mol}$=0.04mol,利用鐵元素守恒得生成Fe2O3的物質的量是0.02mol;通過質量守恒即可計算生成SO2的物質的量是$\frac{6.08-0.01×80-32×0.005-160×0.02}{64}$=0.03mol,反應方程式為:8FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$4Fe2O3+6SO2↑+2SO3↑+O2↑;
故答案為:8FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$4Fe2O3+6SO2↑+2SO3↑+O2↑.
點評 本題考查物質的組成和實驗數據的處理,做題時注意把握實驗基礎知識,充分利用有關數據進行計算,本題具有一定難度.難點是確定硫酸亞鐵的分解方程式的書寫,注意堿石灰吸收的二氧化硫有部分是硫酸亞鐵分解生成的、部分是三氧化硫和水、亞硫酸氫鈉反應生成的二氧化硫,否則會導致計算錯誤.


科目:高中化學 來源: 題型:選擇題
| A. | CO2、CH4、N2等均是造成“溫室效應”的氣體 | |
| B. | 天然氣是一種清潔的化石燃料 | |
| C. | 節能減排符合“低碳經濟”的要求 | |
| D. | 合理開發利用“可燃冰”(固態甲烷水合物)有助于緩解能源緊缺 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol H2O的質量為18g/mol | |
| B. | 11.2L氯氣所含的分子數為0.5NA | |
| C. | 0.1mol/L的Na2CO3溶液中所含Na+的物質的量為0.2mol | |
| D. | 常溫常壓下,1mol氦氣含有的核外電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
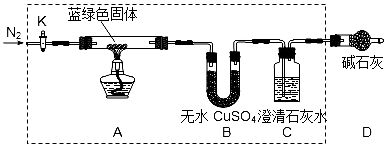
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32g | B. | 50g | C. | 72g | D. | 80g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
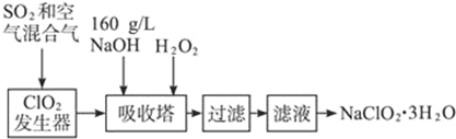
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某反應由兩步反應 A、B、C 構成,它的反應能量曲線如圖所示(E1、E2、E3、E4表示活化能).回答下列問題
某反應由兩步反應 A、B、C 構成,它的反應能量曲線如圖所示(E1、E2、E3、E4表示活化能).回答下列問題查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com