
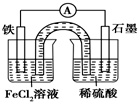
| A. | 原電池工作一段時間后,FeCl2溶液中c(Cl-)增大 | |
| B. | 此電池工作原理與硅太陽能電池工作原理相同 | |
| C. | Fe為正極,石墨上發生的反應為2H++2e-═H2↑ | |
| D. | 該裝置中的鹽橋完全可用金屬導線代替 |
分析 鐵為負極,被氧化,電極反應為Fe-2e-=Fe2+,石墨為正極,發生還原反應,電極反應為2H++2e-=H2↑,陰離子向負極移動,陽離子向正極移動,結合電極反應解答.
解答 解:A.Fe為負極,陰離子向負極移動,則FeCl2溶液中c(Cl-)會增大,故A正確;
B.硅太陽能電池是把太陽能轉化為電能,該電池是化學能轉化為電能,二者原理不同,故B錯誤;
C.Fe為負極,石墨為正極,正極上電極反應為2H++2e-=H2↑,故C錯誤;
D.若裝置中的鹽橋用金屬絲如鐵絲代替,右側中金屬Fe、石墨和稀硫酸溶液形成原電池,左側為電解池,所以電流表指針有偏轉,故D錯誤.
故選A.
點評 本題考查原電池知識,側重于原電池的工作原理的考查,注意把握電極反應的判斷,把握電極方程式的書寫,為解答該類題目的關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
 用已知物質的量濃度的NaOH溶液測定某H2SO4溶液的濃度(H2SO4溶液放入錐形瓶中),圖甲、乙是兩只規格都為50mL的滴定管,下列有關該實驗的說法正確的是( )
用已知物質的量濃度的NaOH溶液測定某H2SO4溶液的濃度(H2SO4溶液放入錐形瓶中),圖甲、乙是兩只規格都為50mL的滴定管,下列有關該實驗的說法正確的是( )| A. | 選用酚酞作指示劑的滴定終點的判斷:當淺紅色變為無色且半分鐘內仍為無色時即為滴定終點 | |
| B. | 滴定終點讀數時,俯視滴定管的刻度(其他操作均正確),會造成測定結果偏低 | |
| C. | 甲滴定管中盛有H2SO4溶液,液面恰好在10.00mL刻度處,并把甲滴定管中的H2SO4溶液全部放入燒杯中,其體積為40.00mL | |
| D. | 量取15.00mLKMnO4溶液應選擇乙滴定管 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ca2+、K+、Cl-、NO3- | B. | Na+、Ca2+、SO32-、ClO- | ||
| C. | Al3+、K+、OH-、NO3- | D. | Na+、Ca2+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
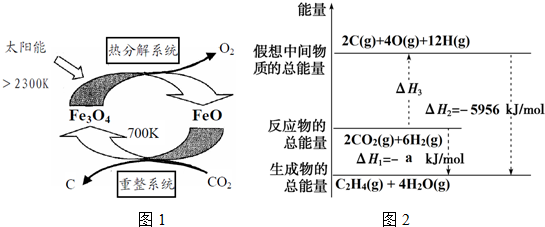
| 物質 | CO2(g) | C2H4(g) | H2O(g) |
| 能量/kJ•mol-1 | -394 | 52 | -242 |
| 化學鍵 | C=O | H-H | C=C | O-H |
| 鍵能/kJ•mol-1 | 803 | b | 615 | 463 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
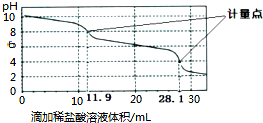
| A. | 上一計量點前發生反應的離子方程式為HCO3-+H+═H2O+CO2↑ | |
| B. | 下一個計量點溶液中存在大量的陰離子是Cl-、HCO3- | |
| C. | 此樣品n(NaHCO3)=(28.1-2×11.9)×10-3mol | |
| D. | 使用該方法測定Na2CO3和NaOH混合物中氫氧化鈉含量,將會得到1個計量點 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com