
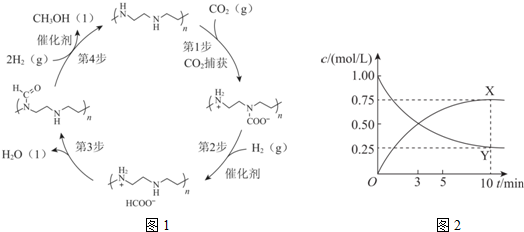
分析 (1)CO2中含有極性共價鍵;
(2)互溶沸點不同的液體混合物用蒸餾的方法分離;
(3)根據蓋斯定律,可知反應熱的大小與起態和始態有關與過程無關;
(4)①由圖可知X的量在增加,Y的量再減少,而且變化量相同,所以Y是反應物,而且計量數與生成物的計量數相同;
②a.Y的轉化率是$\frac{1-0.25}{1}×100%$=75%;
b.因為正反應是氣體體積減少的反應,所以其他條件不變時,若在恒壓條件下進行該反應,相當于增大壓強,Y的轉化率變大;
c.升高溫度使該反應的平衡常數K增大,則可知該反應為吸熱反應;
d.催化劑只改變反應的速率,但平衡不移動;
③速率之比等于對應物質的化學計量數之比,結合v=$\frac{△c}{△t}$進行計算.
解答 解:(1)CO2中含有極性共價鍵,故答案為:極性共價;
(2)甲醇(沸點為64.7℃)與水的沸點不同,所以用蒸餾的方法分離,故答案為:蒸餾;
(3)根據蓋斯定律,可知反應熱的大小與起態和始態有關與過程無關,所以該轉化總反應的熱化學方程式是CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=(a+b+c+d) kJ/mol,故答案為:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=(a+b+c+d) kJ/mol;
(4)①由圖可知X的量在增加,Y的量再減少,而且變化量相同,所以Y是反應物,而且計量數與生成物的計量數相同,所以Y是CO2,故答案為:CO2;Y隨反應進行濃度減小,因此Y為反應物,且其相同時間內轉化量與X相同,則其在方程式中的化學計量數應與X相同,因此Y是CO2;
②a.Y的轉化率是$\frac{1-0.25}{1}×100%$=75%,故正確;
b.因為正反應是氣體體積減少的反應,所以其他條件不變時,若在恒壓條件下進行該反應,相當于增大壓強,Y的轉化率變大,故正確;
c.升高溫度使該反應的平衡常數K增大,則可知該反應為吸熱反應,故正確;
d.催化劑只改變反應的速率,但平衡不移動,故錯誤;
故選:abc;
③v(CO2)=$\frac{0.75}{10}$=0.075mol/(L•min),而v(H2)=$\frac{1}{3}$v(CO2)=0.225 mol/(L•min),故答案為:0.225.
點評 本題為綜合題,涉及化學平衡影響因素分析、化學反應速率的計算、反應熱的計算、熱化學反應方程式的書寫等知識點,注重高考常考考點的考查,題目難度中等.


 手拉手全優練考卷系列答案
手拉手全優練考卷系列答案科目:高中化學 來源: 題型:選擇題
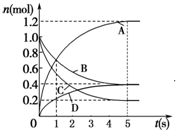 一定溫度下,向容積為2L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如圖所示,對該反應的推斷合理的是( )
一定溫度下,向容積為2L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如圖所示,對該反應的推斷合理的是( )| A. | 該反應的化學方程式為6A+2 D?3B+4C | |
| B. | 反應進行到1 s時,v(A)=v(B) | |
| C. | 反應進行到5 s時,B的平均反應速率為0.06mol/(L•s) | |
| D. | 反應進行到5 s時,v(A)=v(B)=v(C)=v(D) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.37 | B. | 0.24 | C. | 0.16 | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇和汽油都是可再生能源,應大力推廣使用乙醇汽油 | |
| B. | 凡含有食品添加劑的食物對人體健康均有害,不宜食用 | |
| C. | PM2.5主要來自于煤和石油等化石燃料的燃燒 | |
| D. | 汽車尾氣中的一氧化氮遇空氣在低溫下能自發進行反應,說明該反應的△H>O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷不能使酸性高錳酸鉀溶液褪色,而甲苯能使酸性高錳酸鉀溶液褪色 | |
| B. | 乙醇能發生消去反應,而乙烷不能發生消去反應 | |
| C. | 苯與硝酸在加熱的條件下發生取代反應,而甲苯在常溫下就能與硝酸發生硝化反應 | |
| D. | 乙烷在光照條件下能發生取代反應,而乙炔不能發生取代反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
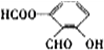 、
、 、
、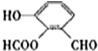 ..
..查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com