
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1| A.使用高效催化劑 | B.降低反應溫度 |
| C.增大體系壓強 | D.不斷將CH3OH從反應混合物中分離出來 |
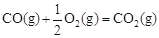 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1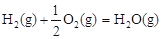 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1 CO2(g)+2H2O(g) △H=-651kJ·mol-1(3分)
CO2(g)+2H2O(g) △H=-651kJ·mol-1(3分)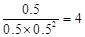 。
。 CH3OH(g)、②
CH3OH(g)、②
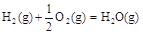 可知,②-①+③×2可得H3OH(g)+3/2O2(g)
可知,②-①+③×2可得H3OH(g)+3/2O2(g) CO2(g)+2H2O(g),所以反應熱是-283 kJ·mol-1+116 kJ·mol-1-242 kJ·mol-1×2=-651kJ·mol-1。
CO2(g)+2H2O(g),所以反應熱是-283 kJ·mol-1+116 kJ·mol-1-242 kJ·mol-1×2=-651kJ·mol-1。

科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
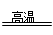 Si+2CO↑,其中氧化劑與還原劑的物質(zhì)的量之比為( )
Si+2CO↑,其中氧化劑與還原劑的物質(zhì)的量之比為( )| A.1 : 3 | B.3 : 1 | C.1 : 2 | D.2 : 1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.純堿 | B.濃硝酸 | C.燒堿溶液 | D.氫氟酸 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com