
 寒假天地重慶出版社系列答案
寒假天地重慶出版社系列答案科目:高中化學 來源: 題型:
 (2010?山東)硫一碘循環分解水制氫主要涉及下列反應:
(2010?山東)硫一碘循環分解水制氫主要涉及下列反應: H2+I2
H2+I2 2HI(g)的平衡常數K=
2HI(g)的平衡常數K=查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 I、下表是實驗室制備氣體的有關內容:
I、下表是實驗室制備氣體的有關內容:| 編號 | 實驗內容 | 實驗原理 | 發生裝置 |
| ① | 制氧氣 | H2O2→O2 | |
| ② | 制氨氣 | NH4Cl→NH3 | |
| ③ | 制氯氣 | HCl→Cl2 |
| ||
| ||


查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
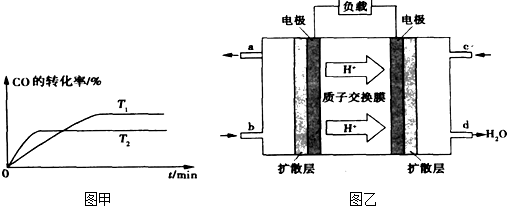
科目:高中化學 來源: 題型:閱讀理解
| 通電 |
| 加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:
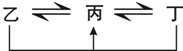 有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系:
有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com