
氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用.請回答下列問題:
(1)下圖是N2和H2反應生成2 mol NH3過程中能量變化示意圖,請計算每生成1 mol NH3放出熱量為________.

(2)在固定體積的密閉容器中,進行如下化學反應:N2(g)+3H2(g)![]() 2NH3(g),其化學平衡常數K與t的關系如下表:
2NH3(g),其化學平衡常數K與t的關系如下表:
請完成下列問題:
①試比較K1、K2的大小,K1________K2(填寫“>”“=”或“<”)
![]()
②下列各項能作為判斷該反應達到化學平衡狀態的依據的是________(填序號字母).
A.容器內N2、H2、NH3的濃度之比為1∶3∶2
B.2v(N2)(正)=v(H2)(逆)
C.容器內壓強保持不變
D.混合氣體的密度保持不變
(3)鹽酸肼(N2H6Cl2)是一種重要的化工原料,屬于離子化合物,易溶于水,溶液呈酸性,水解原理與NH4Cl類似.
①寫出鹽酸肼第一步水解反應的離子方程式________.
②鹽酸肼水溶液中離子濃度的關系表示正確的是________(填序號).
A
.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)B.c(Cl-)>c([N2H5·H2O]+)>c(OH-)>c(H+)
C.2c(N2H62+)+c([N2H5·H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-)
科目:高中化學 來源: 題型:閱讀理解
 氮是地球上含量豐富的元素,氮及其化合物的研究在生產、生活中有著重要意義.
氮是地球上含量豐富的元素,氮及其化合物的研究在生產、生活中有著重要意義.| 1 |
| 2 |
| 3 |
| 2 |
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
| C4(NO)C6(H2O) |
| C4(NH3)C5(O2) |
| C4(NO)C6(H2O) |
| C4(NH3)C5(O2) |
| 催化劑 |
| 高溫高壓 |
| 容器 編號 |
起始時各物質的物質的量/mol | 反應達平衡時的焓變/kJ?mol-1 | ||
| N2 | H2 | NH3 | ||
| A | 1 | 3 | 0 | △H1=-23.1 |
| B | 0.9 | 2.7 | 0.2 | △H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
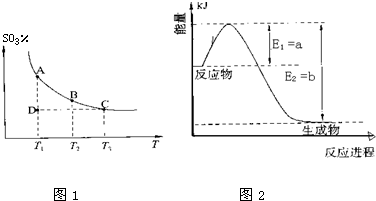
| ||
| 高溫 |
| ||
| 高溫 |
| 4 |
| 7 |
| ||
| 高溫 |
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
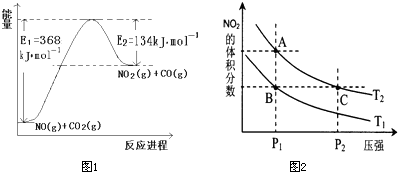
| T/K | 298 | 398 | 498 |
| 平衡常數K | 2.44ⅹ10-6 | K1 | K2 |
| 9 |
| 10 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| t/(K) | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
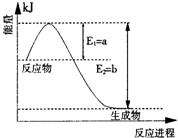
| 催化劑 |
| 高溫高壓 |
| ||
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com