
【題目】根據實驗內容填空:
(1)工業上用鐵質容器盛裝冷的濃硫酸(填“能”或“不能”).為研究鐵質材料與熱濃硫酸的反應,某學習小組進行了以下探究活動:
(2)[探究一] 將已去除表面氧化物的鐵釘(碳素鋼)放入15.0mL濃硫酸中,加熱,充分反應后得到溶液X并收集到氣體Y.
①甲同學認為X中除Fe3+外還可能含有Fe2+ . 若要確認其中的Fe2+ , 應選用
a.KSCN溶液 b.鐵粉和KSCN溶液 c.濃氨水 d.酸性KMnO4溶液
②乙同學取336mL(標準狀況)氣體Y通入足量溴水中,發生反應:SO2+Br2+2H2O=2HBr+H2SO4 , 用單線橋表示電子轉移情況 ,
然后加入足量BaCl2溶液,經適當操作后得干燥固體2.33g.由此推知氣體Y中SO2的體積分數為 .
(3)[探究二] 分析上述實驗中SO2體積分數的結果,丙同學認為氣體Y中還可能含量有H2和CO2氣體.為此設計了下列探究實驗裝置(圖中夾持儀器省略).
裝置B中試劑的作用是 .
(4)認為氣體Y中還含有CO2的理由是(用化學方程式表示).
(5)為確認CO2的存在,需在裝置中添加M于,M中盛裝的是(選填序號). a.A之前,NaOH溶液 b.A﹣B間,NaOH溶液
c.B﹣C間,澄清石灰水 d.C﹣D間,澄清石灰水
(6)如果氣體Y中含有H2 , 預計實驗現象應是 .
【答案】
(1)能
(2)d; ![]() ;66.7%
;66.7%
(3)檢驗SO2是否除盡
(4)C+2H2SO4(濃) ![]() 2SO2↑+CO2↑+2H2O
2SO2↑+CO2↑+2H2O
(5)c
(6)D中氧化銅黑色粉末變紅,E中硫酸銅白色粉末變藍
【解析】解:(1)濃硫酸具有強的氧化性,常溫下遇到鐵發生鈍化,形成致密氧化膜阻止反應進行,工業上能用鐵質容器盛裝冷的濃硫酸
所以答案是:能;(2)①a.溶液中含有三價鐵離子,遇到硫氰酸鉀顯紅色,對二價鐵離子檢驗造成干擾,故a不選;
b.溶液中含有三價鐵離子硫氰酸鉀顯紅色,鐵和鐵離子反應生成亞鐵離子,不能檢驗出亞鐵離子,故b不選;
c.亞鐵離子和濃氨水反應生成白色沉淀,但不穩定,立即轉化為黃綠色最終轉化為紅褐色沉淀,鐵離子和濃氨水反應生成紅褐色沉淀,所以無論是否含有亞鐵離子,加入濃氨水都產生紅褐色沉淀,故c不選;
d.二價鐵離子具有強的還原性,能夠使酸性的高錳酸鉀褪色,三價鐵離子不具有還原性,不能使高錳酸鉀褪色,所以可以用來檢驗二價鐵離子,故d選;
所以答案是:d;
②SO2具有還原性,通入足量溴水中,發生SO2+Br2+2H2O=2HBr+H2SO4,用單線橋表示電子轉移情況的化學方程式為: ![]()
n(混合氣體)= ![]() =0.015mol,
=0.015mol,
SO2 → | BaSO4 |
1mol | 233g |
n | 2.33g |
n=0.01mol;
則 SO2的體積分數: ![]() ×100%=66.7%,
×100%=66.7%,
所以答案是:66.7%; ![]() ;(3)A除去二氧化硫,二氧化硫能使品紅溶液褪色,所以B可以檢驗A中是否完全除去二氧化硫,
;(3)A除去二氧化硫,二氧化硫能使品紅溶液褪色,所以B可以檢驗A中是否完全除去二氧化硫,
所以答案是:檢驗SO2是否除盡;(4)加熱條件下,C和濃硫酸反應生成二氧化碳,所以認為氣體Y中還含有CO2的理由的反應方程式為:C+2H2SO4(濃) ![]() 2SO2↑+CO2↑+2H2O,
2SO2↑+CO2↑+2H2O,
所以答案是:C+2H2SO4(濃) ![]() 2SO2↑+CO2↑+2H2O;(5)實驗室用澄清石灰水檢驗二氧化碳,但二氧化硫也能使澄清石灰水變渾濁,要檢驗二氧化碳應該排除二氧化硫的干擾,所以在確定不存在二氧化硫條件下,將氣體通入澄清石灰水檢驗是否含有二氧化碳,該檢驗裝置應該在B﹣C之間,
2SO2↑+CO2↑+2H2O;(5)實驗室用澄清石灰水檢驗二氧化碳,但二氧化硫也能使澄清石灰水變渾濁,要檢驗二氧化碳應該排除二氧化硫的干擾,所以在確定不存在二氧化硫條件下,將氣體通入澄清石灰水檢驗是否含有二氧化碳,該檢驗裝置應該在B﹣C之間,
所以答案是:c;(6)氫氣具有還原性,能還原性,能還原黑色的氧化銅生成紅色的銅單質,同時生成水,水能使無水硫酸銅變藍色,這是檢驗水的特征反應,所以如果D中氧化銅變紅,E中無水硫酸銅變藍,則證明含有氫氣,
所以答案是:D中氧化銅黑色粉末變紅,E中硫酸銅白色粉末變藍.


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
【題目】金屬鈉與水反應:2Na+2H2O→2Na++2OH-+H2↑,關于該反應過程的敘述錯誤的是( )
A.生成了離子鍵B.破壞了極性共價鍵
C.破壞了金屬鍵D.形成非極性共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能夠達到實驗目的是( ) 
A.實驗室采用圖①所示裝置收集SO2
B.除去NaHCO3溶液中的Na2CO3 , 可加入Ca(OH)2溶液后過濾
C.稱取0.40 g NaOH,置于100 mL容量瓶中,加水溶解,配制0.10 mol/L NaOH溶液
D.可用圖②所示裝置比較KMnO4、Cl2、S的氧化性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟他胺G是一種可用于治療腫瘤的藥物.實驗室由芳香烴A制備G的合成路線如下: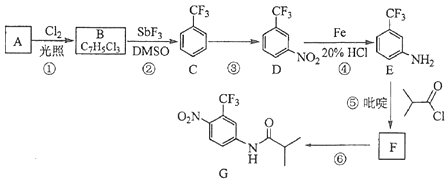
回答下列問題:
(1)A的結構簡式為 . C的化學名稱是 .
(2)③的反應試劑和反應條件分別是 , 該反應的類型是 .
(3)⑤的反應方程式為 . 吡啶是一種有機堿,其作用是 .
(4)G的分子式為 .
(5)H是G的同分異構體,其苯環上的取代基與G的相同但位置不同,則H可能的結構有種.
(6)4﹣甲氧基乙酰苯胺( ![]() )是重要的精細化工中間體,寫出由苯甲醚(
)是重要的精細化工中間體,寫出由苯甲醚( ![]() )制備4﹣甲氧基乙酰苯胺的合成路線(其他試劑任選).
)制備4﹣甲氧基乙酰苯胺的合成路線(其他試劑任選).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據問題填空:
(1)在實驗室中,常使氣體通過干燥劑①濃硫酸②堿石灰,達到干燥氣體的目的.干燥下列氣體可選擇所列出的哪種干燥劑(填序號) SO2NH3Cl2
(2)在氮的單質和常見化合物中: 常用作保護氣(如填充燈泡)的物質是 , 常用作制冷劑的物質是 .
(3)舍勒將軟錳礦與濃鹽酸混合加熱,在世界上首先制得了氯氣.反應的離子方程式為: .其中,氧化劑是 . 高錳酸鉀是強氧化劑,用高錳酸鉀與濃鹽酸混合在常溫下即可反應生成氯氣,從反應條件分析,高錳酸鉀與二氧化錳誰的氧化性更強? .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學已經滲透到人類生活的各個方面,下列說法正確的是
A.垃圾焚燒不僅可以用于發電,還不會帶來任何新污染
B.喂養雞的過程中大量使用抗生素,大量進食這樣的雞肉對人體健康有益
C.油脂在人體內水解為氨基酸和甘油等小分子被吸收
D.銅具有良好的導電性,常用來制作印刷電路板
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫是一種應用范圍極廣的過氧化物,根據題意,回答下列有關問題:
(1)請舉出H2O2的一種用途 .
(2)H2O2是一種二元弱酸,請寫出它的第一步電離方程式 .
(3)將H2O2溶液加入鹽酸酸化的FeCl2溶液中,溶液由淺綠色變為棕黃色,寫出該反應的離子方程式并標出電子轉移情況 .
(4)向盛有少量過氧化鈉固體的試管中滴加水,直到氣體不再放出,再加水稀釋所得溶液,將得到的溶液平均分成兩份盛放在兩只試管中,進行下列實驗:①一只試管中滴加酚酞試液,溶液變紅.半分鐘紅色褪去;②另一只試管中加入少量二氧化錳.又有氣體放出,待氣體不再放出,再滴加酚酞,溶液變紅,持久不褪色.上述實驗表明,過氧化鈉和水反應可分兩步,其化學方程式為: 第一步:;第二步 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com