
【題目】某汽車安全氣囊的產氣藥劑主要含有NaN3、Fe2O3、KClO4等物質。當汽車發生碰撞時,產氣藥劑產生大量氣體使氣囊迅速膨脹,從而起到保護作用。
(1)NaN3是氣體發生劑,其中N的化合價為________,是_____________(用“電解質”或者“非電解質”填空)。NaN3受熱分解產生N2和Na,則該反應方程式為: ________。已知常溫常壓下氣體摩爾體積為24.5L/mol,則在常溫常壓下,反應130g NaN3能產生_____________L的N2。
(2)Fe2O3是主氧化劑,與Na反應生成的還原產物為________________(已知該反應為置換反應)。若已知2.3gNa完全反應,轉移的電子物質的量為____________。
(3)KClO4是助氧化劑,反應過程中與Na作用生成KC1和Na2O,請用單線橋表示該反應電子轉移:KClO4+8Na= KCl+4Na2O_____________________
【答案】![]() 電解質 2NaN3
電解質 2NaN3![]() 2Na+3N2↑ 73.5 Fe 0.1mol
2Na+3N2↑ 73.5 Fe 0.1mol 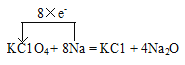
【解析】
(1) NaN3是鹽,屬于電解質;由于Na元素的化合價是+1價,根據化合物中正負化合價的代數和等于0,可知其中N元素的化合價為![]() 價;NaN3是氣體發生劑,受熱分解產生Na和N2,方程式為2NaN3
價;NaN3是氣體發生劑,受熱分解產生Na和N2,方程式為2NaN3![]() 2Na+3N2↑;130g NaN3的物質的量是n(NaN3)=130g÷65g/mol=2mol,根據方程式可知:2mol NaN3反應會產生3molN2,由于在常溫常壓下氣體摩爾體積為24.5L/mol,所以產生的氮氣在常溫常壓下的體積為V(N2)=3mol×24.5L/mol=73.5L;
2Na+3N2↑;130g NaN3的物質的量是n(NaN3)=130g÷65g/mol=2mol,根據方程式可知:2mol NaN3反應會產生3molN2,由于在常溫常壓下氣體摩爾體積為24.5L/mol,所以產生的氮氣在常溫常壓下的體積為V(N2)=3mol×24.5L/mol=73.5L;
(2)Fe2O3是主氧化劑,與Na發生置換反應,Fe元素發生還原反應,還原產物為Fe,Na是還原劑,氧化產物是Na2O;2.3gNa的物質的量是0.1mol,Na是+1價的金屬,所以轉移的電子物質的量為0.1mol;
(3) Cl元素的化合價由反應前KClO4中的+7變為反應后KCl中的-1價,化合價降低,得到電子8e-;Na元素的化合價由反應前單質Na的0價變為反應后Na2O中的+1價,化合價升高,失去電子8×e-,用單線橋表示該反應電子轉移為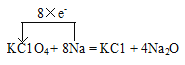 。
。


科目:高中化學 來源: 題型:
【題目】冶煉金屬一般有以下幾種方法:①熱分解法;②焦炭法;③水煤氣法(CO或H2);④活潑金屬置換法;⑤電解法。這幾種方法各有優缺點,它們在工業上均有應用。古代有:a.火燒孔雀石煉銅;b.濕法煉銅;現代有:c.鋁熱法煉鐵;d.光鹵石法煉鎂。對它們的冶煉方法分析不正確的是
A. a用② B. b用③ C. c用④ D. d用⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組采用如下裝置用環己醇制備環己烯。
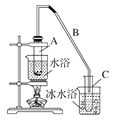
已知:環己醇和濃硫酸混合在85 ℃下制取環己烯。
密度(g/cm3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
環己醇 | 0.96 | 25 | 161 | 能溶于水 |
環己烯 | 0.81 | -103 | 83 | 難溶于水 |
(1)制備粗品
將12.5 mL環己醇加入試管A中,再加入1 mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,在試管C內得到環己烯粗品。
①A中碎瓷片的作用是________,導管B除了導氣外還具有的作用是____________。
②試管C置于冰水浴中的目的是____________________________________________。
(2)制備精品
①環己烯粗品中含有環己醇和少量酸性雜質等。加入飽和食鹽水,振蕩、靜置、分層,環己烯在________層(填“上”或“下”),分液后用________(填入編號)洗滌。
A. KMnO4溶液 B. 稀硫酸 C. Na2CO3溶液
②再將環己烯按如圖裝置蒸餾,冷卻水從________口進入。蒸餾時要加入生石灰,目的是__________________________________________。
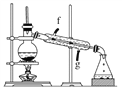
③收集產品時,控制的溫度應在________左右,實驗制得的環己烯精品質量低于理論產量,可能的原因是____________。
a. 蒸餾時從70℃開始收集產品
b. 環己醇實際用量多了
c. 制備粗品時環己醇隨產品一起蒸出
(3)以下區分環己烯精品和粗品的方法,合理的是___________;如果得實際得到產品質量為8.2 g, 則該實驗的產率是_________________(保留3位有效數字)。
a. 用酸性高錳酸鉀溶液 b. 用金屬鈉 c. 測定沸點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是某品牌飲用礦泉水標簽的部分內容。下列說法正確的是

A. 標簽上離子的濃度是物質的量濃度
B. 由礦泉水制蒸餾水必需使用的玻璃儀器有:圓底燒瓶、酒精燈、溫度計、冷凝管、牛角管和錐形瓶
C. 該品牌飲用礦泉水中c(Mg2+)最大值為2×10-4mol/L
D. 一瓶該品牌飲用礦泉水中SO42-的物質的量不超過l×10-5mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)純凈物可根據其組成和性質進行分類。如圖所示的分類方法屬于___________(填字母)。
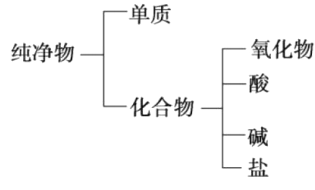
A.交叉分類法 B.樹狀分類法
(2)人們以______________________為分類標準分出溶液、膠體和濁液三種體系。實驗室制備Fe(OH)3膠體的實驗步驟是:________________________________________________________________________,請寫出實驗室制備Fe(OH)3膠體的化學方程式:_________________________________。
(3)以H、O、S、N幾種元素中任意兩種或三種元素組成合適的常見物質,分別將其中一種常見物質的化學式填在下表相應類別中:
物質類別 | 非含氧酸 | 堿 | 酸式鹽 | 酸性氧化物 |
化學式 | ______ | _____ | ____ | _____ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4H2SO4,⑨NH3·H2O,請回答下列問題:
(1)若濃度均為0.1mol·L-1、等體積的NaOH和NH3·H2O分別加水稀釋m倍、n倍,
稀釋后兩種溶液的pH都變成9,則m_______n (填“>”、“<”或“=”)。
(2)已知水存在如下平衡:H2O+H2O![]() H3O++OH-△H>0,現欲使平衡向右移動,且所得溶液顯酸性,選擇的下列方法是_______。
H3O++OH-△H>0,現欲使平衡向右移動,且所得溶液顯酸性,選擇的下列方法是_______。
A.向水中加入NaHSO4固體 B.向水中加NaHCO3固體
C.加熱至100℃ [其中c (H+) =1×10-6 mol·L-1] D.向水中加入NH4Cl固體
(3)常溫下,pH=11的CH3COONa溶液中,水電離出來的c(OH-)=_______;在pH=3的CH3COOH溶液中,水電離出來的c(H+)=_______。
(4)NH4Cl溶液中離子濃度大小順序為______________。
(5)物質的量濃度相同的⑥、⑦、⑧、⑨四種稀溶液中,NH4+濃度由大到小的順序是(填序號)_______。
(6)己知t℃時,Kw=1×10-12,在該溫度時將pH=9的NaOH溶液a L與pH=2的H2SO4溶液bL混和(忽略混合后溶液體積的變化),若所得混合溶液的pH=3,則出a∶b=_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,下列說法正確的是( )
A. 常溫常壓下,11.2L CO2所含的原子數為1.5NA
B. 標準狀況下,22.4L H2和N2的混合物中所含原子數為NA
C. 標準狀況下,11.2L SO3 中含有2NA個原子
D. 3mol單質Fe完全轉變為Fe3O4,失去8NA個電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示實驗裝置,下列說法不正確的是
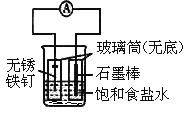
A. 裝置為鐵的吸氧腐蝕實驗
B. 一段時間后,向插入石墨棒的玻璃筒內滴入石蕊試液,可觀察到石墨附近的溶液變紅
C. 一段時間后,向插入鐵釘的玻璃筒內滴入NaOH溶液,即可觀察到鐵釘附近的溶液有沉淀出現
D. 若將裝置中飽和食鹽水換成稀硫酸,裝置為析氫腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組以廢鐵屑、稀硫酸、飽和(NH4)2SO4溶液為原料,經過一系列反應和操作后,合成了淺藍綠色晶體X。為確定其組成,進行如下實驗:
Ⅰ.結晶水的測定:稱取7.84 g淺藍綠色晶體,加熱至100 ℃失去結晶水,冷卻至室溫后,稱重,質量為5.68 g。
Ⅱ.NH4+的測定:將上述5.68 g固體置于如圖所示的三頸瓶中,然后逐滴加入足量10%的NaOH溶液,通入氮氣,用40.00 mL 1 mol·L-1的硫酸溶液吸收產生的氨氣。吸收氨氣結束后取下接收瓶,用2 mol·L-1NaOH標準溶液滴定過剩的硫酸,到終點時消耗20.00 mL NaOH溶液。
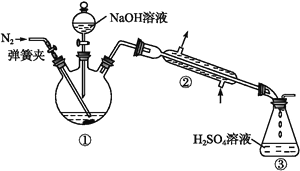
Ⅲ.鐵元素的測定:將上述實驗結束后三頸瓶中的溶液全部倒入錐形瓶中,向其中加入適量3%的H2O2溶液,充分振蕩后濾出沉淀,洗凈、干燥、灼燒后;測得其質量為1.6 g。回答下列問題:
(1)在實驗Ⅰ中,不可能用到的實驗儀器是_____(填正確答案標號)。
A.燒杯 B.鐵架臺(帶鐵圈) C.坩堝 D.蒸發皿 E.酒精燈 F.干燥器 G.托盤天平
(2)在實驗Ⅱ中,通入氮氣的目的是____________。吸收氨氣結束后,為了減少實驗誤差,還需要對直形冷凝管進行“處理”,“處理”的操作方法是_______________。
(3)在實驗Ⅱ中,用NaOH標準溶液滴定過剩的硫酸時,應使用_______式滴定管;可使用的指示劑為_______________。
(4)在實驗中,檢驗沉淀是否洗凈的方法是____________________。
(5)根據上述實驗數據計算,該淺藍綠色晶體的化學式為________。三頸瓶中發生反應的離子方程式為_____________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com