
【題目】火力發電廠釋放的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會造成環境污染和溫室效應。對燃煤廢氣進行脫硝、脫硫和脫碳等處理,可實現節能減排、廢物利用等目的。
(1)脫硝:利用CH4催化還原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=1160kJ·mol-1
CH4直接將NO2還原為N2的熱化學方程為___。
(2)脫碳:將CO2轉化為甲醇(CH3OH)的熱化學方程式如下:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);ΔH3
CH3OH(g)+H2O(g);ΔH3
①取五份等體積的CO2和H2的混合氣體(物質的量之比均為1∶3),分別加入溫度不同、容積相同的恒容密閉容器中,發生上述反應,反應相同時間后,測得甲醇的體積分數φ(CH3OH)與反應溫度T的關系曲線如圖所示,則上述反應的ΔH3____0(填“>”“<”或“=”);
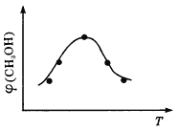
②在一個恒溫恒容密閉容器中充入1molCO2和3molH2,進行上述反應。測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
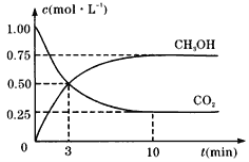
試回答:
0~10min內,CO2的平均反應速率為___mol·L1·min1;該溫度下,反應的平衡常數的值為___(結果保留一位小數);第10min后,若向該容器中再充入1molCO2和3molH2,則再次達到平衡時CH3OH(g)的體積分數____(填“增大”、“減小”或“不變”)。
(3)脫硫:①某種脫硫工藝將廢氣經處理后,與一定量的氨氣、空氣反應,生成硫酸銨和硝酸銨的混合物作為副產品化肥。設參與反應的SO2、NO2的物質的量之比為1∶1,則該反應的化學方程式為___。
②硫酸銨和硝酸銨的水溶液pH<7,其原因用離子方程式表示為___。在一定物質的量濃度的硝酸銨溶液中滴加適量的NaOH溶液,使溶液的pH=7,則溶液中:c(Na+)+c(H+)___c(NO3)+c(OH)(填“>”、“<”或“=”)。
【答案】CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol或2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g) △H=-1734kJ/mol < 0.075 5.3 增大 12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3 NH4++H2O![]() NH3H2O+H+ <
NH3H2O+H+ <
【解析】
(1)根據蓋斯定律,將兩個方程式通過如下變換(①+②)![]() 得到目標熱化學方程式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH =
得到目標熱化學方程式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH =![]() (-574kJ·mol-1-1160kJ·mol-1)=-867 kJ/mol;
(-574kJ·mol-1-1160kJ·mol-1)=-867 kJ/mol;
(2)①根據圖象分析知道:溫度升高,甲醇的體積分數φ(CH3OH)減小,平衡逆向移動,所以反應是放熱的,即ΔH<0;
②0-10min內,二氧化碳的平均反應速率v=![]() =0.075 mol·L-1·min-1;
=0.075 mol·L-1·min-1;
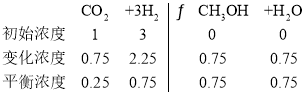
反應常數K=![]() =5.3;
=5.3;
向該容器中再充入1mol CO2和3mol H2,會使得壓強增大,平衡正向移動,所以再次達到平衡時CH3OH(g)的體積分數增大;
(4)①根據題目參與反應的SO2、NO2的物質的量之比為1∶1,二者與氨氣和空氣反應的化學方程式為12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3;
②硝酸銨溶液中滴加適量的NaOH溶液,使溶液的pH=7,溶液中存在電荷守恒:c(Na+)+c(H+)+c(NH4+)=c(NO3-)+c(OH-),則c(Na+)+c(H+)<c(NO3-)+c(OH-)。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】為探究二元化合物X的組成和性質,某研究小組設計并完成了如下實驗(步驟中所加試劑均過量,部分產物已略去)。
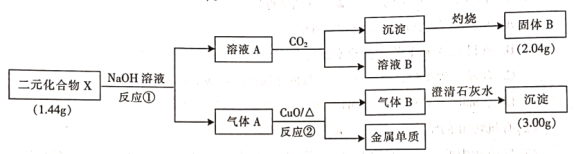
請回答下列問題:
(1)寫出X中含有的元素________(用元素符號表示)。
(2)寫出反應①的離子方程式___________。
(3)寫出反應②的化學方程式___________。
(4)設計實驗檢驗溶液B中所含溶質的陰離子:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A是一種常見的一種金屬,F是一種紅褐色的沉淀。試根據圖中轉化關系,回答下列問題。
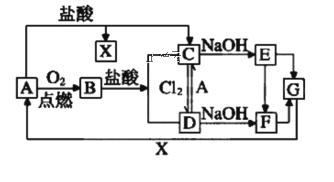
(1)寫出A、B、D、E的化學式:A___、B___、D___、E___。
(2)檢驗D中陽離子的方法:___。
(3)保存C溶液時為什么加固體A___。
(4)寫出下列轉化的離子方程式
①C→E___。
②A→C___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是硫酸試劑瓶標簽上的內容:

(1)某化學興趣小組進行硫酸性質的實驗探究時,需要490mL0.92mol·L-1的稀硫酸,現要配制該濃度的溶液所需的玻璃儀器除量筒、燒杯、玻璃棒、膠頭滴管外,還需要__(填儀器名稱);需要量取98%濃硫酸__mL進行配制;
(2)配制溶液時有如下操作:a.稀釋溶解b.搖勻c.洗滌d.冷卻e.量取f.將溶液移至容量瓶g.定容,實驗操作順序正確的是(_____)
A.e→a→f→d→c→f→g→b B.e→a→d→f→c→f→g→b
C.e→a→f→d→c→f→b→g D.e→a→d→f→c→f→b→g
(3)在配制0.92mol·L-1稀硫酸的過程中,下列情況會引起配制所得的硫酸溶液物質的量濃度偏低的是__;
A.未經冷卻趁熱將溶液注入容量瓶中 B.量取濃硫酸時仰視讀數
C.定容時俯視觀察液面 D.未洗滌燒杯和玻璃棒
(4)為中和100mL2.3mol·L-1KOH溶液使其恰好完全反應,需要加入__mL0.92mol·L-1稀硫酸。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請按要求作答:
(1)請根據官能團的不同對下列有機物進行分類:
① ![]() ②
② ![]() ③
③ ![]() ④
④ ![]()
⑤ ![]() ⑥
⑥![]() ⑦
⑦![]()
Ⅰ.酚:________酮:________醛:________(填序號);
Ⅱ.④的官能團的名稱為______、⑦的官能團的名稱為______;
(2)分子式為C4H8且屬于烯烴的有機物的同分異構體(不考慮順反異構)有 ____種; 高聚物的單體的結構簡式是_________。
高聚物的單體的結構簡式是_________。
(3)![]() 的名稱為:_____________;寫出
的名稱為:_____________;寫出![]() 聚合生成高分子化合物的化學方程式__________________________________;
聚合生成高分子化合物的化學方程式__________________________________;
(4)鍵線式![]() 表示的分子式為___________;與其互為同分異構體且一氯代物有兩種的烴的結構簡式____________________;
表示的分子式為___________;與其互為同分異構體且一氯代物有兩種的烴的結構簡式____________________;
(5)籃烷分子的結構如圖所示:
![]()
①籃烷的分子式為:________,其一氯代物有______種;
②若使1mol該烴的所有氫原子全部被氯原子取代,需要_____mol氯氣。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從甲苯出發,按下面流程可以合成苯甲酸苯甲酯和水楊酸。
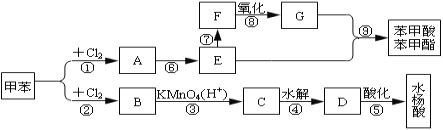
已知水楊酸的結構簡式為![]() 且酚羥基易被氧化。請回答:
且酚羥基易被氧化。請回答:
(1)寫出下列反應的條件:①_____________、②_______;
(2)C、F的結構簡式分別為:C___、F___;
(3)寫出反應⑥、⑨的化學方程式:⑥________________⑨_____
(4)寫出反應類型:②____________ ⑥____________ ⑨______________
(5)③、④兩步反應能否互換,為什么?___。
(6)寫出水楊酸的同分異構體中屬于酯的結構簡式_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用含砷氧化銅礦[含CuO、Cu2(OH)2CO3、As2O3及重金屬鹽等]制取Cu2(OH)2SO4的工藝流程如下:
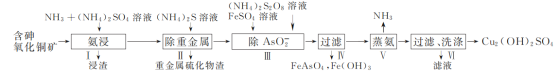
(1) 步驟Ⅰ“氨浸”時,控制溫度為50~55 ℃,pH約為9.5,含銅化合物轉化為[Cu(NH3)4]SO4溶液。
① CuO被浸取的離子方程式為________。
②浸取溫度不宜超過55 ℃,其原因是________。
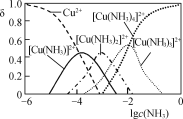
③ Cu2+與NH3結合時,溶液中含銅微粒的物質的量分布分數(δ)與溶液中游離的c(NH3)的對數值的關系如圖所示。若用1 L浸取液(由等物質的量NH3和NH4+組成)將amolCu2(OH)2CO3全部浸出為[Cu(NH3)4]2+(CO32-轉變為HCO3-,不考慮其他反應,溶液體積變化忽略不計),原浸取液中起始時c(NH3)應滿足的條件是________。
(2) “除AsO2-”時,FeSO4需過量,一方面使AsO2-沉淀完全,另一目的是________。
(3) “蒸氨”時發生反應的化學方程式為________。
(4) 為了實現生產過程中物質循環利用,可采取的措施為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有效去除廢水中的H2SiF6、F-,改善水質是環境部門的重要研究課題。
(1)AlF3是有機合成中常用催化劑,利用廢水中的H2SiF6可轉變制得,相關的熱化學方程式如下:
3H2SiF6(aq)+2Al(OH)3(s)=Al2(SiF6)3(aq)+6H2O(l);ΔH=akJ·mol-1
Al2(SiF6)3(aq)+6H2O(l)=2AlF3(aq)+3SiO2(s)+12HF(aq);ΔH=bkJ·mol-1
3HF(aq)+Al(OH)3(s)=AlF3(aq)+3H2O(l);ΔH=ckJ·mol-1
則反應H2SiF6(aq)+2Al(OH)3(s)=2AlF3(aq)+SiO2(s)+4H2O(l)的ΔH=__kJ·mol-1。
(2)廢水的酸堿度及廢水中的Fe3+對F-濃度的測定都會產生一定的影響。
①測定時,通常控制廢水的pH在5~6之間。pH過小所測F-濃度偏低,其原因是__。
②Fe3+與檸檬酸根(C6F5O73-)、F-反應可表示為Fe3++nC6H5O73-![]() Fe(C6H5O7)n(3n-3)-、Fe3++nF-
Fe(C6H5O7)n(3n-3)-、Fe3++nF-![]() FeFn(3-n)。向含有Fe3+的含氟廢水中加入檸檬酸鈉(C6H5O7Na3)可消除Fe3+對F-測定的干擾,其原因是__。
FeFn(3-n)。向含有Fe3+的含氟廢水中加入檸檬酸鈉(C6H5O7Na3)可消除Fe3+對F-測定的干擾,其原因是__。
(3)利用聚苯胺可吸附去除水中F-。用惰性電極電解苯胺(![]() )和鹽酸的混合液可在陽極獲得聚苯胺薄膜,變化過程如圖:
)和鹽酸的混合液可在陽極獲得聚苯胺薄膜,變化過程如圖:
![]()
寫出陽極生成二聚體的電極反應方程式:___。
(4)利用MgCO3、Ca(OH)2和CaCO3等可沉淀去除廢水中F-。
①以MgCl2溶液、尿素[CO(NH2)2]為原料可制得MgCO3,寫出該反應的化學方程式:__。
②取三份相同的含F-的酸性廢水,分別加入足量的MgCO3、Ca(OH)2和CaCO3。相同時間后溶液的pH及F-殘留量如圖1所示。實際廢水處理過程中常選用MgCO3的理由是:__。
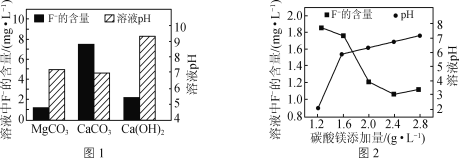
③改變碳酸鎂添加量,處理后廢水中F-含量及溶液pH的變化如圖2所示。添加量超過2.4g·L-1后,F-含量略有升高的原因是___。{Ksp(MgF2)=7.4×10-11,Ksp[Mg(OH)2]=5.6×10-12}
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在某2 L恒容密閉容器中加入納米級氧化亞銅并通入0.1 mol 水(g),發生如下反應:2H2O(g)![]() 2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同時間產生O2的物質的量見下表:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同時間產生O2的物質的量見下表:

下列說法不正確的是( )
A. 前20 min內的平均反應速率v(H2O)=5×10-5mol·L-1·min-1
B. 達到平衡時,需要從外界吸收的能量為0.968 kJ
C. 增大水的濃度,可以改變待反應的限度
D. 使用納米級的氧化亞銅,可以增大平衡時氧氣的體積分數
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com