
【題目】以重要的化工原料A(C2H2)合成有機物E和![]() 的路線如圖所示,部分反應條件及產物略去。其中D在一定條件下可被氧化成酮。
的路線如圖所示,部分反應條件及產物略去。其中D在一定條件下可被氧化成酮。
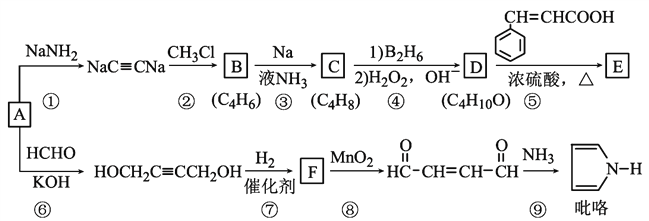
回答下列問題:
(1)B的系統命名是______;已知C是順式產物,則C的結構簡式為_______________。
(2)⑤的反應類型是_________________,E含有的官能團的名稱是________________。
(3)反應⑧產物與新制Cu(OH)2的化學方程式為____________________。
(4)符合下列條件肉桂酸(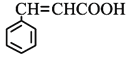 )的同分異構體共____種,分子中含有苯環和碳碳雙鍵,能夠發生銀鏡反應,遇FeCl3溶液顯紫色,寫出其中核磁共振氫譜圖有六組峰,且峰面積之比為1:1:1:1:2:2的結構簡式____________________
)的同分異構體共____種,分子中含有苯環和碳碳雙鍵,能夠發生銀鏡反應,遇FeCl3溶液顯紫色,寫出其中核磁共振氫譜圖有六組峰,且峰面積之比為1:1:1:1:2:2的結構簡式____________________
(5)參照上述合成路線,設計一條由丙炔和甲醛為起始原料制備![]() 的合成路線__________________________。
的合成路線__________________________。
【答案】 2-丁炔 ![]() 加成反應 碳碳雙鍵酯基
加成反應 碳碳雙鍵酯基 ![]() 16種 HO—
16種 HO—![]() — CH=CHCHO
— CH=CHCHO ![]()
【解析】試題分析:A分子式為C2H2,A是乙炔;根據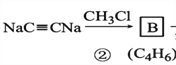 ,可推出B是CH3C
,可推出B是CH3C![]() CCH3;由
CCH3;由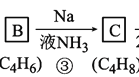 ,可知C是CH3C
,可知C是CH3C![]() CCH3;由CH3C
CCH3;由CH3C![]() CCH3生成D(C4H10O),D在一定條件下可被氧化成酮,D是CH3CH2CHOHCH3;
CCH3生成D(C4H10O),D在一定條件下可被氧化成酮,D是CH3CH2CHOHCH3;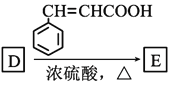 ,E是酯類,結構簡式為
,E是酯類,結構簡式為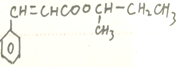
根據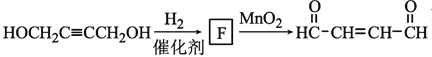 ,可知F是HOCH2CH=CHCH2OH。
,可知F是HOCH2CH=CHCH2OH。
解析:根據以上分析,(1)B是CH3C![]() CCH3,系統命名是2-丁炔;已知C是CH3C
CCH3,系統命名是2-丁炔;已知C是CH3C![]() CCH3, C順式結構簡式為
CCH3, C順式結構簡式為![]() 。
。
(2)![]()
![]() +H2O的
+H2O的
反應類型是取代反應(酯化反應),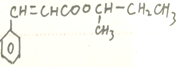 含有的官能團的名稱是碳碳雙鍵、酯基。
含有的官能團的名稱是碳碳雙鍵、酯基。
(3)反應⑧產物屬于醛類,與新制Cu(OH)2反應生成酸和磚紅色氧化亞銅,化學方程式為![]() 。
。
(4),分子中含有苯環和碳碳雙鍵,能夠發生銀鏡反應,說明含有醛基,遇![]() 溶液顯紫色,說明含有酚羥基,符合條件肉桂酸(
溶液顯紫色,說明含有酚羥基,符合條件肉桂酸(![]() )的同分異構體有
)的同分異構體有 (包括鄰、間、對3種)、
(包括鄰、間、對3種)、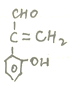 (包括鄰、間、對3種)、
(包括鄰、間、對3種)、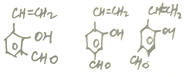 、
、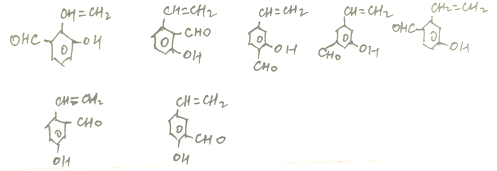
共16種,其中核磁共振氫譜圖有六組峰,且峰面積之比為1:1:1:1:2:2的結構簡式HO—![]() — CH=CHCHO
— CH=CHCHO
(5)根據上述合成路線,由丙炔和甲醛為起始原料制備![]()
的合成路線![]() 。
。


科目:高中化學 來源: 題型:
【題目】A、B、C、D、E五種短周期元素的原子序數依次增大。A和C,B和E同主族,C、D、E同周期。由A、B組成的兩種化合物甲和乙都為液態,甲中A、B原子數之比為2:1,乙中為1:1。由B、C組成的兩種化合物丙和丁都為固態,丙中C、B原子數之比為2:1,丁中為1:1。C、D、E的最高價氧化物對應的水化物兩兩之間均能發生反應,且均有甲生成,且A為原子半徑最小的短周期元素,丁為淡黃色固體。則:
(1)D的原子結構示意圖為:__________________
(2)A元素的單質為:_____________(填化學式);丁的電子式為:_____________
(3)E在周期表中的位置_________________________________
(4)C、D的最高價氧化物對應水化物發生反應的離子方程式為:
____________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】錳元素廣泛分布在自然界中,其單質和化合物在工農業生產中有著重要的應用。
(1)已知相關熱化學方程式為:
4Al(s)+3O2(g)=2Al2O2(s) △H1=a kJmol﹣1
3MnO2(s)=Mn3O4(s)+O2(g) △H2=bkJmol﹣1
3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) △H3=ckJmol﹣1
則3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) △H=__ kJmol﹣1(用含a、b、c的代數式表示).
(2)MnCO3廣泛用作錳鹽原料.通過如圖裝置焙燒MnCO3可以制取MnO2,反應方程式為:2MnCO3(s)+O2(g)═2MnO2(s)+2CO2(g)。
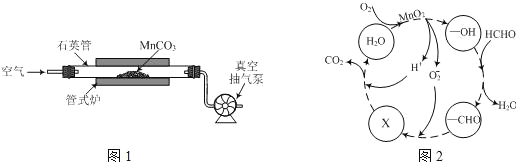
①2MnCO3(s)+O2(g)2MnO2(s)+2CO2(g)的化學平衡常數表達式K=______。
②用真空抽氣泵不斷抽氣的目的除保證反應持續進行外,還有______。
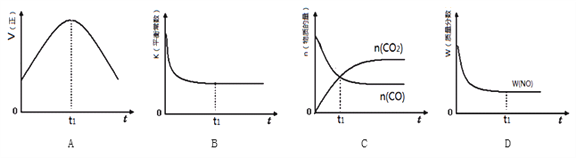
③若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是________(填序號)。(如圖中V正、K、n、w分別表示正反應速率、平衡常數、物質的量、質量分數)
(3)MnO2常用作催化劑。MnO2催化降解甲醛的反應機理如圖所示,圖中X表示的粒子是______,該反應的總反應方程式為______。
(4)MnSO4是重要微量元素肥料。用惰性電極電解MnSO4溶液可以制得更好活性的MnO2,電解時總反應的離子方程式為:______,電解過程中陰極附近的pH______(選填“增大”、“減小”或“不變”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在強酸性的無色溶液中能大量共存的離子組是( )
A.NH4+、Mg2+、SO42﹣、Cl﹣ B.Ba2+、K+、OH﹣、NO3﹣
C.Al3+、Cu2+、SO42﹣、Cl﹣ D.Na+、Ca2+、Cl﹣、HCO3﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【物質結構與性質】A、B、C、D為原子序數依次增大的四種元素,A2-和B+具有相同的電子構型;C、D為同周期元素,C核外電子總數是最外層電子數的3倍;D元素最外層有一個未成對電子。回答下列問題:
(1)四種元素中電負性最大的是____(填元素符號),其中C原子的核外電子排布式為______________;
(2)單質A有兩種同素異形體,其中沸點高的是___________(填分子式),原因是_________________;A和B的氫化物所屬的晶體類型分為______________和______________;
(3)C和D反應可生成組成比1:3的化合物E,E的立體構型為________________,中心原子的雜化軌道類型___________________;
(4)化合物D2A的立體構型為______________,中心原子的價層電子對數為_______________,單質D與濕潤的Na2CO3反應可制備D2A,其化學方程式為_____________________;
(5)A和B能夠形成化合物F,其晶胞結構如圖所示,晶胞參數a=0.566nm,F的化學式為_________,晶胞中A原子的配位數為__________,列式計算晶體F的密度_____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能在有機物的分子中引入羥基官能團的反應類型有:(a)酯化反應,(b)取代反應,(c)氧化反應,(d)加成反應,(e)水解反應。其中正確的組合有
A. (a)(b)(c) B. (d)(e) C. (b)(d)(e) D. (b)(c)(d)(e)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取100mL 0.3molL﹣1和300mL 0.25molL﹣1的硫酸注入500mL的容量瓶中,加水稀釋至刻度線,該混合溶液中H+的物質的量濃度是( )
A.0.21 molL﹣1
B.0.56 molL﹣1
C.0.42 molL﹣1
D.0.26 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制0.1molL﹣1NaCl溶液,下列操作會導致所配溶液的物質的量濃度偏高的是( )
A.稱量時,左盤低,右盤高 B.定容時俯視讀取刻度
C.原容量瓶洗凈后未干燥 D.定容時液面超過了刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的鹽酸,測得溶液中CO32-、HCO3-、AlO2-、Al3+的物質的量與加入鹽酸溶液的體積變化關系如圖所示,則下列說法正確的是( )

A.a曲線表示的離子方程式為AlO2-+H++H2O==Al(OH)3↓
B.原混合溶液中的CO32-與AlO2-的物質的量之比為1∶2
C.V1∶V2=l∶5
D.M點時生成的CO2為0.05 mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com