
【題目】在可逆反應2A(g)+3B(g) ![]() xC(g)+D(g)中,已知:反應開始加的物質只有A、B,起始濃度A為5 mol·L-1,B為3 mol·L-1,前2 min C的平均速率為0.5 mol·L-1·min-1。2 min末,測得D的濃度為0.5 mol·L-1。則關于此反應的下列說法中正確的是
xC(g)+D(g)中,已知:反應開始加的物質只有A、B,起始濃度A為5 mol·L-1,B為3 mol·L-1,前2 min C的平均速率為0.5 mol·L-1·min-1。2 min末,測得D的濃度為0.5 mol·L-1。則關于此反應的下列說法中正確的是
A. x=1
B. 2 min末時A和B的濃度之比為5∶3
C. 2 min末時B的濃度為1.5 mol·L-1
D. 前2 min,A的消耗濃度為0.5 mol·L-1
 導學全程練創優訓練系列答案
導學全程練創優訓練系列答案科目:高中化學 來源: 題型:
【題目】填空題
(1)濃H2SO4能夠用于干燥某些氣體,是由于它具有性;下列氣體能用濃硫酸來進行干燥的是(可多選,但只要有選錯項,即得0分) ①Cl2②H2S ③CO2④NH3
(2)濃H2SO4能使紙片變黑,是由于它具有性;
(3)濃H2SO4可以與Cu反應,是由于它具有強氧化性和性,化學學方程式是: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列措施符合“綠色化學”思想的是
A. 直接排放含磷生活污水
B. 大量使用氟里昂作為冰箱制冷劑
C. 使用可降解塑料代替不可降解塑料
D. 使用化學性質穩定、不易分解的有機氯農藥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖裝置所示,C、D、E、F、X、Y都是惰性電極,甲、乙中溶液的體積和濃度都相同(假設通電前后溶液體積不變),A、B為外接直流電源的兩極。將直流電源接通后,F極附近呈紅色。

請回答:
(1)B極是電源的___________ ,一段時間后,甲中溶液顏色 __________,丁中X極附近的顏色逐漸變淺,Y極附近的顏色逐漸變深,這表明___________ ,在電場作用下向Y極移動。
(2)若甲、乙裝置中的C、D、E、F電極均只有一種單質生成時,對應單質的物質的量之比為 ______________。
(3)現用丙裝置給銅件鍍銀,則H應該是______________ (填“鍍層金屬”或“鍍件”),電鍍液是___________ 溶液(填寫化學式)。當乙中溶液的pH是13時(此時乙溶液體積為500mL),丙中鍍件上析出銀的質量為_____________ ,甲中溶液的pH_____________(填“變大”、“變小”或“不變”)。
(4)若將C電極換為鐵,其他裝置都不變,則甲中發生總反應的離子方程式是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
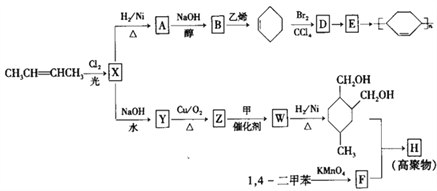
【題目】以烯烴為原料,合成某些高聚物的路線如下:
已知: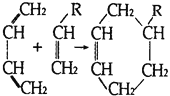 (或寫成
(或寫成![]() )
)
(1)CH3CH=CHCH3的名稱是____________。
(2)X中含有的官能團是______________。
(3)A→B的化學方程式是_____________。
(4)D→E的反應類型是_______________。
(5)甲為烴,F能與NaHCO3反應產生CO2。
①下列有關說法正確的是_______________。
a.有機物Z能發生銀鏡反應 b.有機物Y與HOCH2CH2OH互為同系物
c.有機物Y的沸點比B低 d.有機物F能與己二胺縮聚成聚合物
②Y的同分異構體有多種,寫出分子結構中含有酯基的所有同分異構體的種類數_____。
③Z→W的化學方程式是__________________。
(6)高聚物H的結構簡式是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】意大利羅馬大學的Fulvio Cacace等人獲得了極具理論研究意義的N4分子。N4分子結構如右圖,已知斷裂1mol N≡N鍵吸收942kJ熱量,生成1molN-N鍵釋放167kJ熱量根據以上信息和數據,下列熱化學方程式正確的是

A. 2N2 = N4 △H = -882kJ·mol-1
B. N2 (g) = 0.5N4 (g) △H = +441kJ
C. N2 (g) = 0.5N4 (g) △H = -441kJ·mol-1
D. 2N2(g) = N4(g) △H = +882 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】BaSO4在醫療上可做消化系統造影劑,2mol BaSO4含有的硫原子個數為
A. 2 B. 2×6.02×1023 C. 6 D. 6×6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】100mL 0.3mol/L Na2SO4溶液和50mL 0.2mol/L Al2(SO4)3溶液混合后,溶液中SO42﹣的物質的量濃度約為( )
A.0.20mol/L
B.0.25mol/L
C.0.4mol/L
D.0.5mol/L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com