
| 催化劑 |
| 高溫高壓 |
| 催化劑 |
| 高溫高壓 |
| 240g |
| 160g/mol |


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:閱讀理解
| 催化劑 |
| 高溫高壓 |
| 催化劑 |
| 高溫高壓 |
查看答案和解析>>
科目:高中化學 來源: 題型:
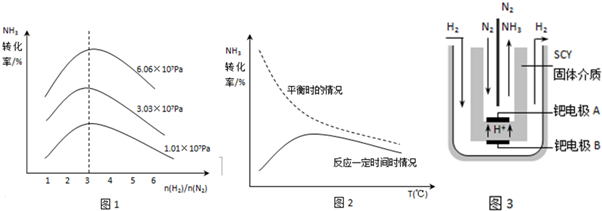
| 3 | 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
某一容積可變的密閉體系中發(fā)生下列反應:N2(g) + 3H2(g) ![]() 2NH3(g) + Q(Q>0),回答下列問題:
2NH3(g) + Q(Q>0),回答下列問題:
(1)對于合成氨工業(yè)生產條件的選擇,下列說法正確的是(選填字母序號) ;
A.溫度、壓強越大,越有利于化學平衡的正向移動;
B.鐵觸媒在該溫度時活性大;
C.工業(yè)生產受動力、材料、設備等條件的限制;
D.使用催化劑有利于提高反應的轉化率。
(2)下圖是某一時間段中反應速率與反應進程的關系圖:

①處于平衡狀態(tài)的時間段是 。
②在t1、t3、t4時刻,體系中分別是何種條件發(fā)生了什么樣變化?
t1: ,t3: , t4: 。
③在下列時間段中,氨的百分含量最高的是 (選填代號)。
a.t0~t1 b.t2~t3 c.t3~t4 d.t5~t6
查看答案和解析>>
科目:高中化學 來源:2011年北京市懷柔區(qū)高考化學適應性練習試卷(解析版) 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com