
| 電離能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1 817 | 2 745 | 11 578 |
| Y | 738 | 1 451 | 7 733 | 10 540 |
| Z | 496 | 4 562 | 6 912 | 9 543 |
 .
. 分析 (1)X、Y、Z為第三周期元素,X的I4電離能突然增大,說明最外層有3個電子,則X應為Al,Y的I3電離能突然增大,說明最外層有2個電子,則Y應為Mg,Z的I2電離能突然增大,說明最外層有1個電子,則Z應為Na,同周期元素從左到右元素的電負性逐漸增強,Mg價電子排布式為3s2完全充滿狀態,比Al穩定,所以Mg的第一電離能大于Al;
(2)A、B、C、D是周期表中前10號元素,它們的原子半徑依次減小.D能分別與A、B、C形成XYn型電子總數相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3雜化,則A、B、C、D分別為碳、氮、氧、氫,M為CH4、N為NH3、W為H2O.
①同周期隨原子序數增大,第一電離能呈增大趨勢,N元素2p能級為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素;
②同種元素之間形成非極性共價鍵,不同元素之間形成極性共價鍵,甲烷分子為正四面體構型,分子中正負電荷重心重合;
③氨分子間存在氫鍵;
④W為H2O,計算O原子價層電子對數、孤電子對數,確定VSEPR模型的空間構型、分子的空間構型;
⑤CN-離子中和N2分子中含有三鍵,三鍵有2個π鍵;
(3)E、F、G三元素的原子序數依次增大,三原子的核外的最外層電子排布均為4s1,則E為K、F為Cr、G為Cu.
解答 解:(1)X、Y、Z為第三周期元素,X的I4電離能突然增大,說明最外層有3個電子,則X應為Al,Y的I3電離能突然增大,說明最外層有2個電子,則Y應為Mg,Z的I2電離能突然增大,說明最外層有1個電子,則Z應為Na,
同周期元素從左到右電負性逐漸增強,則X、Y、Z的電負性從大到小的順序為Al>Mg>Na,因為元素Mg價電子排布式為3s2完全充滿狀態,比Al穩定,所以Mg的第一電離能大于Al,
故答案為:Al>Mg>Na;因為元素Mg價電子排布式為3s2完全充滿狀態,比Al穩定;
(2)A、B、C、D是周期表中前10號元素,它們的原子半徑依次減小.D能分別與A、B、C形成XYn型電子總數相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3雜化,則A、B、C、D分別為碳、氮、氧、氫,M為CH4、N為NH3、W為H2O.
①同周期隨原子序數增大,第一電離能呈增大趨勢,N元素2p能級為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素,故第一電離能:C<O<N,故答案為:C<O<N;
②M為甲烷,甲烷含有C-H極性共價鍵,分子構型為正四面體,分子中正負電荷重心重合,屬于非極性分子,故答案為:極性;非極性;
③N為氨,因為氨分子間存在氫鍵,因而易液化,故答案為:氨分子間存在氫鍵,因而易液化;
④W為H2O,中心原子氧原子含有孤對電子為$\frac{6-1×2}{2}$=2、價層電子對數為4,故水分子的VSEPR模型的空間構型為四面體,水分子的空間構型為V形,故答案為:四面體型;V形;
⑤CN-離子和N2分子中均含有三鍵,π鍵數目比為2:2=1:1,故答案為:1:1;
(3)E、F、G三元素的原子序數依次增大,三原子的核外的最外層電子排布均為4s1,則E為K、F為Cr、G為Cu.
①鉻元素的價電子排布式為3d54s1,故其化合物中最高化合價為+6價,故答案為:+6;
②Cu2+離子的核外電子排布式為1s22s22p63s23p63d9,Cu2+和NH3分子形成的配離子為[Cu(NH3)4]2+,其結構式為 ,
,
故答案為:1s22s22p63s23p63d9; .
.
點評 本題是對物質結構的考查,涉及電離能、電負性、化學鍵、氫鍵、分子構型、核外電子排布、配合物等,題目難度中等,需要學生具備扎實的基礎.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 短周期主族元素A、B、C、D、E、F的原子序數依次增大,已知A的原子半徑比B的小,B在反應中既不容易得到電子也不容易失去電子,C元素的氣態氫化物和其最高價氧化物對應水化物能化合生成鹽,元素D的原子最外層電子數是其電子層數的3倍,E與A同一主族,F常用于制半導體.
短周期主族元素A、B、C、D、E、F的原子序數依次增大,已知A的原子半徑比B的小,B在反應中既不容易得到電子也不容易失去電子,C元素的氣態氫化物和其最高價氧化物對應水化物能化合生成鹽,元素D的原子最外層電子數是其電子層數的3倍,E與A同一主族,F常用于制半導體.
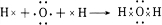 ,寫出A2D與X反應的化學方程式,并用單線橋標出電子轉移
,寫出A2D與X反應的化學方程式,并用單線橋標出電子轉移
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含NA個Na+的Na2O溶解于1L水中,Na+的物質的量濃度為1mo1•L-1 | |
| B. | 標準狀況下,22.4L水所含的分子數為NA | |
| C. | 常溫常壓下NO2和N2O4混合氣體22.4L,其中含有的原子總數為0.3NA | |
| D. | 常溫下,4gCH4含有NA個C-H共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | σ鍵是原子軌道以“頭碰頭”的方式相互重疊 | |
| B. | 共價化合物分子的鍵能越大,鍵長越長,則分子越穩定 | |
| C. | 2個原子形成多個共價鍵中,只有一個σ鍵,而π鍵可以是一個或多個 | |
| D. | 形成共價鍵時鍵與鍵重疊程度越大,體系能量越底,鍵越穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大容器的容積 | B. | 再充入一定量的N2O4 | ||
| C. | 分離出一定量的NO2 | D. | 再充入一定量的He |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .該物質屬于共價化合物(填“離子”或“共價”).向X的水溶液中滴加石蕊溶液,會觀察到:溶液變紅色.并用方程式解釋原因NH3+H2O=NH3.H2O?NH4++OH-.
.該物質屬于共價化合物(填“離子”或“共價”).向X的水溶液中滴加石蕊溶液,會觀察到:溶液變紅色.并用方程式解釋原因NH3+H2O=NH3.H2O?NH4++OH-.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 羅伯特•洛夫科維茨 | B. | 丹•謝赫特曼 | ||
| C. | 理查德•赫克 | D. | 托馬斯•施泰茨 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 根據某種原子的質量數可以確定該元素的相對原子質量 | |
| B. | H-N=C=O與H-O-C≡N互為同分異構體 | |
| C. | 化學鍵存在于化合物中,也可能存在于單質中 | |
| D. | 35Cl與37Cl是兩種不同的核素 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com