
| A. | 工業上常使用過量的空氣,目的是為了使SO2的轉化率達100% | |
| B. | 工業上選用V2O5作該反應的催化劑,目的是為了加快化學反應速率 | |
| C. | 工業上常選用常壓,原因是增大壓強不能改變該反應的化學反應速率 | |
| D. | 升高溫度可以加快反應速率,所以在工業生產中該反應溫度越高越好 |
分析 A、該反應是可逆反應,反應物不能完全轉化;
B、加入催化劑可以改變化學反應速率,根據工業生產選擇合適的催化劑;
C、增大壓強能加快化學反應速率;
D、升高溫度使得化學反應速率加快,但溫度過高反應轉換率低并且會使催化劑失效;
解答 解:A、可逆反應的反應物不能完全轉化,所以SO2的轉化率達不到100%,故A錯誤;
B、加入催化劑可以加快化學反應速率,故B正確;
C、增大壓強能加快化學反應速率,故C錯誤;
D、升高溫度使得化學反應速率加快,但溫度過高反應轉換率低并且會使催化劑失效,故D錯誤.
故選B.
點評 本題考查影響化學反應速率的因素:溫度、濃度、催化劑、壓強等,注意催化劑的特點是解題的易錯點,難度不大.


 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硫酸、濃硝酸、稀硝酸都是氧化性酸,常溫下都能使金屬鐵鈍化 | |
| B. | 濃硫酸與蔗糖混合攪拌產生刺激性氣味氣體,此過程只體現了濃硫酸的脫水性 | |
| C. | 某溶液中加鹽酸產生使澄清石灰水變渾濁的氣體,說明該溶液中一定含CO32- 或SO32- | |
| D. | 某溶液中滴加BaCl2.溶液產生不溶于稀硝酸的白色沉淀,不能說明該溶液中一定含SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH3+Cl2 $\stackrel{光照}{→}$CH3CH2Cl+HCl | |
| B. | CH2═CH2+HBr→CH3CH2Br | |
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{濃硫酸}$H3COOCH2CH3+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氮氣的電子式: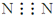 | |
| B. | 乙酸乙酯的結構簡式:C4H8O2 | |
| C. | O2-的結構示意圖: | |
| D. | 氫氧化鋇的電離方程式:Ba(OH)2═Ba2++(OH-)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com