
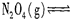


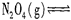
 當溫度升高時,氣體顏色變深,說明反應向正反應方向移動,即溫度升高,平衡向正反應方向移動,故該反應的正反應方向為吸熱反應;(2)1mol N2O4充入一恒壓密閉容器中,該反應為反應的分子數增多,恒壓,說明反應的體積逐漸增多,直到平衡,故氣體的密度變小,當達到平衡時,氣體的密度不變,故a正確;b中△H會發生變化,故b錯誤;達到平衡時反應物的反應速率與生成物的反應速率相等,故c錯誤,反應物的轉化率隨著反應的進行逐漸增多,當達到化學平衡時,轉化率為一定值,故d正確,故本題的答案選擇ad,溫度相同,故平衡常數不變,3s后NO2的物質的量為0.6mol,則參加反應的N2O4為0.3mol,所以v(N2O4)=0.3/1/3mol·L-1·s-1)=0.1mol·L-1·s-1。
當溫度升高時,氣體顏色變深,說明反應向正反應方向移動,即溫度升高,平衡向正反應方向移動,故該反應的正反應方向為吸熱反應;(2)1mol N2O4充入一恒壓密閉容器中,該反應為反應的分子數增多,恒壓,說明反應的體積逐漸增多,直到平衡,故氣體的密度變小,當達到平衡時,氣體的密度不變,故a正確;b中△H會發生變化,故b錯誤;達到平衡時反應物的反應速率與生成物的反應速率相等,故c錯誤,反應物的轉化率隨著反應的進行逐漸增多,當達到化學平衡時,轉化率為一定值,故d正確,故本題的答案選擇ad,溫度相同,故平衡常數不變,3s后NO2的物質的量為0.6mol,則參加反應的N2O4為0.3mol,所以v(N2O4)=0.3/1/3mol·L-1·s-1)=0.1mol·L-1·s-1。

 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源:不詳 題型:單選題
| A.恒T、P時,充入少量的NH3 | B.恒T、V時,充入少量的N2 |
| C.恒T、P時,充入少量的He | D.恒T、V時,充入少量的He |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.將5 mL 0.02 mol/L的H2SO4溶液與5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的體積為10 mL,則混合液的pH=2 |
| B.某物質的溶液中由水電離的c(H+) = 1×10-a mol/L,若a>7,則pH一定為14-a |
| C.pH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,c(Na+)大小關系:①>③>② |
| D.CH3COONa溶液中加入少量KNO3固體后的堿性溶液一定有: |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
| 實驗 序號 | 鐵的質量/g | 鐵的 形態 | V(H2SO4) /mL | c(H2SO4) /mol·L-1 | 反應前溶液 的溫度/℃ | 金屬完全消 失的時間/s |
| 1 | 0.10 | 片狀 | 50 | 0.8 | 20 | 200 |
| 2 | 0.10 | 粉狀 | 50 | 0.8 | 20 | 25 |
| 3 | 0.10 | 片狀 | 50 | 1.0 | 20 | 125 |
| 4 | 0.10 | 片狀 | 50 | 1.0 | 35 | 50 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 C(g)+D(g)正反應速率增大的措施是 ( )
C(g)+D(g)正反應速率增大的措施是 ( )| A.增大C或D的濃度 | B.減小B或A的濃度 |
| C.減小C或D的濃度 | D.充入稀有氣體 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
| 實 驗 步 驟 | 現 象 | 結 論 |
| ①分別取等體積的2 mol/L硫酸于試管中; ②分別投入大小、形狀相同的Cu、Fe、Mg。 | 反應快慢: Mg>Fe>Cu | 反應物的性質越活潑,反應速率越快。 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com