
【題目】下列各組有機物中,無論以何種比例混合,只要二者的物質的量之和不變,完全燃燒時消耗的氧氣及生成的水的物質的量也不變的是
A.C2H2和C6H6
B.C2H6和C2H5OH
C.C2H4和C2H6O
D.C6H6和C7H6O2
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數,下列敘述中正確的是( )
A.標準狀況下,22.4 L H2O含有的分子數為NA
B.常溫常壓下,1.06 g Na2CO3含有的Na+數為0.02NA
C.常溫常壓下,NA個CO2分子占有的體積為22.4 L
D.物質的量濃度為0.5 molL-1的MgCl2溶液中含有Cl﹣個數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】迄今為止,煤不但是人類使用的主要能源,也是重要的化工原料。如圖是以煤為原料合成聚苯乙烯塑料的流程。
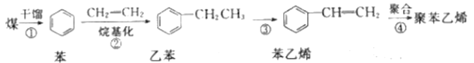
(1)苯在一定條件與Cl2反應可生成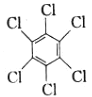 ,該反應類型為___(填“取代”或“加成”)反應;
,該反應類型為___(填“取代”或“加成”)反應;
(2)如圖流程中原子利用率為100%的反應是___(填字母);
A.①③ B.②④
(3)能使酸性高錳酸鉀溶液褪色的是___(填“![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電化學脫硫技術是一種溫和的凈化技術,其基本原理為利用陽極反應產生的羥基自由基(·OH,氧元素為-1價)將燃煤中的含硫物質氧化除去,其裝置示意圖如圖所示。
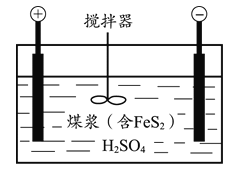
(1)將煤打成煤漿加入電解槽的目的是________。
(2)陽極的電極反應式為________。
(3)補全用羥基自由基除去煤中二硫化亞鐵(FeS2)的反應的離子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +___。
(4)利用上述裝置對某含FeS2的煤樣品進行電解脫硫,測得一定時間內隨溶液起始pH的改變脫硫率(溶于水中的硫元素質量占煤樣中硫元素總質量的百分比)的變化如下圖所示。

pH大于1.5后脫硫率下降的可能原因有:隨著pH的升高,反應物的氧化性或還原性降低;________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某原電池裝置如圖所示,電池總反應為2Ag+Cl2=2AgCl。下列說法正確的是

A. 正極反應為AgCl +e-=Ag +Cl-
B. 放電時,交換膜右側溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替鹽酸,則電池總反應隨之改變
D. 當電路中轉移0.01 mol e-時,交換膜左側溶液中約減少0.02 mol離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應mA(固)+nB(氣)![]() pC(氣)+qD(氣),反應過程中其它條件不變時C的百分含量C%與溫度(T)和壓強(P)的關系如圖所示,下列敘述中正確的是
pC(氣)+qD(氣),反應過程中其它條件不變時C的百分含量C%與溫度(T)和壓強(P)的關系如圖所示,下列敘述中正確的是
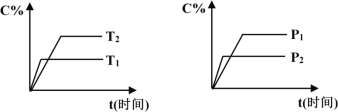
A. 達到平衡后,使用催化劑,C%將增大
B. 達到平衡后,若升高溫度、化學平衡向逆反應方向移動
C. 方程式中n>p+q
D. 達到平衡后,增加A的量有利于化學平衡向正反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對燃煤煙氣和汽車尾氣進行脫硝、脫碳和脫硫等處理,可實現綠色環保、節能減排等目的。汽車尾氣脫硝脫碳的主要原理為:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H=-Q(Q>0)。一定條件下,在一密閉容器中,用傳感器測得該反應在不同時間的NO和CO濃度如下表:
N2(g)+2CO2(g)△H=-Q(Q>0)。一定條件下,在一密閉容器中,用傳感器測得該反應在不同時間的NO和CO濃度如下表:
時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)寫出該反應的平衡常數表達式____________________。
(2)前2s內的平均反應速率υ(N2)=__________;達到平衡時,CO的轉化率為___________。
(3)采用低溫臭氧氧化脫硫脫硝技術,同時吸收SO2和NOx,獲得(NH4)2SO4的稀溶液,往(NH4)2SO4溶液中再加入少量 (NH4)2SO4固體,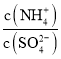 的值將_______(填 “變大”、“不變”或“變小”)。
的值將_______(填 “變大”、“不變”或“變小”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向BaCl2溶液中通入足量SO2氣體,沒有沉淀生成,繼續滴加一定量的氨水后,生成BaSO3沉淀。用電離平衡原理解釋上述現象。_______________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是一種食鹽包裝標簽上的文字。
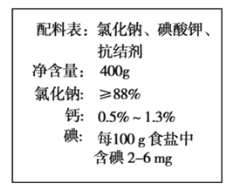
(1)標簽上碘含量中,碘是指__________(填字母序號)。
A.碘元素 B.碘單質 C.碘離子 D.碘酸鹽
(2)完成實驗:配制![]()
![]() 的
的![]() 溶液。
溶液。
①實驗所需的玻璃儀器有燒杯、玻璃棒、量筒、_______、膠頭滴管。
②向容量瓶中加入蒸餾水,直到液面距瓶頸刻度線下![]() 時,改用膠頭滴管滴加蒸餾水至液面的最低點與刻度線______________,蓋好瓶塞,反復上下顛倒,搖勻。
時,改用膠頭滴管滴加蒸餾水至液面的最低點與刻度線______________,蓋好瓶塞,反復上下顛倒,搖勻。
③配制好的溶液__________(填“能”或“不能”)長期存放在容量瓶中。
(3)下列操作中,會導致所配溶液濃度偏低的是___________(填字母序號)。
A.轉移溶液至容量瓶后,未洗滌燒杯和玻璃棒
B.移液時容量瓶中有少量蒸餾水
C.搖勻后發現液面低于容量瓶刻度線,但未補加水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com