
【題目】向用鹽酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀質量與滴入NaOH溶液體積關系如右圖,則原混合溶液中MgCl2與FeCl3的物質的量之比為( ) 
A.![]()
B.![]()
C.![]()
D.![]()
【答案】D
【解析】解:向用鹽酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先發生反應NaOH+HCl=NaCl+H2O,即為圖象中0﹣amL,沉淀的質量為0g;FeCl3只能在酸性較強的溶液中存在,當酸性減弱時,會轉化為Fe(OH)3沉淀,從amL開始,bmL時沉淀完全.bmL時,溶液仍然呈酸性,到cmL時,才開始產生Mg(OH)2沉淀,
令氫氧化鈉濃度為xmol/L,
Fe3+完全沉淀消耗氫氧化鈉為(b﹣a)mL,結合Fe3++3OH﹣═Fe(OH)3↓可知,溶液中n(Fe3+)= ![]() ×(b﹣a)×10﹣3Lxmol/L,
×(b﹣a)×10﹣3Lxmol/L,
Mg2+完全沉淀消耗氫氧化鈉為(d﹣c)mL,結合Mg2++2OH﹣═Mg(OH)2↓可知,溶液中n(Mg2+)= ![]() ×(d﹣c)×10﹣3Lxmol/L,
×(d﹣c)×10﹣3Lxmol/L,
故原混合溶液中n(MgCl2):n(FeCl3)= ![]() ×(d﹣c)×10﹣3Lxmol/L:
×(d﹣c)×10﹣3Lxmol/L: ![]() ×(b﹣a)×10﹣3Lxmol/L=
×(b﹣a)×10﹣3Lxmol/L= ![]() ,
,
故選D.
向用鹽酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先發生反應NaOH+HCl=NaCl+H2O,即為圖象中0﹣amL,沉淀的質量為0g;FeCl3只能在酸性較強的溶液中存在,當酸性減弱時,會轉化為Fe(OH)3沉淀,從amL開始,bmL時沉淀完全.bmL時,溶液仍然呈酸性,到cmL時,才開始產生Mg(OH)2沉淀,結合Fe3++3OH﹣═Fe(OH)3↓、Mg2++2OH﹣═Mg(OH)2↓計算判斷.


 同步輕松練習系列答案
同步輕松練習系列答案 課課通課程標準思維方法與能力訓練系列答案
課課通課程標準思維方法與能力訓練系列答案科目:高中化學 來源: 題型:
【題目】Cu2O主要用于制造船底防污漆,它是一種鮮紅色粉末,幾乎不溶于水,在濕空氣中逐漸氧化成黑色氧化銅。用含NaOH的Na2SO3溶液還原CuSO4制備Cu2O的工藝流程如下:

回答下列問題:
(1)流程中涉及的化學反應主要包括:
Ⅰ.Cu2++2OH-=Cu(OH)2↓;Ⅱ.生成CuOH;Ⅲ.2CuOH=Cu2O+H2O。
寫出第Ⅱ步反應的離子方程式: ______________________________。
(2)其他反應條件相同時,測得反應時間和溶液的pH對Cu2O產率的影響如下圖所示:
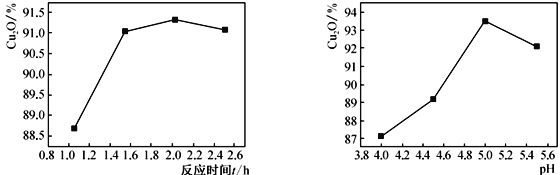
①反應時間超過2h時,Cu2O產率開始降低其原因是____________________________。
②pH<5時,Cu2O產率隨pH減小而減小,產品中銅含量增加明顯,其原因是______________________(用離子方程式說明)。
(3)為測定產品中Cu2O的含量,稱取3.96 g產品于錐形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反應后用0.2000 mol·L-1標準KMnO4溶液滴定,至終點時消耗50mL標準液。
①滴定時應選用______(填“酸式”或“堿式”)滴定管,滴定終點的現象是______________________。
②產品與硫酸酸化的Fe2(SO4)3溶液反應的離子方程式為________________________________。
③假定雜質不參與反應,產品中Cu2O的質量分數為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人工腎臟可采用間接電化學方法除去代謝產物中的尿素[CO(NH2)2],原理如下圖所示。下列說法不正確的是( )

A. B為電源的負極
B. 陽極室中發生的反應依次為:2Cl--2e-=Cl2↑,CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl
C. 電解結束后,陰極室溶液的pH與電解前相比一定會減小
D. 若兩極共收集到氣體13.44 L(標準狀況),則理論可去除尿素為7.2g(忽略氣體的溶解)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在相同條件下,一定量的氫氣在氧氣中充分燃燒并放出熱量。若生成液態水放出的熱量為Q1 kJ;若生成氣態水放出的熱量為Q2 kJ,那么Q1與Q2的大小關系是
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2 D.不能確定
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,充分燃燒一定量的丁烷放出熱量Q kJ(Q>0),經測定完全吸收生成的CO2需消耗5 mol/L的KOH溶液100 mL,恰好生成正鹽,則此條件下反應C4H10(g)+13/2O2(g)===4CO2(g)+5H2O(g)的ΔH為
A. +8Q kJ/mol B. +16Q kJ/mol
C. -8Q kJ/mol D. -16Q kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把6mol銅粉投入含8mol硝酸和2mol硫酸的稀溶液中,則標準狀況下放出的氣體的物質的量為( )
A.2 mol
B.3 mol
C.4 mol
D.5 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在101kPa、25℃時,1.0g乙烷氣體完全燃燒生成液態水時,放出熱量52.0kJ,則乙烷燃燒的熱化學方程式為( )
A.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=﹣1560kJmol﹣1
C.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
D.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJmol﹣1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com