
“天宮一號”使用鎳氫電池供電。鎳氫電池的負極材料為儲氫合金(用—表示,氫以單原子填入合金晶格),總反應為 ,下列說法正確的是
,下列說法正確的是
A. 電池充電時氫原子被氧化
B. 電池放電時正極為NiOOH
C. 電池充電時,與電源負極相連的電極反應為:
D. 電池放電時,負極反應為:
科目:高中化學 來源:2016-2017學年江西省南昌市、洪都中學、麻丘中學、十七中、桑海中學高二3月聯考化學試卷(解析版) 題型:選擇題
某有機物分子的結構簡式如圖所示:下列相關敘述正確的是( ) 
A.該有機化合物含有3種官能團
B.該有機物分子中最多有12個碳原子在同一平面內
C.該有機物分子中最多有6個碳原子共線
D.該有機物分子中最多有14個碳原子在同一平面內
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省安慶市高三第二次模擬考試理科綜合化學試卷(解析版) 題型:簡答題
鎢是熔點最高的金屬,是重要的戰略物資,廣泛用于鋼鐵工業,電真空照明材料等方面。黑鎢礦是一種有開采價值的鎢礦石,其主要成分是鐵和錳的鎢酸鹽(常用FeWO4、MnWO4表示)。它的傳統冶煉工藝的第一階段如下圖所示:

注:①上述流程中鎢的化合價不變 ②鎢酸(H2WO4)是一種難溶性酸
(1)寫出C的化學式:______;寫出生成B的化學方程式:_________
(2)上述流程中,第一次過濾所得濾渣的主要成份除MnO2外,還含有_________,請寫出FeWO4在熔融條件下發生反應生成該成分的化學方程式_________
(3)冶煉金屬鎢是用非整比的鎢氧化物為原料,鎢元素在其中存在兩種價態:+5價和+6價,試確定組成為WO2.7的氧化鎢中兩種對應價態的鎢原子個數的整數比為_____________。
(4)黑鎢礦還含少量Si、As的化合物,上述流程需優化(見下圖)。向含Na2WO4的濾液中加硫酸調節pH=10后,再除雜凈化。
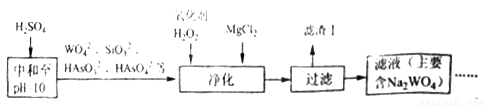
則“凈化”過程中,加入H2O2的目的是__________,濾渣Ⅰ的主要成分是____________。
(5)某溫度下,Ca(OH)2、CaWO4的相關數據見下表
項目 | CaWO4 | Ca(OH)2 |
-lgc(陰離子) | 4 | 2 |
-lgc(Ca2+) | 6 | 4 |
將鎢酸鈉溶液加入石灰乳中,發生反應的離子方程式為WO42-(aq)+Ca(OH)2(s)  CaWO4(s)+2OH-(aq)該溫度下此反應的平衡常數為______mol/L。
CaWO4(s)+2OH-(aq)該溫度下此反應的平衡常數為______mol/L。
查看答案和解析>>
科目:高中化學 來源:2017屆內蒙古赤峰市寧城縣高三一模理科綜合化學試卷(解析版) 題型:選擇題
下列化合物中同分異構體數目最少的是( )
A.戊烷 B.戊醇 C.戊烯 D.乙酸乙酯
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省高三2月模擬理科綜合化學試卷(解析版) 題型:簡答題
硫代硫酸鈉(Na2S2O3)商品名“海波”,俗名“大蘇打”,分析化學上常用于 滴定實驗。某化學興趣小組在實驗室制備硫代硫酸鈉晶體并探究其化學性質。
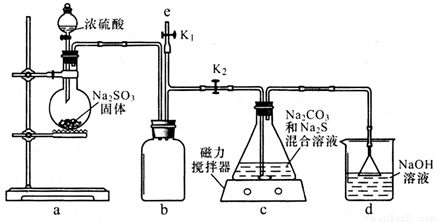
I.制備 Na2S2O3
(1)如圖,關閉K1打開K2, 反應開始后,裝置c中的產物除 了 Na2S2O3外還有一種無色無味 的氣體,這種氣體是______。
(2)裝置c中反應結束后, 先關閉分液漏斗旋塞,在e處連 接盛NaOH溶液的注射器,再關閉K2打開K1 ,其目的是_______________。待c中溶液冷卻后,倒入蒸發皿,通過加熱蒸發、冷卻結晶和干燥等操作獲得Na2S2O3 CH2O晶體。
(3)實驗結束后,裝置d中的溶質可能有__________________。
探究Na2S2O3的部分化學性質
【分析推理】Na2S2O3可以看成是一個S原子取代了 Na2SO4中一個O原子形成的。據此 推測,下列說法正確的是____________。
A.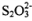 和
和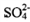 都是正四面體結構 B.
都是正四面體結構 B.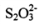 中硫硫鍵的鍵長大于硫氧鍵
中硫硫鍵的鍵長大于硫氧鍵
C.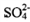 中的鍵角均為
中的鍵角均為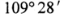 D.
D.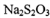 中所有原子都滿足8電子結構
中所有原子都滿足8電子結構
【提出假設】①Na2S2O3與Na2SO4結構相似,化學性質也應該相似,因此室溫時Na2S2O3 溶液pH=7。②從S元素的化合價推測Na2S2O3具有較強的還原性。
【驗證假設】配制適量Na2S2O3溶液,進行如下實驗(請填空):
實驗操作 | 實驗現象 | 現象解釋(用離子方程式表示) | |
① | ___________________ | 溶液pH=8 | ___________ |
② | 向新制氯水中滴入適量Na2S2O3溶液 | 氯水褪色 | _____________ |
【實驗結論】__________________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省高二2月聯考化學試卷(解析版) 題型:簡答題
按要求填寫下列問題:
(1)某些共價化合物(如H2O、NH3、N2O4等)在液態時會發生微弱的電離,如:2H2O  H3O+ + OH—,則液態NH3電離的方程式是_______________________
H3O+ + OH—,則液態NH3電離的方程式是_______________________
(2)某溫度(t℃)時,測得0.01mol/L的NaOH溶液的pH=11,則該溫度下水的KW=_______,在此溫度下,將pH=a的H2SO4溶液Va L與pH=b的NaOH溶液Vb L混合,若所得混合液為中性,且a+b=12,則Va:Vb=_________
(3)一定條件下,CO可與粉末狀的氫氧化鈉作用生成甲酸鈉。
①常溫時,甲酸的電離平衡常數Ka=1.70×10-4。甲酸鈉的水溶液呈堿性,請用離子反應方程式表示其原因 ____________,0.1mol/L的甲酸鈉溶液pH約為_______(已知:lg17 ≈1.23, 計算結果保留一位小數)
②向20ml 0.1mol/L的甲酸鈉溶液中小心滴加10ml 0.1mol/L的鹽酸,混合液呈酸性,請按由大到小的順序給溶液中離子濃度排序_______________
(4)室溫時,M(OH)2(s) M2+(aq) + 2OH-(aq),Ksp=a;c(M2+)=b mol·L?1時,溶液的pH等于_________
M2+(aq) + 2OH-(aq),Ksp=a;c(M2+)=b mol·L?1時,溶液的pH等于_________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省高二2月聯考化學試卷(解析版) 題型:選擇題
為了除去MgCl2酸性溶液中的Fe3+,可在加熱、攪拌的條件下加入一種試劑,過濾后再加入適量鹽酸,這種試劑是( )
A.NH3H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省棗莊市南校區高一3月月考化學試卷(解析版) 題型:選擇題
鐳是元素周期表中第七周期的ⅡA族元素。下面關于鐳的性質的描述中不正確的是
A. 在化合物中呈+2價 B. 單質與水反應放出氫氣
C. 氫氧化物呈兩性 D. 鐳的還原性大于鎂
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下列敘述不正確的是
A.H2S、H2O、HF的穩定性依次增強
B.RbOH、KOH、Mg(OH)2的堿性依次減弱
C.Na+、Mg2+、Al3+的氧化性依次減弱
D.H4SiO4、H2CO3、H2SO4酸性依次增強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com