
【題目】錳的單質(zhì)及其化合物的用途非常廣泛![]() 回答下列問題:
回答下列問題:
⑴基態(tài)錳原子的外圍電子排布式為______________________,其d軌道中未成對電子數(shù)為__________。
⑵MnO的熔點(1650℃)比MnS的熔點(1610℃)高原因是_____________________________________。
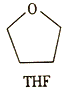
⑶錳的一種配合物的化學(xué)式為Mn(BH4)2(THF)3,THF的結(jié)構(gòu)簡式如圖所示。
①THF中的元素的電負性從大到小的順序是__________________。
②與Mn2+形成配位鍵的原子為______(填元素符號)。
③BH4-的空間構(gòu)型為_______,其中B原子的雜化軌道類型為________。
④寫出兩種與BH4-互為等電子體的分子或離子___________。
⑷一種磁性材料的單晶胞結(jié)構(gòu)如圖所示。
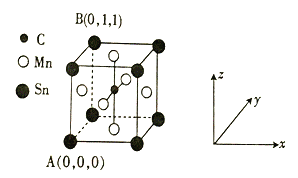
①該晶胞中碳原子的原子坐標(biāo)為________。
②Mn在晶體中的堆積方式為_______(填“簡單立方”“體心立方”或“面心立方最密”)堆積。
③若該晶胞的邊長為a pm,NA表示阿伏加德羅常數(shù)的數(shù)值,則該晶體密度的表達式為ρ = ___________________ gcm-3。
【答案】3d54s2 5 同為離子晶體,MnO和MnS的電荷數(shù)一樣,r(O2-) < r (S2-),MnO的晶格能大,熔點更高 O > C > H O 正四面體 sp3 CH4、SiH4(或NH4+等其他合理答案) (![]() ,
,![]() ,
,![]() ) 面心立方最密
) 面心立方最密 ![]()
【解析】
⑴基態(tài)錳原子的外圍電子排布式為:3d54s2。
⑵MnO、MnS同為離子晶體,MnO和MnS的電荷數(shù)一樣,r(O2-) < r (S2-),MnO的晶格能大。
⑶①非金屬性越強,電負性越大;②與Mn2+形成配位鍵的原子為O原子;③BH4-計算價層電子對數(shù)。
④價電子數(shù)B-=C=Si=N+,寫出等電子體。
⑷①根據(jù)晶胞可知,碳原子都位于![]() 處,故其原子坐標(biāo)為:(
處,故其原子坐標(biāo)為:(![]() ,
,![]() ,
,![]() );②Mn在晶體中的堆積方式為面心立方最密;③若該晶胞的邊長為a pm,NA表示阿伏加德羅常數(shù)的數(shù)值,晶體密度的表達式。
);②Mn在晶體中的堆積方式為面心立方最密;③若該晶胞的邊長為a pm,NA表示阿伏加德羅常數(shù)的數(shù)值,晶體密度的表達式。
⑴基態(tài)錳原子的外圍電子排布式為:3d54s2;其d軌道中未成對電子數(shù)為5,故答案為:3d54s2;5。
⑵MnO的熔點(1650℃)比MnS的熔點(1610℃)高原因是:同為離子晶體,MnO和MnS的電荷數(shù)一樣,r(O2-) < r (S2-),MnO的晶格能大,熔點更高;故答案為:同為離子晶體,MnO和MnS的電荷數(shù)一樣,r(O2-) < r (S2-),MnO的晶格能大,熔點更高。
⑶①非金屬性越強,電負性越大,故電負性大小為:O > C > H;故答案為:O > C > H。
②與Mn2+形成配位鍵的原子為O原子,故答案為:O。
③BH4-價層電子對數(shù)4對,空間構(gòu)型為正四面體,其中B原子的雜化軌道類型為sp3;故答案為:正四面體;sp3。
④價電子數(shù)B-=C=Si=N+,因此與BH4-互為等電子體的分子或離子CH4、SiH4(或NH4+等其他合理答案);故答案為:CH4、SiH4(或NH4+等其他合理答案)。
⑷①根據(jù)晶胞可知,碳原子都位于![]() 處,故其原子坐標(biāo)為:(
處,故其原子坐標(biāo)為:(![]() ,
,![]() ,
,![]() );故答案為:(
);故答案為:(![]() ,
,![]() ,
,![]() )。
)。
②Mn在晶體中的堆積方式為面心立方最密,故答案為:面心立方最密。
③若該晶胞的邊長為a pm,NA表示阿伏加德羅常數(shù)的數(shù)值,晶胞質(zhì)量為:![]() 則該晶體密度的表達式為
則該晶體密度的表達式為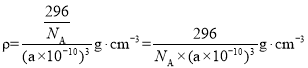 ;故答案為:
;故答案為:![]() 。
。


科目:高中化學(xué) 來源: 題型:
【題目】亞氯酸鈉是一種高效氧化劑漂白劑,主要用于棉紡、亞麻、紙漿等漂白。亞氯酸鈉![]() 在溶液中可生成
在溶液中可生成![]() 、
、![]() 、
、![]() 、
、![]() 等,其中
等,其中![]() 和
和![]() 都具有漂白作用,但
都具有漂白作用,但![]() 是有毒氣體;經(jīng)測定,
是有毒氣體;經(jīng)測定,![]() 時各組分含量隨pH變化情況如圖所示
時各組分含量隨pH變化情況如圖所示![]() 沒有畫出
沒有畫出![]() 則下列分析正確的是( )
則下列分析正確的是( )
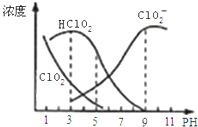
A.亞氯酸鈉在酸性條件下較穩(wěn)定
B.![]() 時,
時,![]() 的電離平衡常數(shù)的數(shù)值
的電離平衡常數(shù)的數(shù)值![]()
C.pH越大,該漂白劑的漂白性能越好
D.![]() ,
,![]() 時,
時,![]() 溶液中:
溶液中:![]()
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下表是![]() 時某些鹽的溶度積常數(shù)和弱酸的電離平衡常數(shù),下列說法正確的是( )
時某些鹽的溶度積常數(shù)和弱酸的電離平衡常數(shù),下列說法正確的是( )
化學(xué)式 | AgCl |
|
| HClO |
|
|
|
|
|
|
|
A.相同濃度![]() 和
和![]() 的混合液中,各離子濃度的大小關(guān)系是
的混合液中,各離子濃度的大小關(guān)系是![]()
B.碳酸鈉溶液中滴加少量氯水的離子方程式為![]()
C.向![]() HClO溶液中滴加NaOH溶液至
HClO溶液中滴加NaOH溶液至![]() :
:![]() 1:3,此時溶液
1:3,此時溶液![]()
D.向濃度均為![]() 的KCl和
的KCl和![]() 混合液中滴加
混合液中滴加![]() 的
的![]() 溶液,
溶液,![]() 先形成沉淀
先形成沉淀
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】碳及其化合物有許多用途。回答下列問題:
⑴碳元素有12C、13C和14C等核素。下列對12C基態(tài)原子結(jié)構(gòu)的表示方法中,對電子運動狀態(tài)描述最詳盡的是_______(填標(biāo)號)。
A. B.
B.![]()
C.1s22s22p2 D.
基態(tài)13C原子核外有________種不同空間運動狀態(tài)的電子。
⑵K3[Fe(CN)6]晶體中Fe3+與CN-之間的化學(xué)鍵的類型為________,該化學(xué)鍵能夠形成的原因是________。
⑶有機物 是________(填“極性”或“非極性”)分子;該有機物中存在sp3雜化的原子,其對應(yīng)元素的第一電離能由大到小的順序為________。
是________(填“極性”或“非極性”)分子;該有機物中存在sp3雜化的原子,其對應(yīng)元素的第一電離能由大到小的順序為________。
⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均屬于胺,兩者相對分子質(zhì)量接近,但乙二胺比三甲胺的沸點高得多,原因是________。
⑸碳酸鹽中的陽離子不同,熱分解溫度就不同。下表為四種碳酸鹽的熱分解溫度和金屬陽離子半徑:
碳酸鹽 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
熱分解溫度/℃ | 402 | 900 | 1172 | 1360 |
金屬陽離子半徑/pm | 66 | 99 | 112 | 135 |
隨著金屬陽離子半徑的增大,碳酸鹽的熱分解溫度逐步升高,原因是________。
⑹石墨的晶體結(jié)構(gòu)和晶胞結(jié)構(gòu)如圖所示。已知石墨的密度為ρgcm-3,C—C鍵長為γ cm,阿伏加德羅常數(shù)的值為NA,則石墨晶體的層間距為________cm。

查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列表述中正確的是 ( )
A.任何能使熵值增大的過程都能自發(fā)進行
B.已知熱化學(xué)方程式2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-Q kJ·mol-1(Q>0),則將2 mol SO2(g)和1 mol O2(g)置于一密閉容器中充分反應(yīng)后放出Q kJ的熱量
2SO3(g)ΔH=-Q kJ·mol-1(Q>0),則將2 mol SO2(g)和1 mol O2(g)置于一密閉容器中充分反應(yīng)后放出Q kJ的熱量
C.化學(xué)平衡發(fā)生移動,平衡常數(shù)一定發(fā)生變化
D.1 mol NaOH分別和1 mol CH3COOH、1 mol HNO3反應(yīng),后者比前者放出的熱量多
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列實驗方案不能達到實驗?zāi)康牡氖?/span>

A. 圖A裝置Cu和濃硝酸制取NO B. 圖B裝置實驗室制備Cl2
C. 圖C裝置實驗室制取乙酸乙酯 D. 圖D裝置實驗室分離CO和CO2
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】鋁、鈦、鋇(第2主族)等元素在能源、材料等領(lǐng)域應(yīng)用廣泛。回答下列問題:
⑴與鈦同周期的所有副族元素的基態(tài)原子中,最外層電子數(shù)與基態(tài)鈦原子相同的元素有________種。基態(tài)Ti2+的最外層電子排布式為________________。
⑵鋁的逐級電離能數(shù)據(jù)為:I1=580 kJmol-1、I2=1820 kJmol-1、I3=2750 kJmol-1、I4=11600 kJmol-1。請分析數(shù)據(jù)規(guī)律,預(yù)測鋇的逐級電離能的第一個數(shù)據(jù)“突躍”點出現(xiàn)在________之間(用I1、I2、I3等填空![]() 。
。
⑶已知第ⅡA族元素的碳酸鹽MCO3熱分解的主要過程是:M2+結(jié)合碳酸根離子中的氧離子。則CaCO3、BaCO3的分解溫度較高的是________________(填化學(xué)式),理由是________________。
⑷催化劑M能催化乙烯、丙烯、苯乙烯等的聚合,其結(jié)構(gòu)如圖1所示。
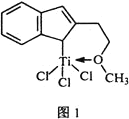
①M中,碳原子的雜化類型有________________。
②M中,不含________![]() 填標(biāo)號
填標(biāo)號![]() 。
。
A. π鍵 B. δ鍵 C. 配位鍵 D.氫鍵 E. 離子鍵
⑸氫化鋁鈉(NaAlH4)是一種新型輕質(zhì)儲氫材料,其晶胞結(jié)構(gòu)如圖2所示,為長方體。寫出與AlH4-空間構(gòu)型相同的一種分子_______________(填化學(xué)式)。NaAlH4晶體中,與AlH4-緊鄰且等距的Na+有________個;NaAlH4晶體的密度為________ gcm-3(用含a、NA的代數(shù)式表示)。
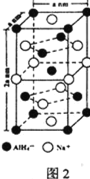
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】實驗室常用乙醇和濃硫酸共熱制取乙烯:![]()
![]()
![]() 。某同學(xué)用如圖裝置進行乙烯制取實驗。下列敘述不正確的是( )
。某同學(xué)用如圖裝置進行乙烯制取實驗。下列敘述不正確的是( )
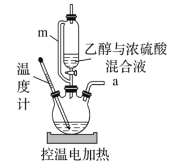
A.m的作用是確保乙醇與濃硫酸能順利流下
B.電控溫值可設(shè)置在165~175℃
C.反應(yīng)混合液的加入順序依次為乙醇、濃硫酸
D.加熱時若發(fā)現(xiàn)三頸瓶中未加碎瓷片,應(yīng)立即補加
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】阿司匹林(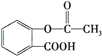 )是常用的解熱鎮(zhèn)痛藥,下列說法不正確的是( )
)是常用的解熱鎮(zhèn)痛藥,下列說法不正確的是( )
A.1mol阿司匹林可以與3molNaOH反應(yīng)
B.阿司匹林與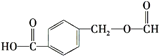 互為同分異構(gòu)體
互為同分異構(gòu)體
C.阿司匹林可以發(fā)生取代反應(yīng)、加成反應(yīng)、酯化反應(yīng)
D.1mol阿司匹林可以與5molH2發(fā)生加成反應(yīng),也可與1mol碳酸氫鈉反應(yīng)
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com