
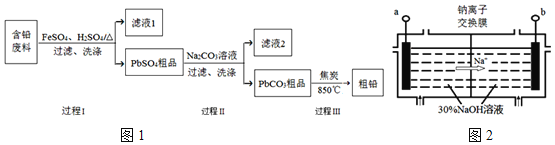
【題目】以廢舊鉛酸電池中的含鉛廢料(Pb、PbO、PbO2、PbSO4及炭黑等)為原料,制備粗鉛,實現鉛的再生利用.其工作流程如圖1所示:
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)過程Ⅰ中,在Fe2+催化下,Pb和PbO2反應生成PbSO4的化學方程式是______.
(2)過程Ⅰ中,Fe2+催化過程可表示為:
![]()
![]() .
.
![]() 寫出ii的離子方程式:______.
寫出ii的離子方程式:______.
![]() 下列實驗方案可證實上述催化過程.將實驗方案補充完整.
下列實驗方案可證實上述催化過程.將實驗方案補充完整.
![]() 向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量PbO2,溶液變紅.
向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量PbO2,溶液變紅.
![]() ______.
______.
(3)過程Ⅱ的目的是脫硫.若濾液2中c(SO42-)=1.6molL-1,c(CO32-)=0.1molL-1,則PbCO3中______![]() 填“是”或“否”
填“是”或“否”![]() 混有PbSO4.
混有PbSO4.
(4)鈉離子交換膜固相電解法是從含鉛廢料中提取鉛的一種新工藝,其裝置如圖2所示.將含鉛廢料投入陰極室,含鉛廢料中的PbSO4與NaOH溶液發生反應:![]()
![]() 與外接電源的______極相連.
與外接電源的______極相連.
![]() 電解過程中,PbO2、PbO、HPbO2-在陰極放電,其中PbO2放電的電極反應式為______.
電解過程中,PbO2、PbO、HPbO2-在陰極放電,其中PbO2放電的電極反應式為______.
![]() 與傳統無膜固相電解法相比,使用鈉離子交換膜可以提高Pb元素的利用率,原因是______.
與傳統無膜固相電解法相比,使用鈉離子交換膜可以提高Pb元素的利用率,原因是______.
【答案】![]() 4
4![]()
![]()
![]() 取a中紅色溶液少量,加入足量Pb,充分反應后,紅色褪去 否 負
取a中紅色溶液少量,加入足量Pb,充分反應后,紅色褪去 否 負 ![]() 阻止HPbO2-進入陽極室被氧化
阻止HPbO2-進入陽極室被氧化
【解析】
(1)在催化下,Pb、PbO2和H2SO4反應生成PbSO4和水,據此書寫反應方程式;
(2)①根據題給信息知反應i中Fe2+被PbO2氧化為Fe3+,則反應ii中Fe3+被Pb還原為Fe2+,據此書寫離子方程式;
②加入過量的Pb平衡逆向進行充分反應后,紅色褪去;
(3)根據Ksp(PbCO3)=3.3×10-14和c(CO32-)=0.1molL-1計算出c(Pb2+)利用濃度積Qc和Ksp(PbSO4)之間的大小關系確定PbCO3中是否混有PbSO4;
(4)①根據鈉離子的移動方向確定陰陽極;
②電解過程中,PbO2在陰極得電子,發生還原反應;
③鈉離子交換膜只允許鈉離子通過。
(1)根據題給化學工藝流程知,過程Ⅰ中,在催化下,Pb、PbO2和H2SO4反應生成PbSO4和水,化學方程式為:![]()
![]()
![]() ;
;
(2)①催化劑通過參加反應,改變反應歷程,降低反應的活化能,加快化學反應速率,而本身的質量和化學性質反應前后保持不變,根據題給信息知反應i中Fe2+被PbO2氧化為Fe3+,則反應ii中Fe3+被Pb還原為Fe2+,離子方程式為:![]() ;
;
②a實驗證明發生反應i,則b實驗需證明發生反應ii,實驗方案為:
![]() 向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量PbO2,溶液變紅,亞鐵離子被氧化為鐵離子,
向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量PbO2,溶液變紅,亞鐵離子被氧化為鐵離子,
![]() 取a中紅色溶液少量,溶液中存在平衡,
取a中紅色溶液少量,溶液中存在平衡,![]() ,加入過量Pb,和平衡狀態下鐵離子反應生成亞鐵離子,平衡逆向進行充分反應后,紅色褪去,
,加入過量Pb,和平衡狀態下鐵離子反應生成亞鐵離子,平衡逆向進行充分反應后,紅色褪去,
(3)因為Ksp(PbCO3)=3.3×10-14和c(CO32-)=0.1molL-1,可知c(Pb2+)=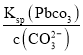 =
=![]() mol/L=3.3×10-13 mol/L , 因此Qc= c(Pb2+) c(SO42-)=3.3×10-13×1.6=5.28×10-13< Ksp(PbSO4),說明PbSO4在母液中未飽和,即PbCO3中不混有PbSO4;
mol/L=3.3×10-13 mol/L , 因此Qc= c(Pb2+) c(SO42-)=3.3×10-13×1.6=5.28×10-13< Ksp(PbSO4),說明PbSO4在母液中未飽和,即PbCO3中不混有PbSO4;
(4)①根據鈉離子向陰極移動知,b為陰極,與電源負極相連;
②電解過程中,PbO2在陰極得電子,發生還原反應,電極反應式為![]() ;
;
③鈉離子交換膜只允許鈉離子通過,阻止HPbO2-進入陽極室被氧化,從而提高Pb元素的利用率;


科目:高中化學 來源: 題型:
【題目】元素周期表中七個周期可填充的元素種類如下表所示:
周期數 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
元素種類 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期均比第4、5周期多了14種元素,其原因是__。
(2)周期表中__族所含元素最多。
(3)請分析周期數與元素種類的關系,可推測出第8周期可能含有的元素種類為__(填序號)。
A.18 B.32 C.50 D.64
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸在生活和生產中應用廣泛。
Ⅰ 某工廠以黃鐵礦(主要成分為FeS2)為原料,采用“接觸法”制備硫酸。
已知298 K和101 kPa條件下:
2FeS2(s)=2FeS(s)+S(s) ΔH1
S(s)+2O2(g)=2SO2(g) ΔH2
4FeS(s)+7O2(g)=2Fe2O3(s)+4SO2(g) ΔH3
則在該條件下FeS2與O2生成Fe2O3和SO2的總熱化學方程式是________。
Ⅱ 催化氧化反應:2SO2(g)+O2(g)2SO3(g) ΔH<0
(1) 在體積可變的密閉容器,維持壓強為1×105 Pa和初始n(SO2)=2 mol,充入一定量的O2,SO2平衡轉化率α(SO2)隨O2物質的量n(O2)的變化關系如圖所示:
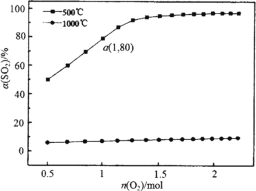
①在1000℃時,SO2平衡轉化率隨著O2物質的量的增大緩慢升高,解釋其原因________。
②a點時SO3的平衡分壓p(SO3)=________Pa(保留2位有效數字,某組分的平衡分壓=總壓×某組分的物質的量分數)。
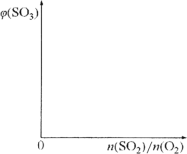
(2)保持溫度不變,向固定體積的密閉容器中充入一定量的SO2、O2。請畫出平衡體系中SO3的體積分數φ(SO3)隨初始SO2、O2的物質的量之比[n(SO2)/n(O2)]的變化趨勢圖。
(3)已知活化氧可以把SO2快速氧化為SO3。根據計算機模擬結果,在炭黑表面上O2轉化為活化氧的反應歷程與能量變化如圖所示。下列說法正確的是________。
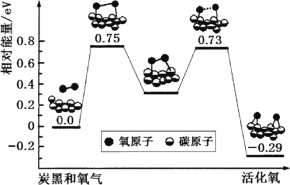
A O2轉化為活化氧是氧氧鍵的斷裂與碳氧鍵的生成過程
B 該過程中最大能壘(活化能)E正=0.73 eV
C 每活化一個O2吸收0.29 eV的能量
D 炭黑可作為SO2轉化為SO3的催化劑
E 其它條件相同時,炭黑顆粒越小,反應速率越快
Ⅲ 硫酸工廠尾氣中的SO2可被NaOH溶液吸收,用惰性電極將所得的Na2SO3溶液進行電解,可循環再生NaOH的同時得到H2SO4,寫出陽極的電極方程式________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物H是有機合成重要的中間體,其合成路線如圖:
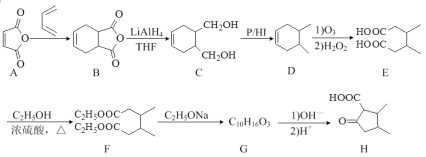
(1)H中官能團的名稱為_________。
(2)B→C的反應類型為________。
(3)![]() 的名稱為 _______。
的名稱為 _______。
(4)化合物G的結構簡式為 _______。
(5)B的一種同分異構體同時滿足下列條件,寫出該同分異構體的結構簡式:________。
①能與FeCl3溶液發生顯色反應;
②堿性水解后酸化,所得兩種產物分子均只有2種不同化學環境的氫原子。
(6)以乙烯和![]() 為原料,制備
為原料,制備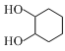 的合成路線流程圖(無機試劑和有機溶劑任用,合成路線流程圖示例見本題題干)____________________。
的合成路線流程圖(無機試劑和有機溶劑任用,合成路線流程圖示例見本題題干)____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知五種元素為短周期元素,其原子序數的大小順序為C>A>B>D>E;A、C同周期,B、C同主族;A與B形成離子化合物,A2B中所有離子的電子數相同,其電子總數為30;D和E可形成4核10個電子分子。試回答下列問題:
(1)寫出五種元素名稱A________,B________,C________,D________,E________;
(2)用電子式表示A2C的形成過程________________________________;
(3)D與E形成常見離子的空間構型為________________;
(4)A、B兩元素形成的化合物A2B2屬于__________晶體(填類型),晶體內存在的化學鍵有___________;A2B晶體的熔點_______(填“>”“=”“<”)A2C晶體的熔點;
(5)由A、B、C、E四種元素,可以共同形成兩種不同化合物,它們的水溶液可以反應生成一種氣體,請寫出離子方程式:___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2020年5月1日起,新版《北京市生活垃圾管理條例》正式實施,下列垃圾分類對應不正確的是
|
|
|
|
A. 雞蛋殼、剩飯菜 | B. 市民使用后一次性口罩 | C. 過期藥品 | D. 一 次性干電池 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組進行有關電解食鹽水的探究實驗,電解裝置如圖所示。
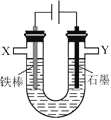
實驗一:電解飽和食鹽水。
(1)配制飽和食鹽水所需的玻璃儀器有:燒杯、量筒、_________________。
(2)電解飽和食鹽水的化學方程式為________________。
實驗二:電解不飽和食鹽水及產物分析。
相同條件下,電解1mol·L-1 NaCl溶液并收集兩極產生的氣體。在X處收集到V1mL氣體,同時,在Y處收集到V2mL氣體,停止電解。結果發現V2<V1,且與電解飽和食鹽水相比,Y處收集到的氣體顏色明顯較淺。經討論分析,導致上述現象的原因有:
ⅰ.有部分Cl2溶于NaCl溶液中;ⅱ.有O2生成。
(3)設計實驗證明有部分Cl2溶于NaCl溶液中。實驗方案為:取少量__________電極附近溶液。
(4)證明有O2生成并測定O2的體積。按如右圖所示裝置進行實驗,通過注射器緩緩地將在Y處收集到V2mL氣體全部推入裝置A(盛有足量試劑NaOH溶液)中,最終,量氣管中收集到V3mL氣體(設V1、V2、V3均在相同條件下測得)。
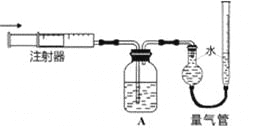
①裝置A的作用是_______________。
②本實驗中,觀察到________________的現象,說明石墨電極上有O2生成。
③實驗中是否需要預先除盡裝置中的空氣?____________(填“是”或“否”)。
(5)實驗二中,在石墨電極上產生的Cl2的總體積為________mL(用代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素R、T、Q、W、G在元素周期表中的相對位置如下表所示,其中Q是無機非金屬材料的主角。下列判斷正確的是( )
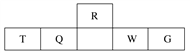
A. 離子半徑:T<W<G
B. 等物質的量的W、G單質分別與足量鐵粉反應,后者消耗的鐵粉多
C. 最簡單氣態氫化物的熱穩定性:Q<R
D. T和G組成的化合物溶于水,其水溶液呈中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關![]() 反應的敘述正確的為
反應的敘述正確的為
A.還原劑與氧化劑物質的量之比為5:3
B.生成lmolO2,反應共轉移4mol電子
C.若有5mol水做還原劑時,被BrF3還原的BrF3為![]() mol
mol
D.若有5mol水參與反應時,被水還原的BrF3為2mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com