
【題目】常溫下,將20.0g質量分數為14%的KNO3溶液與30.0g質量分數為24%的KNO3溶液混合,得到密度為1.15g/cm3的混合溶液。計算:
(1)混合后溶液中KNO3的質量分數為____,物質的量濃度為_____。
(2)在1000g水中需溶解____molKNO3才能使其濃度恰好與上述混合溶液的濃度相等。
(3)標準狀況下44.8LHCl溶于水配成500mL溶液。則其濃度為_____,100mL該溶液與足量NaHCO3反應,生成氣體在標準狀況下為_____L。
【答案】20%; 2.28mol/L; 2.48mol; 4mol/L; 8.96L。
【解析】
(1)根據溶質的質量分數的計算公式![]() ,以及溶液的稀釋定律(稀釋前后溶質的質量、物質的量不變)計算混合后溶質的質量,且混合后溶液質量不變,據此計算混合后溶液中KNO3的質量分數;已知溶液的密度、溶質的質量分數,利用公式
,以及溶液的稀釋定律(稀釋前后溶質的質量、物質的量不變)計算混合后溶質的質量,且混合后溶液質量不變,據此計算混合后溶液中KNO3的質量分數;已知溶液的密度、溶質的質量分數,利用公式![]() 計算溶質的物質的量濃度;
計算溶質的物質的量濃度;
(2)設需要硝酸鉀物質的量為xmol,根據m=nM計算出硝酸鉀的質量,根據(1)中溶液中溶質的質量分數及![]() 進行計算;
進行計算;
(3)根據n=V/Vm計算HCl的物質的量,再根據c=n/V計算其物質的量濃度;根據n=cV計算100mL該溶液中HCl的物質的量,再根據反應方程式:HCO3- + H+ = H2O + CO2↑,計算與足量NaHCO3反應生成CO2氣體在標準狀況下的體積。
(1)混合后溶液的質量為m(溶液)=20.0g+30.0g=50.0g,溶質硝酸鉀的質量:m(溶質)= 20.0g×14%+30.0g×24%=10.0g,則混合后溶質的質量分數為:![]() ,溶質的物質的量濃度為:
,溶質的物質的量濃度為:
![]()
故答案為:20%;2.28mol/L;
(2)設需要硝酸鉀物質的量為xmol,則硝酸鉀的質量為101xg,則溶液的質量為(1000+101x)g,該溶液濃度恰好與上述混合溶液的濃度相等,則該溶液的質量分數也為20%,![]() ,解得:x≈2.48mol;
,解得:x≈2.48mol;
故答案為:2.48mol;
(3)標準狀況下44.8LHCl的物質的量為![]() ,則其濃度為
,則其濃度為![]() ,100mL該溶液中氫離子物質的量n(H+)=cV=4mol/L×0.1L=0.4mol,與足量NaHCO3反應的方程式為:HCO3- + H+ = H2O + CO2↑,則生成0.4mol CO2,V(CO2)=nVm=0.4mol×22.4L/mol=8.96L;
,100mL該溶液中氫離子物質的量n(H+)=cV=4mol/L×0.1L=0.4mol,與足量NaHCO3反應的方程式為:HCO3- + H+ = H2O + CO2↑,則生成0.4mol CO2,V(CO2)=nVm=0.4mol×22.4L/mol=8.96L;
故答案為:4mol/L;8.96L。


 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,表中序號分別代表某一元素。請回答下列問題.
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)可作半導體材料的元素是 ______(填元素符號);氣態氫化物與其最高價氧化物的水化物可直接化合生成一種鹽的元素是 _____(填名稱);
(2)第三周期中離子半徑最小的是___________(填離子符號);
(3)① ~ ⑨的最高價氧化物的水化物中:酸性最強的是 __________(填化學式);堿性最強的是________(填化學式),它與⑥的最高價氧化物的水化物反應的離子方程式為__________。
(4)⑧、⑨可形成A2B2型的化合物,分子中二者均滿足8電子穩定結構,則其電子式為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下將1 mol N2和3 mol H2置于密閉容器中發生反應N2+3H2![]() 2NH3(正反應是放熱反應)。下列關于該反應的說法正確的是
2NH3(正反應是放熱反應)。下列關于該反應的說法正確的是
A. 降低溫度可以加快反應速率
B. 達到化學反應限度時,生成2mol NH3
C. 向容器中再加入N2可以加快反應速率
D. 1mol N2 和3mol H2的總能量低于2mol NH3的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種三室微生物燃料電池污水凈化系統原理如圖所示,圖中含酚廢水中有機物可用C6H5OH表示,左、中、右室間分別以離子交換膜分隔。下列說法錯誤的是
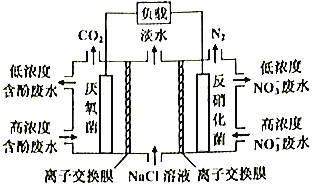
A. 左室電極為該電池的負極
B. 右室電極反應式可表示為:2NO3-+10e-+12H+=N2↑+6H2O
C. 左室電極附近溶液的pH增大
D. 工作時中間室的Cl-移向左室,Na+移向右室
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將AgCl分別加入盛有:①5 mL水;② 6 mL0.5mol·L-1 NaCl溶液;③10 mL0.2mol·L-1 CaCl2溶液;④50 mL0.1mol·L-1鹽酸的燒杯中,均有固體剩余,各溶液中c(Ag+)從大到小的順序排列正確的是
A. ④③②① B. ②③④① C. ①④③② D. ①③②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,電子轉移發生在不同物質的同種元素之間的是
A. 2H2S+SO2=3S↓+2H2OB. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C. 2KClO3![]() 2KCl+3O2↑D. CuO+H2SO4=CuSO4+H2O
2KCl+3O2↑D. CuO+H2SO4=CuSO4+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于如圖裝置說法正確的是

A. 裝置中電子移動的途徑是:負極→Fe→M溶液→石墨→正極
B. 若M為NaCl溶液,通電一段時間后,溶液中可能有NaClO
C. 若M為FeCl2溶液,可以實現石墨上鍍鐵
D. 若M是海水,該裝置是通過“犧牲陽極的陰極保護法”使鐵不被腐蝕
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com