
已知草酸是一種二元弱酸,草酸氫鈉(NaHC2O4)溶液顯酸性。
(1)用離子方程式解釋NaHC2O4溶液顯酸性的原因:________________。
(2)常溫下,向10mL 0.01mol/L NaHC2O4溶液中滴加10mL 0.01mol/L NaOH溶液時,比較所得溶液中各種離子濃度的大小關系:________________。
(3)配平以下氧化還原反應方程式。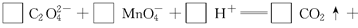
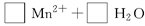
(4)稱取6.0g含H2C2O4·2H2O、KHC2O4和K2SO4的試樣,加水溶解,配成250mL溶液。量取兩份該溶液各25mL,分別置于兩個錐形瓶中。
①第一份溶液中加入2滴酚酞試液,滴加20 mL 0.25 mol/L NaOH溶液時,溶液由無色變為淺紅色。該溶液中被中和的H+的物質的量為________mol。
②第二份溶液中滴加16mL 0.10mol/L酸性KMnO4溶液時反應完全,該溶液中還原劑的物質的量為________mol。
③原試樣中H2C2O4·2H2O的物質的量為________mol,KHC2O4的質量分數為________。
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:填空題
(8分)無論是從在國民經濟中的地位來看,還是從科學發展的角度來看,硅都發揮著重要的作用。
(1)人類使用硅酸鹽產品(陶瓷等)的歷史已經快一萬年了,但在1823年才獲得單質硅,瑞典化學家貝采尼烏斯用金屬鉀還原SiF4獲得單質硅,寫出化學方程式_______________ 。
(2)由于制取方法和條件的不同,得到的單質硅形態不同,其性質也不同。
①用鋁熱法還原氟硅酸鉀制得較純凈的晶體硅:4Al+3K2SiF6高溫3Si+2KAlF4+2K2AlF5,關于該反應的說法正確的是________(填序號)。
| A.Al是還原劑 | B.氧化產物只有KAlF4 |
| C.每轉移6NA電子,得到42 g Si | D.Al元素在KAlF4和K2AlF5中化合價不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
向FeI2溶液中不斷通入Cl2,溶液中I-、I2、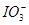 、Fe2+、Fe3+等粒子的物質的量隨n(Cl2)∶n(FeI2)變化的曲線如圖所示。
、Fe2+、Fe3+等粒子的物質的量隨n(Cl2)∶n(FeI2)變化的曲線如圖所示。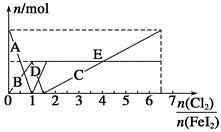
已知:2Fe3++2I-=I2+2Fe2+。
請回答下列問題:
(1)指出圖中折線E和線段C所表示的意義:折線E表示 ;線段C表示 。
(2)寫出線段D所表示的反應的離子方程式: 。
(3)當n(Cl2)∶n(FeI2)=6.5時,溶液中n(Cl-)∶n(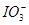 )= 。
)= 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
催化劑是化工技術的核心,絕大多數的化工生產均需采用催化工藝。
⑴人們常用催化劑來選擇反應進行的方向。如圖所示為一定條件下1mol CH3OH與O2發生反應時,生成CO、CO2或HCHO的能量變化圖[反應物O2(g)和生成物H2O(g)略去]。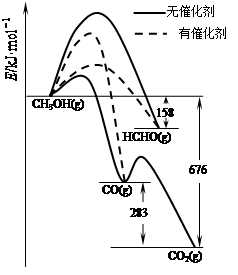
①在有催化劑作用下,CH3OH與O2反應主要生成 (填“CO、CO2或HCHO”)。
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
③在稀硫酸催化下,HCHO可以通過反應生成分子式為C3H6O3的環狀三聚甲醛分子,其分子中同種原子的化學環境均相同。寫出三聚甲醛的結構簡式: 。
④甲醇制取甲醛可用Ag作催化劑,含有AgCl會影響Ag催化劑的活性,用氨水可以溶解除去其中的AgCl,寫出該反應的離子方程式: 。
⑵一種以銅作催化劑脫硫有如下兩個過程:
①在銅的作用下完成工業尾氣中SO2的部分催化氧化,所發生反應為:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O="2n" CuSO4+(2-2n) H2SO4
從環境保護的角度看,催化脫硫的意義為 ;每吸收標準狀況下11.2L SO2,被SO2還原的O2的質量為 g。
②利用下圖所示電化學裝置吸收另一部分SO2,并完成Cu的再生。寫出裝置內所發生反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫單質及其化合物在工農業生產中有著重要的應用。
(1)已知25℃時:SO2(g)+2CO(g)=2CO2(g)+1/xSx(s) △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+3/xSx(s) △H=bkJ/mol。
則COS(g)生成CO(g)與Sx(s)反應的熱化學方程式是 。
(2)雄黃(As4S4)和雌黃(As2S3)是提取砷的主要礦物原料。已知As2S3和HNO3有如下反應:As2S3+10H++ 10NO3?=2H3AsO4+3S+10NO2↑+ 2H2O,當生成H3AsO4的物質的量為0.6 mol反應中轉移電子的數目為 ,
(3)向等物質的量濃度Na2S、NaOH混合溶液中滴加稀鹽酸至過量。其中H2S、HS?、S2?的分布分數(平衡時某物種的濃度占各物種濃度之和的分數)與滴加鹽酸體積的關系如下圖所示(忽略滴加過程H2S氣體的逸出)。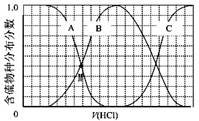
①B表示 。
②滴加過程中,溶液中微粒濃度大小關系正確的是 (填字母)。
a.c(Na+)= c(H2S)+c(HS?)+2c(S2?)
b.2c(Na+)=c(H2S)+c(HS?)+c(S2?)
c.c(Na+)=3[c(H2S)+c(HS?)+c(S2?)]
③NaHS溶液呈堿性,當滴加鹽酸至M點時,溶液中各離子濃度由大到小的順序為 。
(4)工業上用硫碘開路循環聯產氫氣和硫酸的工藝流程如下圖所示: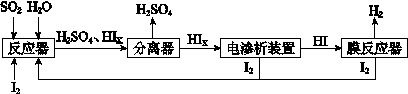
① 寫出反應器中發生反應的化學方程式是 。
② 電滲析裝置如圖所示,寫出陽極的電極反應式 。該裝置中發生的總反應的化學方程式是 。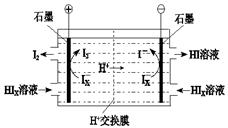
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)等物質的量的下列化合物與足量濃鹽酸反應,得到氯氣的物質的量最多的是
________(填序號)。
已知:MnO4-+H++Cl-―→Mn2++Cl2↑+H2O(未配平)
ClO3-+H++Cl-―→Cl2↑+H2O(未配平)
ClO-+H++Cl-―→Cl2↑+H2O(未配平)
A.KClO3 B.KMnO4 C.MnO2 D.Ca(ClO)2
(2)已知Co2O3在酸性溶液中易被還原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次減弱。下列反應在水溶液中不可能發生的是________(填序號)。
A.3Cl2+6FeI2=2FeCl3+4FeI3
B.Cl2+FeI2=FeCl2+I2
C.Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
D.2Fe3++2I-=2Fe2++I2
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
溴的氧化性介于氯和碘之間,利用這一性質解決下面的問題。
(1)你認為:將含有下列哪種分子或離子的試劑加入到含有Br-的溶液中,可以將Br-氧化為Br2__________。
| A.I2 | B.I | C.Cl2 | D.Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)將廢釩催化劑(主要成分V2O5)與稀硫酸、亞硫酸鉀溶液混合,充分反應,所得溶液顯酸性,含VO2+、K+、SO42-等。寫出該反應的化學方程式_________________________________。
(2)向上述所得溶液中加入KClO3溶液,充分反應后,溶液中新增加了VO2+、Cl-。寫出并配平該反應的離子方程式,并標出電子轉移的數目和方向______________________。
(3)在20.00 mL的0.1 mol·L-1 VO2+溶液中,加入0.195 g鋅粉,恰好完成反應,則還原產物可能是______________________________________________________________。
a.V b.V2+ c.VO2+ d.VO2+
(4)已知V2O5能和鹽酸反應生成氯氣和VO2+。請再寫一個離子反應方程式,說明還原性:SO32->Cl->VO2+__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某探究小組將一批電子廢棄物簡單處理后,得到含Cu、Al、Fe及少量Au、Pt等金屬的混合物,并設計如下制備硫酸銅晶體和無水氯化鐵的方案: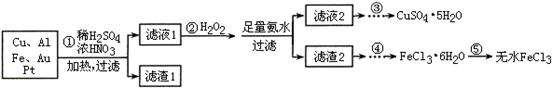
已知:Cu2+ + 4NH3·H2O=[Cu(NH3)4]2+ + 4H2O
請回答下列問題:
(1)步驟①Cu與酸反應的離子方程式為 。
(2)步驟②加H2O2的作用是 ,濾渣2為(填化學式) 。
(3)步驟⑤不能直接加熱脫水的理由是 。
(4)若濾液1中Cu2+的濃度為0.02mol·L-1,則氫氧化銅開始沉淀時的pH =
(已知:Ksp[Cu(OH)2]=2.0×10-20)。
(5)已知:2Cu2++4I-= 2CuI↓+I2 I2+2S2O32-= 2I-+S4O62-
某同學為了測定CuSO4·5H2O產品的質量分數可按如下方法:取3.00g產品,用水溶解后,加入足量的KI溶液,充分反應后過濾、洗滌,將濾液稀釋至250mL,取50mL加入淀粉溶液作指示劑,用0.080 mol·L-1 Na2S2O3標準溶液滴定,達到滴定終點的依據是 。
四次平行實驗耗去Na2S2O3標準溶液數據如下:
| 實驗序號 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3標準溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com