
分析 Na、Na2O2的混合物與足量的水反應得到的氣體是氫氣和氧氣的混合物,將該混合氣體通過放電,恰好完全反應,說明氫氣和氧氣反應的物質的量之比恰好等于它們反應的計量數之比;然后分別根據反應方程式計算出鈉、過氧化鈉的物質的量,再根據m=nM計算出其質量,最后計算出質量之比.
解答 解:Na、Na2O2 的混合物與足量的水反應得到的氣體是氫氣和氧氣的混合物,將該混合氣體通過放電,恰好完全反應,說明氫氣和氧氣反應的物質的量之比恰好等于它們反應的計量數之比,
該混合氣體通過放電,恰好完全反應,根據方程式2H2+O2$\frac{\underline{\;點燃\;}}{\;}$2H2O可知,氫氣和氧氣反應的物質的量之比恰好等于它們反應的計量數之比,即氫氣和氧氣的物質的量之比為2:1,設氫氣為2nmol,則氧氣為nmol,所以2nmol×2+32n=0.36g,則n=0.01mol,
根據2Na+2H2O=2NaOH+H2↑可知,鈉的物質的量為4nmol,鈉的質量為:23g/mol×4nmol=92ng=0.92g;
根據2Na2O2+2H2O=4NaOH+O2↑可知,過氧化鈉的物質的量為2nmol,過氧化鈉的質量為:2nmol×78g/mol=156ng=1.56g,
(1)混合物中過氧化鈉的質量分數是:$\frac{1.56g}{1.56g+0.92g}$×100%=62.9%;
(2)所得溶液的物質的量濃度:c=$\frac{n}{V}$=$\frac{0.04+0.02×2}{0.2}$=0.4mol/L;
答:(1)混合物中過氧化鈉的質量分數為:62.9%;
(2)所得溶液的物質的量濃度為:0.4mol/L.
點評 本題考查混合物計算,題目難度中等,確定混合氣體中氫氣與氧氣的物質的量之比為2:1是解答關鍵,注意掌握鈉、過氧化鈉與水反應的方程式.


科目:高中化學 來源: 題型:選擇題
| A. | 按系統命名法,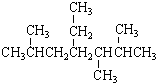 的名稱為2,5,6-三甲基-4-乙基庚烷 的名稱為2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常壓下,鄰二甲苯、間二甲苯、對二甲苯的沸點依次增大 | |
| C. | 已知1mol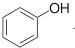 可以與1molNaOH發生反應.則1mol 可以與1molNaOH發生反應.則1mol 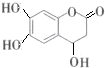 與足量的NaOH溶液發生反應時,需消耗4molNaOH 與足量的NaOH溶液發生反應時,需消耗4molNaOH | |
| D. | 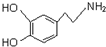 屬于氨基酸,既能與強酸反應,又能與強堿反應 屬于氨基酸,既能與強酸反應,又能與強堿反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 左盤上升 | B. | 右盤下沉 | C. | 仍保持平衡 | D. | 無法判斷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中加入BaCl2溶液,產生白色沉淀,加入HNO3后,白色沉淀不溶解,也無其他現象,說明原溶液中一定含有SO42- | |
| B. | 向某溶液中加鹽酸產生無色無味氣體,該氣體能使澄清的石灰水變渾濁,說明該溶液中一定含有CO32- | |
| C. | 收集氯氣時,用濕潤的KI淀粉試紙放置于瓶口,觀察試紙是否變藍判斷是否收集滿 | |
| D. | 某樣品的焰色反應呈黃色,則該樣品一定是單質鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
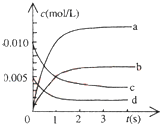 在2L密閉容器內,800℃時反應:2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:
在2L密閉容器內,800℃時反應:2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com