
下列與化學反應能量變化相關的敘述正確的是
A.反應熱就是反應放出的熱量
B.放熱反應的反應速率總是大于吸熱反應的反應速率
C.應用蓋斯定律,可計算某些難以直接測量的反應熱
D.同溫同壓下,H2(g)+Cl2(g)===2HCl(g)在光照和點燃條件下的ΔH不同
科目:高中化學 來源:2016-2017學年山西省高二上第一次月考化學試卷(解析版) 題型:填空題
將2molI2(g)和1molH2置于某2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g) 2HI(g) ΔH<0,并達平衡,HI的體積分數φ(HI)隨時間變化如下圖中曲線(Ⅱ)所示.
2HI(g) ΔH<0,并達平衡,HI的體積分數φ(HI)隨時間變化如下圖中曲線(Ⅱ)所示.

(1)達平衡時,I2(g)的物質的量濃度為 .
(2)若改變反應條件下,在甲條件下ω(HI)的變化如圖曲線(I)所示,在乙條件下ω(HI)的變化如圖曲線(III)所示。則甲條件可能是 (填入下列條件的序號。下同),乙條件可能是 。
①恒溫條件下,擴大反應容器體積
②恒容條件下,降低溫度
③恒溫條件下,縮小反應容器體積
④恒容條件下,升高溫度
⑤恒溫恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2L密閉容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、c 均大于0),發生反應,達平衡時,HI的體積分數仍為0.60,則a、b、c的關系是 。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年寧夏高二上第一次月考化學卷(解析版) 題型:選擇題
已知下列兩個熱化學方程式:
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
CH4(g)+2O2(g)=2H2O(l)+CO2(g) △H=-890.3kJ/mol
實驗測得氫氣和甲烷的混合氣體共5 mol,完全燃燒時放熱為3695kJ,則混合氣體中氫氣和甲烷的體積比為
A.3 : 5 B.1 : 3 C.3 : 2 D.5 : 3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省高二上10月月考化學試卷(解析版) 題型:選擇題
用1.0mol·L-1 NaOH溶液中和某濃度硫酸溶液時,其pH和所加NaOH溶液的體積關系如圖所示。原硫酸溶液的物質的量濃度和完全反應后溶液的總體積是
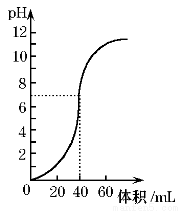
A.1mol·L-1,60mL B.0.5mol·L-1,80mL
C.0.5mol·L-1,40mL D.1mol·L-1.80mL
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省高二上10月月考化學試卷(解析版) 題型:選擇題
常溫下已知兩種一元弱酸HX和HY,如果向NaX溶液中通入少量CO2氣體生成HX和NaHCO3;往NaY溶液中通入少量CO2生成HY和Na2CO3。下列有關敘述正確是
A.酸性由強至弱:HX>HY>H2CO3
B.結合H+的能力:Y->CO32->X->HCO3-
C.溶液堿性:NaX>Na2CO3>NaY>NaHCO3
D.NaX溶液中通入足量CO2后的離子濃度:c(Na+)>c(HCO3-)>c(X-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學試卷(解析版) 題型:填空題
在汽車上安裝三效催化轉化器,可使汽車尾氣中的主要污染物(CO、NOx、碳氫化合物)進行相互反應,生成無毒物質,減少汽車尾氣污染。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ/mol;
2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol。
尾氣轉化的反應之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH__________。
(2)某研究性學習小組在技術人員的指導下,按下列流程探究某種催化劑在不同空燃比(空氣與燃油氣的質量比)條件下對汽車尾氣的催化效果。

①實驗過程中除空燃比不同外,其他條件:汽車尾氣的流速、_____________等必須相同。
②在一定條件下,測得尾氣中的主要污染物的轉化率與空燃比的關系如圖所示。空燃比約為____________時,催化劑對汽車尾氣的催化效果最好。

查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學試卷(解析版) 題型:選擇題
在25℃、10 1 kPa條件下,C(s)、H2(g)、CH3COOH(l)的燃燒熱分別為393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,則2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反應熱為( )
1 kPa條件下,C(s)、H2(g)、CH3COOH(l)的燃燒熱分別為393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,則2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反應熱為( )
A.-488.3 kJ/mol B.+488.3 kJ/mol C.-191 kJ/mol D.+191 kJ/mol
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上學期第二次月考化學試卷(解析版) 題型:填空題
要準確掌握化學基本概念和研究方法。按要求回答下列問題:
(1)下列是某同學對有關物質進行分類的列表:
堿 | 酸 | 鹽 | 堿性氧化物 | 酸性氧化物 | |
第一組 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
第二組 | NaOH | HCl | NaCl | Na2O | CO |
第三組 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
每組分類均有錯誤,其錯誤的物質分別是______________(填化學式,下同)、________、________。
(2)膠體和溶液的本質區別是_____________________;
鑒別膠體和溶液所采用的方法是觀察是否能發生________現象。
(3)下列3個反應,按要求填寫相關量。
①2Na2O2+2H2O==4NaOH+O2↑反應中,每消耗1 mol Na2O2生成________g O2;
②2NaHCO3 Na2CO3+H2O+CO2↑反應中,每消耗168 g NaHCO3,標況下生成______L CO2;
Na2CO3+H2O+CO2↑反應中,每消耗168 g NaHCO3,標況下生成______L CO2;
③Cl2+H2O=HCl+HClO反應中,標況下每消耗22.4 L Cl2,轉移________ mol電子。
(4)在一個密閉容器中放入M、N、Q、P四種物質,在一定條件下發生化學反應,一段時間后,測得有關數據如下表,按要求回答下列問題:
物質 | M | N | Q | P |
反應前質量(g) | 50] | 1 | 3 | 12 |
反應后質量(g) | X | 26 | 3 | 30 |
①該變化的基本反應類型是________反應;
②物質Q在反應中起的作用是________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年寧夏高一上第一次月考化學試卷(解析版) 題型:實驗題
(1)如何鑒定某溶液中含有SO42﹣?請答出實驗步驟、現象和結論:
(2)在分液漏斗中用四氯化碳與水混合后分層,但上下兩層均無色,如何用實驗方法知道那一層是水層。試設計一種最簡便的判斷方法: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com