
【題目】下列關于鈉及其化合物的說法正確的是( )
A.將剩余的金屬鈉丟棄在廢紙簍里
B.小蘇打可用于制作糕點的膨松劑,蘇打可用于治療胃酸過多
C.侯氏制堿法的工藝過程中應用了物質溶解度的差異
D.生活中用熱的燒堿溶液洗去油污
科目:高中化學 來源: 題型:
【題目】科學處理NOx、SO2等大氣污染物,對改善人們的生存環境具有重要的現實意義。
(1)利用甲烷催化還原氮氧化物。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJmol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJmol-1
則CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=___kJmol-1。
(2)利用氧化氮氧化物的流程如下:
![]()
已知反應I的化學方程式為2NO+ClO2+H2O=NO2+HNO3+HCl,
若反應I中轉移3mol電子,則反應Ⅱ中可生成N2的體積為_________L(標準狀況下)。
(3)常溫下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收過程中水的電離平衡_________(填“增大”、“減小”或“不變”);試計算溶液中c(SO32-)/c(HSO3-)=_______。(常溫下H2SO3的電離常數:Ka1=1×10-2 mol/L,Ka2=6.0×10-8mol/L)
(4)利用Fe2(SO4)3溶液也可處理SO2廢氣,所得Fe2+溶液有很多重要用途。保存1.8mol·L-1的FeSO4溶液時,為防止溶液中Fe2+被氧化,常加入________;為確保溶液中不出現渾濁,應調節溶液的pH不超過______。(常溫下,Ksp[Fe(OH)2]=1.8×10-16)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是
A. 分子中含兩個一CH3、分子式為C5H11Cl的同分異構體有3種
B. HNO3能與苯、甲苯、甘油、纖維素等有機物發生取代反應
C. 石油裂解的目的是為了提高輕質液體燃料的產量和質量
D. 有機物![]() 的一溴代物有4種
的一溴代物有4種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某芳香族化合物A的相對分子質量小于150,所含氫氧元素質量比為1:8,完全燃燒后只生成CO2和H2O。取等質量的A分別與足量NaHCO3和Na反應,生成的氣體在同溫同壓下的體積比為1:1。工業常用A來合成藥物B及醫藥中間體G,流程如下:
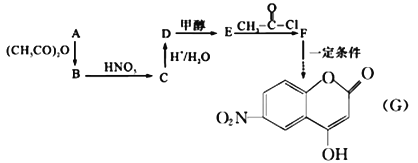
已知: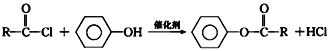

(1)A的結構簡式為_____________________。
(2)寫出D含有的官能團的名稱:____________________________。
(3)合成路線中設計A→B、C→D兩步反應的目的是__________________________________________。
(4)G的分子式:________________________。
(5)寫出F與過量NaOH水溶液共熱時反應的化學方程式:_________________________________________。
(6)B的芳香族同分異構體中,既能與NaHCO3發生反應,又能發生銀鏡反應和水解反應的____種,其中核磁共振譜有五組峰、且峰面積之比為2:2:2:1:1的同分異構體結構簡式為______________(寫出一種即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人工光合作用能夠借助太陽能,用CO2和H2O制備化學原料。如圖是通過人工光合作用制備HCOOH的原理示意圖,下列說法不正確的是
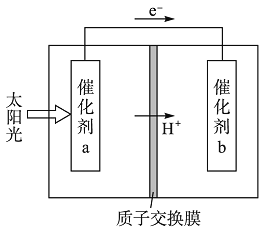
A. 該過程是將太陽能轉化為化學能的過程
B. 催化劑a表面發生氧化反應,有O2產生
C. 催化劑a附近酸性減弱,催化劑b附近酸性增強
D. 催化劑b表面的反應是CO2+2H++2e-=HCOOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是一種常用的化工原料,如合成氨和尿素[CO(NH2)2]等。
(1)以H2合成CO(NH2)2的有關熱化學方程式有:
①N2(g)+3H2(g)===2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+![]() CO2(g)===
CO2(g)===![]() NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)===CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
則N2(g)、H2(g)與CO2(g)反應生成CO(NH2)2(s)和H2O(l)的熱化學方程式為_______________________________________________________。
(2)電解制H2的原理為C(s)+2H2O(l)![]() CO2(g)+2H2(g)。某學習小組擬以二甲醚(CH3OCH3)-空氣堿性燃料電池為電源,電解煤漿液(由煤粉與稀硫酸組成)探究上述原理,裝置如圖所示。
CO2(g)+2H2(g)。某學習小組擬以二甲醚(CH3OCH3)-空氣堿性燃料電池為電源,電解煤漿液(由煤粉與稀硫酸組成)探究上述原理,裝置如圖所示。
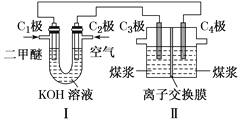
①分別寫出電極C1和C3的電極反應式__________________;___________________。
②離子交換膜可能是________(填字母)。
a.陽離子交換膜 b.陰離子交換膜 c.質子交換膜
③已知4.6 g二甲醚參與反應,假設裝置Ⅰ的能量轉化率為100%,C4極收集到11.2L(標準狀況)氣體,裝置Ⅱ的電流效率η=________。![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質分類的正確組合是( )
堿 | 酸 | 鹽 | 酸性氧化物 | |
A | 純堿 | 鹽酸 | 燒堿 | 二氧化硫 |
B | 燒堿 | 硫酸 | 食鹽 | 一氧化碳 |
C | 苛性鈉 | 醋酸 | 石灰石 | 水 |
D | 苛性鉀 | 碳酸 | 蘇打 | 三氧化硫 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com