
(原創)將SO2和NO2混合氣體通入BaCl2溶液中,其結果是( )
A.2種氣體都被吸收,并有白色沉淀析出
B.生成BaSO4和BaSO32種沉淀
C.2種氣體都被吸收,并有白色沉淀析出,還有無色氣體從溶液中逸出,遇空氣變紅棕色
D.生成BaSO3沉淀,NO2從溶液中逸出
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
(原創)下列敘述錯誤的是( )
A、標準狀況下,1molNO和1molSO2體積都為22.4L
B、NO和SO2熔沸點都較低,在常溫下都是無色氣體
C、SO2有毒而NO對人無害
D、SO2和NO2都是大氣染物,是形成酸雨的主要物質
查看答案和解析>>
科目:高中化學 來源:2012屆山東省濰坊市三縣市高三上學期期中聯合考試化學試卷 題型:填空題
(11分)(1)化學是一門以實驗為基礎的學科,化學實驗是化學學習的重要內容。根
據你掌握的知識判斷,下列實驗操作的描述中正確的是 。
(填寫下列各項序號)
A.任何從試劑瓶中取出的藥品,若有剩余均不能再放回原試劑瓶
B.用稀鹽酸洗滌盛放過石灰水的試劑瓶
C.配制H2SO4溶液時,可先在量筒中加入一定體積的水,再在攪拌下慢慢加入濃硫酸
D.各放一張質量相同的濾紙于天平的兩托盤上,將NaOH固體放在左盤紙上稱量
E.Na2CO3溶液不能保存在帶有磨口玻璃塞的試劑瓶中
F.將用水潤濕的PH試紙浸入稀鹽酸中,測定溶液的PH
(2)據報道,目前一些地區酸 雨、灰霾和光化學煙霧等區域性大氣污染突出,嚴重威脅
雨、灰霾和光化學煙霧等區域性大氣污染突出,嚴重威脅
群眾健康,影響環境安全。二氧化硫和氮的氧化物是大氣的主要污染物,關注臭氧層、
防止和治理環境污染是當前環保工作的重要研究內容之一。
①汽 車尾氣主要含有CO2、CO、SO2、NO及汽油、柴油等到物質,這種尾氣越來越成
車尾氣主要含有CO2、CO、SO2、NO及汽油、柴油等到物質,這種尾氣越來越成
為城市空氣污染的主要來源,汽車尾氣中的CO來自  ,
,
NO來自(用方程式表示) 。
②空氣中微量的臭氧對人有益,濃度過大則是一種污染氣 體,臭氧作為強氧化劑,幾乎
體,臭氧作為強氧化劑,幾乎
能與任何生物組織反應。下列有關說法正確的是 。
A.停止使用氟里昂是為了保護臭氧層
B.光化學煙霧與大氣臭氧的生成有關
C.家用電器消毒柜中產生的臭氧能夠高效殺菌消毒
D.臭氧能使濕潤的碘化鉀一淀粉試紙變藍
③在一定條件下用氨可將氮氧化物轉化為 無毒氣體。同溫同壓下,7LNH3恰好將6LNO
無毒氣體。同溫同壓下,7LNH3恰好將6LNO
和NO2的混合氣體完全轉化為N2,則原混合氣體中NO和NO2的體積比是 。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
空氣質量與我們的健康息息相關,目前我國通過監測6項污染物的質量濃度來計算空氣質量指數(AQI),SO2、NO2和CO是其中3項中的污染物。
(1)上述3種氣體直接排入空氣后會引起酸雨的氣體有 (填化學式)。
(2)早期人們曾經使用鉛室法生產硫酸,其主要反應為:
SO2(g)+NO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g)![]() 2SO3(g) ΔH=a kJ·mol-1
2SO3(g) ΔH=a kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=b kJ·mol-1
2NO2(g) ΔH=b kJ·mol-1
則SO2(g)+NO2(g)![]() SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。
②一定溫度下,向固定體積為2 L的密閉容器中充入SO2和NO2各1 mol,發生反應:
SO2(g)+NO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
下列事實中不能說明該反應達到平衡狀態的是 (選填序號)。
a.體系壓強保持不變 b.混合氣體的顏色保持不變
c.NO的物質的量保持不變 d.每生成1 mol SO3的同時消耗1 mol NO2
③測得②中反應5 min末到達平衡,此時容器中NO與NO2的體積比為3︰1,則這段時間內SO2的反應速率υ(SO2)= ,此反應在該溫度下的平衡常數K= 。
(3)甲醇日趨成為重要的有機燃料,通常利用CO和H2合成甲醇,其反應的化學方程式為CO(g)+2H2(g)![]() CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉化率(α)與溫度(T)、壓強(P)的關系如圖所示:
CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉化率(α)與溫度(T)、壓強(P)的關系如圖所示:
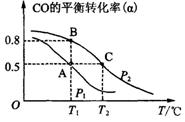
①上述合成甲醇的反應為 反應(填“放熱”或“吸熱”)。
②A、B、C三點的平衡常數KA、KB、KC的大小關系為 。
③若將達到平衡狀態A時生成的甲醇用于構成甲醇一氧氣燃料電池,電解質溶液為KOH濃溶液,則該電池工作時正極的電極反應式為 ,理論上通過外電路的電子最多為 mol。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com