
| A. | ③⑤⑥⑧ | B. | ①②④⑦ | C. | ③⑤ | D. | ③④⑤⑥ |
分析 ①根據質量、摩爾質量、分子數、電子數、阿伏伽德羅常數之間的關系式計算判斷;
②根據同溫、同壓下,體積、氣體摩爾體積、分子數、原子數之間的關系式計算判斷;
③根據體積、氣體摩爾體積、分子數、原子數之間的關系式計算判斷;
④根據氣體摩爾體積的適用范圍判斷;
⑤根據體積、密度、摩爾質量、分子數、原子數、阿伏伽德羅常數之間的關系式計算判斷;
⑥二氧化硅中含有4個Si一0鍵;
⑦根據物質的量與轉移電子之間的關系判斷;
⑧鋁離子易水解.
解答 解:①每個D2O分子中含有10個電子,但18gD2O的物質的量小于1mol,所以18gD2O含有的電子數小于10NA,故錯誤;
②同溫、同壓下,相同體積的氟氣和氬氣的物質的量相等,但氟氣是雙原子分子,氬氣是單原子分子,所以所含的原子數不等,故錯誤;
③標準狀況下,11.2L以任意比例混合的氮氣和氧氣的物質的量是0.5mol,氮氣和氧氣都是雙原子分子,所以標準狀況下,11.2L以任意比例混合的氮氣和氧氣所含的原子數為NA,故正確;
④標準狀況下,SO3是固體,氣體摩爾體積不適用于該物質,故錯誤;
⑤4℃時,水的密度是1g/mL,所以5.4mL的水的質量是5.4g,物質的量是0.3mol,所含的原子總數為0.9NA,故正確;
⑥60gSiO2物質的量=$\frac{60g}{60g/mol}$=1mol,結合二氧化硅中含有4個Si一0鍵分析,60g SiO2晶體中含有4NA個Si一0鍵,故錯誤;
⑦2mol過氧化鈉與水反應轉移電子數為2NA,所以1molNa2O2與水完全反應時轉移電子數為NA,故錯誤;
⑧鋁離子易水解,離子總數小于NA,故錯誤;
故選C.
點評 本題考查阿伏加德羅常數的有關計算和判斷,題目難度中等,注意明確標況下氣體摩爾體積的使用條件,掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,準確弄清分子、原子、原子核內質子中子及核外電子的構成關系.試題有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力.


 優學名師名題系列答案
優學名師名題系列答案科目:高中化學 來源: 題型:解答題
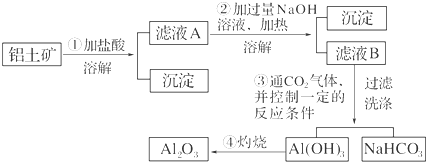
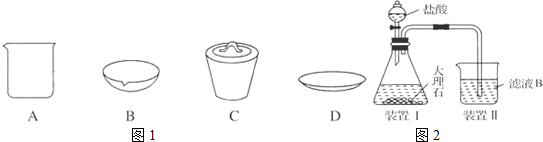
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵和稀硫酸反應:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 鈉和冷水反應 Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氫氧化鋇溶液與稀 H2SO4 反應:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O | |
| D. | 少量NaHCO3溶液與Ca(OH)2溶液反應:OH-+HCO3-═CO32-+H2O |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二上第一次月考化學卷(解析版) 題型:選擇題
圖中的曲線表示的是其他條件一定時,反應:2NO+02 2N02 △H<0中N0的平衡轉化率與溫度的關系。圖中標有a、b、c、d四點,其中表示未達到平衡狀態,且v(正)﹤v(逆)的點是 ( )
2N02 △H<0中N0的平衡轉化率與溫度的關系。圖中標有a、b、c、d四點,其中表示未達到平衡狀態,且v(正)﹤v(逆)的點是 ( )
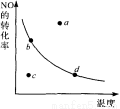
A.a點 B.b點 C. c點 D.d點
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x)kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y)kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y)kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(8x-2y)kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應中B2O3是氧化劑 | B. | 若消耗2.24LNH3理論上可得2.5gBN | ||
| C. | 填料的作用可使反應物充分接觸 | D. | 反應時NH3需要用無水CaCl2干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
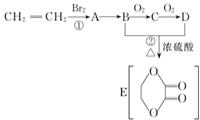 由乙烯和其他無機原料合成環狀酯,其合成過程如下(水及其他無機產物均已省略)
由乙烯和其他無機原料合成環狀酯,其合成過程如下(水及其他無機產物均已省略)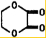 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com