
【題目】某研究性學習組利用H2C2O4溶液和酸性KMnO4溶液之間的反應來探究“外界條件改變對化學反應速率的影響”,實驗如下:
實驗序號 | 實驗溫度 | KMnO4溶液 | H2C2O4溶液 | H2O | 溶液褪色時間 | ||
V(mL) | C(mol/L) | V(mL) | C(mol/L) | V(mL) | t(s) | ||
A | 293K | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313K | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(1)通過實驗A、B,可探究出_______的改變對反應速率的影響,其中V1=_____,T1=_____,通過實驗/span>_______可探究出溫度變化對化學反應速率的影響。
(2)若t1<8,則由實驗A、B可以得出的結論是______________________________;利用實驗B中數據計算,用KMnO4的濃度變化表示的反應速率為____________。
(3)該反應中有無色無味氣體產生且錳被還原為Mn2+,寫出相應反應的離子方程式_________________________。
(4)該小組的一位同學通過查閱資料發現:反應一段時間后該反應速率會加快,造成此種變化的原因是反應體系中的某種粒子對KMnO4與H2C2O4之間的反應有某種特殊的作用,則該作用是_______________,相應的粒子最有可能是(填符號)_______。
【答案】 濃度 1 293K BC 其他條件相同時,增大反應物濃度,反應速率增大 8.3×10-4mol/(L·s) 2MnO42-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 作催化劑 Mn2+
【解析】(1)實驗A、B中KMnO4溶液的濃度相等,可探究出在相同溫度下,H2C2O4溶液濃度的改變對反應速率的影響,其中V1=2mL+4mL-2mL-3mL=1mL,T1=293K;B和C實驗中,V2=3mL時,兩實驗反應物的濃度均相同,可探究不同溫度對化學反應速率的影響;
(2)因A中H2C2O4溶液濃度濃度比B中大,若t1<8,則由實驗A、B可以得出的結論是其他條件相同時,增大反應物濃度,反應速率增大;利用實驗B中數據計算,用KMnO4的濃度變化表示的反應速率為![]() =8.3×10-4mol/(L·s);
=8.3×10-4mol/(L·s);
(3)反應中有無色無味氣體CO2產生且錳被還原為Mn2+,則發生反應的離子方程式為2MnO42-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(4)KMnO4與H2C2O4反應后的溶液中出現了Mn2+,Mn2+可能是此反應的催化劑,促進了反應速率加快。


 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:
【題目】化學與生活密切相關。下列敘述錯誤的是( )
A. 硅膠、鐵粉均可作為食品包裝中的抗氧化劑
B. 福爾馬林能防腐,但不能用于食品保鮮
C. 可溶性的鋁鹽和鐵鹽可用作凈水劑
D. 人工合成的硅橡膠是既耐高溫又耐低溫的橡膠
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某工廠用軟錳礦(主要成分是MnO2,含少量Al2O3和SiO2)和閃鋅礦(主要成分是ZnS,含少量FeS、CuS等雜質)為原料制備MnO2和Zn(干電池原料),其簡化流程如下:
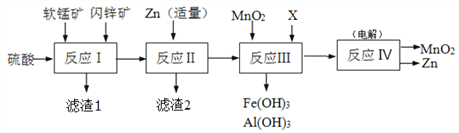
已知:反應Ⅰ中所有金屬元素均以離子形式存在。
回答下列問題:
(1)濾渣1中除了SiO2以外,還有一種淡黃色物質,該物質是由MnO2、CuS與硫酸共熱時產生的,請寫出該反應的離子方程式________________________________。
(2)反應Ⅱ中加入適量金屬鋅的目的是為了回收某種金屬,濾渣2的主要成分是______(填名稱)。
(3)反應Ⅲ中MnO2的作用是______,另外一種物質X可以是______。(填字母代號)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反應Ⅳ中電極均是惰性電極,寫出陽極電極反應式_______________。本工藝可以循環利用的物質有MnO2、Zn和_____。
(5)已知:H2S的電離常數K1=1.0×107,K2=7.0×1015。0.1 mol/L NaHS的pH___7(填“>”“=”或“<”),理由是________________________________________。
(6)在廢水處理領域中常用H2S將Mn2+轉化為MnS除去,向含有0.020 mol·L1 Mn2+廢水中通入一定量的H2S氣體,調節溶液的pH=a,當HS濃度為1.0×104 mol·L1時,Mn2+開始沉淀,則a=________。[已知:Ksp(MnS)=1.4×1015]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒容密閉容器中進行的反應:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H 。在某壓強下起始時按不同氫碳比[n(H2)/n(CO2)]投料(見右圖中曲線①②③),測得CO2的平衡轉化率與溫度關系如下圖所示,
C2H5OH(g)+3H2O(g) △H 。在某壓強下起始時按不同氫碳比[n(H2)/n(CO2)]投料(見右圖中曲線①②③),測得CO2的平衡轉化率與溫度關系如下圖所示,

下列有關說法正確的是
A.該反應:△H >0
B.氫碳比:①<②<③
C.其它條件不變的情況下,縮小容器的體積可提高CO2的轉化率
D.若起始CO2濃度為2mol·L-1、H2為4mol·L-1,在圖中曲線③氫碳比條件下進行,則400K時該反應的平衡常數數值約為1.7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)能源危機是當前全球問題,開源節流是應對能源危機的重要舉措。下列做法有助于能源“開源節流”的是________(填序號)。
a.大力發展農村沼氣,將廢棄的秸稈轉化為清潔高效的能源
b.大力開采煤、石油和天然氣以滿足人們日益增長的能源需求
c.開發太陽能、水能、風能、地熱能等新能源、減少使用煤、石油等化石燃料
d.減少資源消耗,增加資源的重復使用、資源的循環再生
(2)金剛石和石墨均為碳的同素異形體,它們燃燒氧氣不足時生成一氧化碳,充分燃燒生成二氧化碳,反應中放出的熱量如下圖所示。

①在通常狀況下,金剛石和石墨中_______更穩定,石墨的燃燒熱為__________。
②12 g石墨在一定量空氣中燃燒,生成氣體36 g,該過程放出的熱量為_______。
(3)由石墨轉變成金剛石的反應的ΔS=+1.6J·mol-1·K-1,則為了保持此反應自發進行,溫度應______(填“低于”或“高于”)______K。
(4)已知熔融碳酸鹽燃料電池的工作原理如下圖所示:

①放電過程中K+和Na+向電極_______(填“A”或“B”)移動。
②該電池的負極反應式為_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關能量轉換的說法正確的是( )
A. 煤燃燒是化學能全部轉化為熱能的過程
B. 化石燃料和植物燃料燃燒時放出的能量均來源于太陽能
C. 動物體內葡萄糖被氧化成CO2是熱能轉變成化學能的過程
D. 植物通過光合作用將CO2轉化為葡萄糖是太陽能轉變成熱能的過程
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中錯誤的是
①化學性質相似的有機物是同系物 ②分子組成相差一個或幾個CH2的有機物是同系物 ③若烴中碳、氫元素的質量分數相同,它們必是同系物 ④具有同一通式的物質屬于同系物
A. 只有①②③ B. 只有①②④ C. 只有①③④ D. ①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中既能使溴水和酸性KMnO4溶液褪色,又能發生銀鏡反應的是( )
A. CH3—CH=CH2 B. CH2=CH—CH2OH
C. CH3CH2CH2OH D. CH2=CH—CHO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列哪一實例能證明微量元素是生命活動必需的 ( )
A. Mg是葉綠素的組成成分 B. 油菜缺少B時只開花不結果
C. 哺乳動物體內Ca鹽含量太低,會抽搐 D. 缺少P會影響ATP的合成
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com