
【題目】常溫下,將兩個鉑電極插入一定量的硫酸鈉飽和溶液中進行電解,通過一段時間后,在陽極產生a mol氣體,同時有WgNa2SO4·10H2O析出,若溫度不變,此時剩余溶液中溶質的質量分數為( )
A.![]() ×100%B.
×100%B.![]() %C.
%C.![]() %D.
%D.![]() %
%
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:
【題目】普羅帕酮,為廣譜高效膜抑制性抗心律失常藥。具有膜穩定作用及競爭性β受體阻滯作用。能降低心肌興奮性,延長動作電位時程及有效不應期,延長傳導。化合物I是合成普羅帕酮的前驅體,其合成路線如圖:
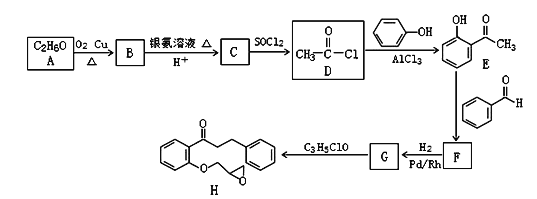
已知:CH3COCH3+CH3CHO![]() CH3COCH=CHCH3+H2O
CH3COCH=CHCH3+H2O
回答下列問題:
(1)H的分子式為_____________;化合物E中含有的官能團名稱是_________。
(2)G生成H的反應類型是______。
(3)F的結構簡式為_____。
(4)B與銀氨溶液反應的化學方程式為__________。
(5)芳香族化合物M與E互為同分異構體,M中除苯環外,不含其他環狀結構,且1molM能與2molNaOH反應,則M的結構共有___種,其中能發生銀鏡反應且核磁共振氫譜上顯示4組峰的M的結構簡式為:_______ 。
(6)參照上述合成路線,以2-丙醇和苯甲醛為原料(無機試劑任選),設計制備![]() 的合成路線:____。
的合成路線:____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Cu2O是重要的催化劑和化工原料,工業上制備Cu2O的主要反應如下:
①C(s)+CO2(g)2CO(g) ΔH=+172.5 kJ·mol-1
②CO(g)+2CuO(s) Cu2O(s)+CO2(g) ΔH=-138.0 kJ·mol-1
(1)C與CuO反應生成Cu2O和CO的熱化學方程式為_______。
(2)一定溫度下,向5L恒容密閉容器中加入1molCO和2 molCuO,發生反應②,5 min時達到平衡,測得容器中CuO的物質的量為0.8mol。
①0~5 min內,用CO2表示的反應速率v(CO2)=____。
②CO的平衡轉化率α=_______。
(3)向5L密閉容器中加入1molC和1molCO2,發生反應①,CO2、CO的平衡體積分數(φ)與溫度(T)的關系如圖所示:
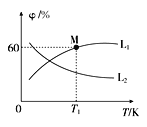
①能表示CO2的平衡體積分數與溫度關系的曲線為____(填“L1”或“L2”),理由為_______。
②溫度為T1時,該反應的平衡常數K=_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式不正確的是( )
A.氫氧化鐵溶于鹽酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B.用惰性電極電解飽和食鹽水:2Cl- + 2H2O![]() 2OH- + H2↑+ Cl2↑
2OH- + H2↑+ Cl2↑
C.過氧化鈉投入重水中:2Na2O2 + 2D2O = 4Na+ + O2↑+ 4OD-
D.向氫氧化鋇溶液中逐滴加入少量碳酸氫鈉溶液:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有機化學反應方程式及反應類型均正確的是
選項 | 化學反應方程式 | 反應類型 |
A | CH3COOH+CH3CH2OH | 酯化反應 |
B | CH4+Cl2 | 置換反應 |
C | CH2=CH2+Br2 CH3CHBr2 | 加成反應 |
D |
| 取代反應 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聯合國將2019年定為“國際化學元素周期表年”,以紀念門捷列夫發現元素周期律150周年。元素周期律把元素及其化合物納入一個統一的理論體系,為系統研究元素及其化合物提供了科學方法,為發現和探索新元素、新物質提供了有效思路。
【1】為紀念門捷列夫,科學家將1955年人工合成的一種新元素用符號“Md”表示,中文命名為“鍆”。核素![]() Md的質量數為( )
Md的質量數為( )
A.101B.157C.258D.359
【2】Mg和Si都屬于元素周期表第3周期元素,它們原子結構中相同的是( )
A.質子數B.電子層數C.核外電子數D.最外層電子數
【3】判斷Cl的非金屬性比S的強,可依據的事實是( )
A.HCl的熱穩定性比H2S的強B.氯氣能溶于水,硫難溶于水
C.常溫下,氯單質呈氣態,硫單質呈固態D.AgCl是白色固體,Ag2S是黑色固體
【4】鋰是第2周期ⅠA族元素,下列有關鋰元素性質推測正確的是( )
A.最高化合價為+2B.原子半徑比鈉的大
C.單質與水的反應比鈉更劇烈D.最高價氧化物對應的水化物堿性比鈉的弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新技術的開發應用,不僅有利于改善環境質量,而且能充分開發“廢物”的潛在價值。
回答下列問題:
(1)用煙道氣與氫氣來合成甲醇涉及到如下幾個反應:
①CO(g)+2H2(g)=CH3OH(g) △H=-91kJ·mol-1
②2CO2(g)=2CO(g)+O2(g) △H=+566kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
④CO2(g)+3H2(g)=CH3OH(g)+H2O(g)H=__kJ·mol-1。
(2)在容積均為2L的兩個恒容密閉容器中發生反應CO(g)+H2O(g)![]() CO2(g)+H2(g),有關數據如下:
CO2(g)+H2(g),有關數據如下:

①800°C時該反應的平衡常數K=__。
②容器2中x=__,n=___。
③若800℃起始時,在2L恒容密閉容器中加入CO、H2O、CO2、H2各1mol,則此時v正__v逆(填“>”“<”或“=”)。
(3)反應(NH4)2CO3+H2O+CO2![]() 2NH4HCO3OH可用于捕捉空氣中的CO2,為研究溫度對(NH4)2CO3捕獲CO2效率的影響,在某溫度T1下,將一定量的(NH4)2CO3溶液置于密閉容器中,并充入一定量的CO2氣體,在t時刻,測得容器中CO2氣體的濃度。然后分別在溫度為T2、T3、T4、T5下,保持其他初始實驗條件不變,重復上述實驗,經過相同時間測定CO2氣體的濃度,得到的曲線圖如圖:
2NH4HCO3OH可用于捕捉空氣中的CO2,為研究溫度對(NH4)2CO3捕獲CO2效率的影響,在某溫度T1下,將一定量的(NH4)2CO3溶液置于密閉容器中,并充入一定量的CO2氣體,在t時刻,測得容器中CO2氣體的濃度。然后分別在溫度為T2、T3、T4、T5下,保持其他初始實驗條件不變,重復上述實驗,經過相同時間測定CO2氣體的濃度,得到的曲線圖如圖:
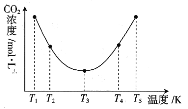
①H__0(填“>”“<”或“=”)。T1~T2區間,c(CO2)變化的原因是___。
②已知常溫下NH3·H2O的電離常數K=1.8×10-5,碳酸的電離常數K1=4.4×10-7、K2=4.7×10-11,則恰好完全反應時所得的NH4HCO3溶液中c(H+)__c(OH-)(填“>”“<”或“=”)。
③在圖中所示五種溫度下,該反應的平衡常數最大的溫度是__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究發現,鋁元素能損害人的腦細胞。適當地補充碘元素可預防甲狀腺腫大,但攝入過多也會導致甲狀腺腫大,因此補充人體所需的元素時也要適可而止。試回答下列問題:
(1)Fe也是人體需要補充的元素之一,試寫出Fe2+的核外電子排布式:__。
(2)與Al同一周期的Na、Mg元素也是人體所需元素,Na、Mg、Al基態原子第一電離能的大小關系是__。
(3)氯化鋁的熔點是194℃,氧化鋁的熔點是2054℃,但是工業上不能用電解熔融氯化鋁的方法獲取鋁單質,這是因為__。
(4)F與I是同一主族的元素,BeF2與H2O都是由三個原子構成的共價化合物分子,二者分子中的中心原子Be和O的雜化方式分別為__、__,BeF2分子的立體構型是___,H2O分子的立體構型是__。
(5)I2晶體的晶胞結構如圖所示,該晶胞中含有__個I2分子,設該晶胞的晶胞參數為acm,則I2的密度是__g·cm-3。
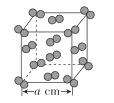
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學準備用下圖所示裝置制取H2還原氧化銅,在實驗中發現稀硫酸不足,與鋅粒無法接觸而又無其他酸液可加入,經思考后他從長頸漏斗中加入適量的合適試劑完成了實驗,下列試劑中不合適的是
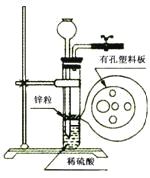
A.苯B.四氯化碳C.酒精D.KCl溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com