
【題目】NA為阿伏加德羅常數的值。下列說法正確的是
A. 常溫常壓下,7.0 g由丁烯與丙烯組成的混合氣體中含有的氫原子數目為NA
B. T ℃時,1 L pH=6的純水中,含OH-的數目為10-8NA
C. 向1 L的密閉容器中充入46 g NO2氣體,容器中氣體的分子數為NA
D. 標準狀況下,1 mol Na2O2與22.4 L SO2反應,轉移電子數為NA
【答案】A
【解析】
A.常溫常壓下,7.0由丁烯與丙烯組成的混合氣體中含有CH2原子團的物質的量為![]() =0.5mol,則含有的氫原子數目為:0.5mol×2×NA=NA,故A正確;B、pH=6的純水中c(H+)=10-6mol/L,而純水顯中性,故純水中c(OH-)=10-6mol/L,則氫氧根的物質的量n=cV=10-6mol/L×1L=10-6mol,個數為10-6NA,故B錯誤;C.NO2中存在平衡:2NO2N2O4,導致分子個數減小,則容器中氣體分子個數小于NA個,故C錯誤;D. 標準狀況下,22.4 L SO2為1mol,1mol Na2O2與1molSO2反應生成1mol硫酸鈉,轉移了2mol電子,轉移的電子數為2NA,故D錯誤;故選A。
=0.5mol,則含有的氫原子數目為:0.5mol×2×NA=NA,故A正確;B、pH=6的純水中c(H+)=10-6mol/L,而純水顯中性,故純水中c(OH-)=10-6mol/L,則氫氧根的物質的量n=cV=10-6mol/L×1L=10-6mol,個數為10-6NA,故B錯誤;C.NO2中存在平衡:2NO2N2O4,導致分子個數減小,則容器中氣體分子個數小于NA個,故C錯誤;D. 標準狀況下,22.4 L SO2為1mol,1mol Na2O2與1molSO2反應生成1mol硫酸鈉,轉移了2mol電子,轉移的電子數為2NA,故D錯誤;故選A。


 一諾書業暑假作業快樂假期云南美術出版社系列答案
一諾書業暑假作業快樂假期云南美術出版社系列答案科目:高中化學 來源: 題型:
【題目】下列表示水解的離子方程式正確的是
A. CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
B. NH4++H2O![]() NH4OH+H+
NH4OH+H+
C. S2-+2H2O![]() H2S+2OH-
H2S+2OH-
D. HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,已知AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲線如圖所示,下列說法錯誤的是
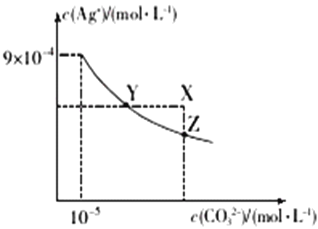
A. Ag2CO3的Ksp為8.1×10-12
B. Ag2CO3(s)+2Cl-(aq)2AgCl(s)+CO32-(aq)的平衡常數K=2.5×108
C. 在Ag2CO3的飽和溶液中加入K2CO3(s)可使c(CO32-)增大(由Y點到Z點)
D. 在0.001molL-1AgNO3溶液中滴入同濃度的KCl和K2CO3的混合溶液,CO32-先沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖1所示,某同學設計了一個燃料電池并探究氯堿工業原理和粗銅的精煉原理,其中乙燒杯中X為陽離子交換膜。請按要求回答相關問題:
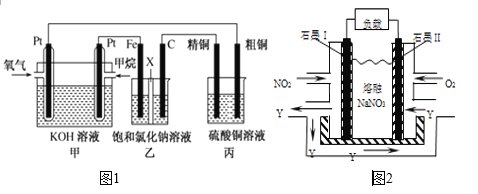
(1)甲烷燃料電池負極電極反應式是___________;正極電極反應式是___________________
(2)石墨(C)為__________極,其電極反應式為____________________________;乙中總反應的離子方程式為__________________________________________________
(3)若在標準狀況下,有2.24 L氧氣參加反應,則丙裝置中陰極析出銅的質量為_________g ;
(4)若將甲裝置中的甲烷換成甲醇(CH3OH),KOH溶液換成稀硫酸,則負極電極反應式為___________,消耗等量氧氣時,需要甲烷與甲醇的物質的量之比為_________。
(5)NO2、O2和熔融NaNO3可制作燃料電池,其原理見圖2,該電池在使用過程中石墨I電極上生成氧化物Y,其電極反應式為________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容容器中,當下列哪些物理量不再發生變化時,表明反應A(s)+2B(g)![]() C(g)+D(g)已達到平衡狀態( )
C(g)+D(g)已達到平衡狀態( )
①混合氣體的壓強 ②混合氣體的密度 ③ B的物質的量濃度 ④混合氣體的總物質的量 ⑤混合氣體的平均相對分子質量 ⑥v(C)與v(D)的比值 ⑦混合氣體的總質量 ⑧C、D的分子數之比為1∶1
A. ②③④⑤ B. ①③⑤⑦ C. ②③⑤⑦ D. ②③⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于裂解和裂化的敘述不正確的是( )
①裂解與裂化的產物都含有不飽和烴 ②裂解與裂化都是為了得到氣態烴 ③裂解與裂化的原料都是石油分餾產品 ④裂解與裂化都是為了得到輕質油
A.①②B.②③C.①③D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上通常利用SiO2 和碳反應來制取硅,寫出反應的化學方程式___________________。
工業上還可以利用鎂制取硅,反應為2Mg+SiO2 = 2MgO+Si,同時會發生副反應:2Mg + Si = Mg2Si。如圖是進行Mg與SiO2反應的實驗裝置,試回答下列問題:

(1)由于O2和H2O(g)的存在對該實驗有較大影響,實驗中應通入氣體X作為保護氣,試管中的固體藥品可選用________(填序號)。
a.石灰石 b.鋅粒 c.純堿
(2)實驗開始時,必須先通一段時間X氣體,再加熱反應物,其理由是 ___________________________;當反應引發后,移走酒精燈,反應能繼續進行,其原因是______________________。
(3)反應結束后,待冷卻至常溫時,往反應后的混合物中加入稀鹽酸,可觀察到閃亮的火星,產生此現象的原因是副產物Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)氣體,然后SiH4自燃.用化學方程式表示這兩個反應①________________________②___________________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com