
分析 (1)海藻中的碘元素以碘化物形式存在,反應中I元素發生氧化反應,Mn元素被還原,還原產物應為硫酸錳;
(2)當AgCl開始沉淀時,說明溶液中的c(I-)和c(Cl-)均已達到飽和狀態,因此可以根據溶度積表達式進行計算,溶液中 $\frac{c({I}^{-})}{c(C{l}^{-})}$=$\frac{Ksp(AgI)}{Ksp(AgCl)}$;
(3)正反應為吸熱反應,化學鍵斷裂時需吸收的能量-化學鍵生成時需放出的能量=反應吸收的熱量;
(4)依據化學平衡三行計算列式,在457.6℃時,將0.2molH2和0.1mol I2氣態混合物充入10L的密閉容器中,充分反應,達到平衡后,測得HI的體積分數為20%,設反應的氫氣物質的量濃度為x,
H2(g)+I2(g)?2HI(g),
起始量(mol/L) 0.02 0.01 0
變化量(mol/L) x x 2x
平衡量(mol/L)0.02-x 0.01-x 2x
結合碘化氫體積分數計算x,平衡常數等于生成物濃度的冪次方乘積除以反應物平衡濃度的冪次方乘積;
(5)該溫度下0.01mol/L的NaIO溶液中存在水解平衡,IO-+H2O?HIO+OH-,Kh=$\frac{c(O{H}^{-})c(HIO)}{c(I{O}^{-})}$=$\frac{Kw}{Ka}$.
解答 解:(1)海藻中的碘元素以碘化物形式存在,反應中I元素發生氧化反應,Mn元素被還原,還原產物應為硫酸錳,故答案為:MnSO4;
(2)當AgCl開始沉淀時,說明溶液中的c(I-)和c(Cl-)均已達到飽和狀態,因此可以根據溶度積表達式進行計算,溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$=$\frac{Ksp(AgI)}{Ksp(AgCl)}$=$\frac{8.5×1{0}^{-17}}{1.8×1{0}^{-10}}$$\frac{8.5×1{0}^{-17}}{1.7×1{0}^{-10}}$=5.0×10-7,
故答案為:5.0×10-7;
(3)2HI(g)?H2(g)+I2(g)△H=+11kJ•mol-1,設1molHI(g)分子中化學鍵斷裂時需吸收的能量為x kJ,則:2x kJ-436kJ-151kJ=11kJ,解得x=299,
故答案為:299;
(4)設反應的氫氣物質的量濃度為x,
H2(g)+I2(g)?2HI(g),
起始量(mol/L) 0.02 0.01 0
變化量(mol/L) x x 2x
平衡量(mol/L)0.02-x 0.01-x 2x
$\frac{2x}{0.02-x+0.01-x+2x}$×100%=20%
x=0.003mol/L,
平衡常數K=$\frac{{c}^{2}(HI)}{c({I}_{2})c({H}_{2})}$=$\frac{(2×0.003)^{2}}{(0.02-0.003)(0.01-0.003)}$=0.3,
故答案為:0.3;
(5)25℃時HIO的電離常數為2.5×10-9,則該溫度下0.01mol/L的NaIO溶液中存在水解平衡,IO-+H2O?HIO+OH-,Kh=$\frac{c(O{H}^{-})c(HIO)}{c(I{O}^{-})}$=$\frac{c(O{H}^{-})c(HIO)}{c(I{O}^{-})}$×$\frac{c({H}^{+})}{c({H}^{+})}$=$\frac{Kw}{Ka}$=$\frac{1{0}^{-14}}{2.5×1{0}^{-9}}$=4×10-6,c(OH-)=$\sqrt{\frac{4×1{0}^{-6}}{0.01}}$=2×10-4mol/L,c(H+)=$\frac{1{0}^{-14}}{2×1{0}^{-4}}$=5×10-11mol/L,
PH=-lgc(H+)=11-lg5=11-0.7=10.3,故答案為:10.3.
點評 本題比較綜合,涉及考查氧化還原反應、反應熱計算、化學平衡常數計算等,屬于拼合型題目,側重考查學生自學能力、分析解決問題的能力,注意水解平衡和電離平衡的關系計算,題目難度中等.


科目:高中化學 來源: 題型:解答題
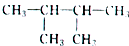 的系統命名為2,3-二甲基丁烷;
的系統命名為2,3-二甲基丁烷;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對水加熱到100℃,測得pH=6 | B. | 在水中滴入稀硫酸 | ||
| C. | 在水中加入小蘇打 | D. | 在水中加入氯化鋁固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應熱就是反應發出的熱量 | |
| B. | 由C(s)+$\frac{1}{2}$O2(g)═CO(g)的反應熱為110.5kJ•mol-1,可知碳的燃燒熱為110.5 kJ•mol-1 | |
| C. | 反應熱的大小與反應物所具有的能量和生成物所具有的能量無關 | |
| D. | 1mol NaOH分別和1mol CH3COOH、1mol HNO3反應放出的熱量:CH3COOH<HNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
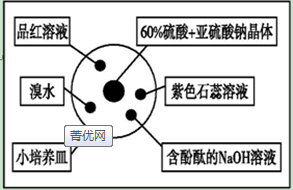
| A. | 品紅溶液褪色 | B. | 溴水橙色褪去 | ||
| C. | 含酚酞的NaOH溶液紅色變淺 | D. | 紫色石蕊溶液先變紅后褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1 NaCl | B. | 0.1mol•L-1 NH4NO3 | ||
| C. | 0.1mol•L-1NaOH | D. | 0.1mol•L-1Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3Cl只代表一種物質 | B. | CH2Cl2只代表一種物質 | ||
| C. | CHCl3只代表一種物質 | D. | CCl4和CH4的結構相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com