
下列離子方程式正確的是
A. 氯氣溶于水:Cl2+H2O 2H++ClO-+Cl-
2H++ClO-+Cl-
B. 亞硫酸鈉溶液被空氣中的氧氣氧化:SO32-+O2=SO42-
C. 氫氧化鐵溶于氫碘酸中:Fe(OH)3+3H+=Fe3++3H2O
D. 碳酸氫銨溶液和足量的氫氧化鈉溶液混合加熱:NH4++HCO3-+2OH-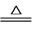 NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
 導學教程高中新課標系列答案
導學教程高中新課標系列答案 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源:2016-2017學年河北省張家口市高一上學期期末考試化學試卷(解析版) 題型:選擇題
將Cl2通入200mL0.5mol·L-1氫氧化鉀溶液中,二者恰好完全反應得到KCl、KClO、KClO3的混合溶液,經測定ClO-與ClO3-的物質的量之比是1︰2,則通入的Cl2在標準狀況下的體積為
A. 0.56L B. 1.68L C. 2.24L D. 1.12L
查看答案和解析>>
科目:高中化學 來源:2017屆山西省名校高三下學期聯考理綜化學試卷(解析版) 題型:簡答題
人口資源環境委員會副主任、中國科學院院士秦大河表示,當前情況下散燒煤和沒有清潔的煤是造成中國城市霧霾或者東部霧霾的主要原因。煤的氣化是解決霧霾,清潔地利用煤炭的重要途徑之一。
⑴已知:H2O(g)=H2O(I) △H=-44kJ/mol
物質 | H2(g) | C(s) | CO(g) |
燃燒熱kJ/mol | -285.8 | -393.5 | -283.0 |
①請寫出煤的氣化反應生成合成氣(CO和H2)的熱化學方程式___________。
②在恒溫、恒容的反應器中,能表明上述反應達到平衡狀態的是_______。
a.混合氣體平均相對分子質量不再改變
b.氣體壓強不再改變
c.各氣體濃度相等
d.反應體系中溫度保持不變
e.斷裂氫氧鍵速率是斷裂氫氫鍵速率的2倍
f.混合氣體密度不變
g.單位時間內,消耗水的質量與生成氫氣的質量比為9:1
⑵在催化劑作用下合成氣合成甲烷過程中會發生如下反應:
I CO(g)+3H2(g) = CH4(g)+H2O(g) △H1= -206 kJ/mol
II CO(g)+H2O(g) = CO2(g)+H2(g) △H2= -41 kJ/mol
Ⅲ 2CO(g)+2H2(g)= CH4(g)+CO2(g) △H 3= -247.4 kJ/mol
①圖1是太原理工大學煤化工研究所利用熱力學數據分析得到溫度對反應ⅠInK(化學平衡常數K的自然對數)的曲線圖,請分析出現這樣趨勢的原因是____________。
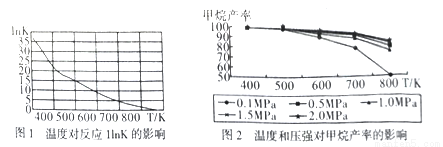
②提高甲烷反應選擇性的關鍵因素是_______,根據相關知識和圖2分析合成甲烷適宜的反應條件是
在550~630K,1MPa的原因是__________________。
③850℃時在體積為5L反應器中發生反應Ⅱ,CO和H2O(g)濃度變化如圖所示,請列式計算此條件下的平衡常數_____________ 。
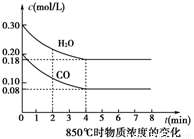
(3)CH4燃料電池利用率很高,裝置中添加1L2mol/L的KOH溶液為電解質,持續緩慢通入標準狀況下甲烷22.4L~33.6 L時負極電極反應為___________。
查看答案和解析>>
科目:高中化學 來源:浙江省臺州市2017屆高三2月選考科目教學質量評估測試化學試卷 題型:選擇題
已知還原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的幾種,為確定其組成,某同學進行如下實驗:
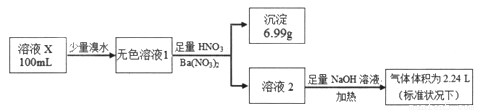
下列說法正確的是
A. 溶液X肯定只存在NH4+、SO42-
B. 溶液X一定不含有Ba2+、Fe3+,可能含有I-
C. 為確定可能存在的陰離子,可另取試液滴加足量鹽酸、BaCl2溶液
D. 為確定可能存在的陽離子,可用經過稀硫酸洗過的鉑絲蘸取溶液X在酒精燈火焰上灼燒
查看答案和解析>>
科目:高中化學 來源:浙江省臺州市2017屆高三2月選考科目教學質量評估測試化學試卷 題型:選擇題
下列說法不正確的是
A. NH4Cl溶液呈酸性說明NH3·H2O是弱電解質
B. 醋酸鈉溶液中c(Na+)>c(CH3COO-)
C. 常溫下相同pH的NaOH溶液和CH3COONa溶液中水電離出的OH-濃度相同
D. 常溫下,在1mol·L-1的鹽酸中加入等體積等濃度的氨水,溶液導電能力減弱
查看答案和解析>>
科目:高中化學 來源:浙江省臺州市2017屆高三2月選考科目教學質量評估測試化學試卷 題型:選擇題
下列有關鐵、銅及其化合物的說法正確的是
A. 鐵和銅在自然界中主要以游離態的形式存在
B. 工業上在高溫下用CO還原含Fe2O3的鐵礦石煉鐵
C. 常溫下鐵與濃硫酸不反應
D. 用激光照射硫酸銅溶液可觀察到丁達爾現象
查看答案和解析>>
科目:高中化學 來源:浙江省臺州市2017屆高三2月選考科目教學質量評估測試化學試卷 題型:選擇題
下列物質屬于堿性氧化物的是
A. SiO2 B. CaO C. CO D. NaOH
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高二下學期基礎訓練(15)化學試卷(解析版) 題型:選擇題
設NA代表阿伏加德羅常數,下列說法正確的是
A. 24g金屬鎂變為鎂離子時失去的電子數為NA
B. 18g水所含的電子數目為NA
C. 在常溫常壓下11.2L二氧化硫所含的分子數目為0.5NA
D. 在常溫常壓下32g氧氣所含的原子數目為2NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省西安市高一上學期期末考試化學試卷(解析版) 題型:選擇題
2FeS + 6H2SO4(濃) = Fe2(SO4)3 + 2 S ↓ + 3SO2 ↑ + 6H2O ,下列說法正確的是( )
A. 反應中氧化產物為Fe2(SO4)3和SO2
B. 氧化劑和還原劑的物質的量之比為3:1
C. 反應中每產生32g沉淀轉移電子的數目為2NA
D. 反應中被Fe還原的硫酸和被S還原的硫酸之比1:2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com