
| X | ||||
| Y | Z | W |
 .
.| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
分析 I.由元素在周期表中位置,可知X處于第二周期,Y、Z、W處于第三周期,Y所處的周期序數與族序數相等,則Y為Al,可推知Z為Si、X為N、W為Cl;
Ⅱ.(3)負極發生氧化反應,Si在負極失去電子,堿性條件下生成SiO32-、H2O;
(4)已知:①C(s)+O2(g)═CO2(g)△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g)△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s)△H=c kJ•mol-1
根據蓋斯定律,①+②-③可得2C(s)+SiO2(s)=Si(s)+2CO(g),反應熱也進行相應的計算;
(5)由表中數據可知,升高溫度,平衡常數減小,說明平衡向逆反應方向移動;
令CO和H2O起始物質的量均為1mol,設平衡時參加反應CO的物質的量為xmol,利用三段式表示出各組分物質的量變化量、平衡時各組分物質的量,反應前后氣體體積不發生變化,用物質的量代替濃度代入平衡常數表達式列方程計算解答.
解答 解:I.由元素在周期表中位置,可知X處于第二周期,Y、Z、W處于第三周期,Y所處的周期序數與族序數相等,則Y為Al,可推知Z為Si、X為N、W為Cl.
(1)N原子結構示意圖為 ,故答案為:
,故答案為: ;
;
(2)說明Cl非金屬性強于Si的方程式為:2HClO4+Na2SiO3=2NaClO4+H2SiO3↓,
故答案為:2HClO4+Na2SiO3=2NaClO4+H2SiO3↓;
Ⅱ.(3)負極發生氧化反應,Si在負極失去電子,堿性條件下生成SiO32-、H2O,負極電極反應式為:Si-4e-+6OH-=SiO32-+3H2O,
故答案為:Si-4e-+6OH-=SiO32-+3H2O;
(4)已知:①C(s)+O2(g)═CO2(g)△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g)△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s)△H=c kJ•mol-1
根據蓋斯定律,①+②-③可得:2C(s)+SiO2(s)=Si(s)+2CO(g)△H=(a+b-c)kJ•mol-1,
故答案為:2C(s)+SiO2(s)=Si(s)+2CO(g)△H=(a+b-c)kJ•mol-1;
(5)由表中數據可知,升高溫度,平衡常數減小,說明平衡向逆反應方向移動,則正反應為放熱反應,即該反應的△H<0;
令CO和H2O起始物質的量均為1mol,設平衡時參加反應CO的物質的量為xmol,則:
CO(g)+H2O(g)?H2(g)+CO2(g)
開始(mol):1 1 0 0
轉化(mol):x x x x
平衡(mol):1-x 1-x x x
反應前后氣體體積不發生變化,可用物質的量代替濃度計算平衡常數,故$\frac{x×x}{(1-x)×(1-x)}$=9,解得x=0.75,故CO平衡轉化率為$\frac{0.75mol}{1mol}$×100%=75%,
故答案為:<;75%.
點評 本題屬于拼合型題目,涉及結構性質位置關系、電極反應式、熱化學方程式、平衡常數影響因素及應用等,難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題

 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將紅熱的銅絲迅速插入乙醇中,可觀察到銅絲表面變紅,并能聞到刺激性氣味 | |
| B. | 乙醇(CH3CH2OH)與二甲醚(CH3-O-CH3)互為同分異構體 | |
| C. | 在蛋白質溶液中加入飽和硫酸銨溶液,會使蛋白質發生變性 | |
| D. | 煤的干餾是化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含大量Fe3+的溶液中:NH4+、Mg2+、Cl-、HSO3- | |
| B. | 加入Al有H2生成的溶液中:Na+、NH4+、Cl-、NO3- | |
| C. | NaOH溶液中:K+、Na+、AlO2-、CO32- | |
| D. | NaHCO3溶液中:K+、Al3+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
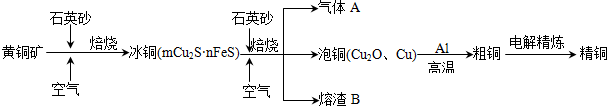
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解時,石墨作陰極,不銹鋼作陽極 | |
| B. | 電解時,陽極反應是:I--6e-+3H2O═IO3-+6H+ | |
| C. | 溶液調節至強酸性,對生產不利 | |
| D. | 電解后陰極周圍溶液的pH升高 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
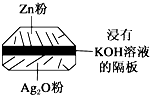 (1)鉛蓄電池是典型的可充型電池,電池總反應式為:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充電}^{放電}$2PbSO4+2H2O.請回答下列問題(不考慮氫、氧的氧化還原):
(1)鉛蓄電池是典型的可充型電池,電池總反應式為:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充電}^{放電}$2PbSO4+2H2O.請回答下列問題(不考慮氫、氧的氧化還原):查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com