
| A. | c(H+)=10-13mol/L的溶液中:NO3-、S2O32-、K+、Na+ | |
| B. | 酸性高錳酸鉀溶液中:Na+、C2O42-、CH3COO -、NH4+ | |
| C. | 澄清石灰水中:HCO3-、Ba2+、Cl-、NO3- | |
| D. | 空氣中:SO2、NO、N2、NH3 |
分析 A.c(H+)=10-13mol/L的溶液為堿性溶液,四種離子之間不反應,都不與氫氧根離子反應;
B.酸性高錳酸鉀溶液能夠氧化草酸根離子、醋酸根離子;
C.碳酸氫根離子與氫氧化鈣反應;
D.NO與空氣中氧氣反應生成二氧化氮.
解答 解:A.c(H+)=10-13mol/L的溶液中存在大量氫氧根離子,NO3-、S2O32-、K+、Na+之間不反應,都不與氫氧根離子反應,在溶液中能夠大量共存,故A正確;
B.酸性高錳酸鉀溶液具有強氧化性,能夠氧化C2O42-、CH3COO-,在溶液中不能大量共存,故B錯誤;
C.澄清石灰水中含有氫氧化鈣,HCO3-與氫氧化鈣反應,在溶液中不能大量共存,故C錯誤;
D.NO與氧氣反應,在空氣中不能大量共存,故D錯誤;
故選A.
點評 本題考查離子共存的判斷,為高考的高頻題,屬于中等難度的試題,注意明確離子不能大量共存的一般情況,如:能發生復分解反應的離子之間;能發生氧化還原反應的離子之間等;還應該注意題目所隱含的條件,如:溶液的酸堿性,據此來判斷溶液中是否有大量的 H+或OH-;溶液的顏色,如無色時可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色離子的存在;溶液的具體反應條件,如“氧化還原反應”、“加入鋁粉產生氫氣”;是“可能”共存,還是“一定”共存等.


科目:高中化學 來源: 題型:選擇題
| A. | Mg2+、Cl-、Na+、NO3- | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Na+、Cl-、AlO2-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學是在原子、分子水平上研究物質的組成、結構、性質、制備等的自然科學 | |
| B. | 化學是一門具有創造性的科學,可以利用化學知識創造出自然界中不存在的物質 | |
| C. | 化學的發展經過了從宏觀到微觀,從感性到理性的逐步深化的過程 | |
| D. | 隨著化學的發展,人們最終會實現通過化學變化使水變油的夢想 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
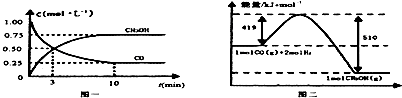
| 容器 | 反應物投入的量 | 反應物的 轉化率 | CH3OH的濃度 | 能量變化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ熱量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ熱量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
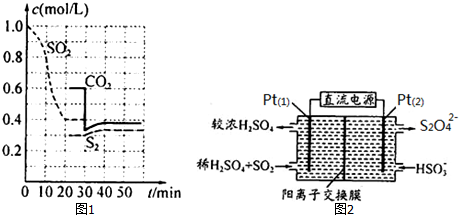
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | △H>0表示放熱反應,△H<0表示吸熱反應 | |
| B. | 熱化學方程式中的化學計量數只表示物質的量,可以是分數也可以是小數 | |
| C. | 1molH2SO4和1mo Ba(OH)2反應生成BaSO4沉淀時放出的熱叫做中和熱 | |
| D. | 1molH2和0.5mol O2反應放出的熱就是H2的燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 治療胃酸過多,可用NaHCO3,不能用Al(OH)3,因其含有Al元素 | |
| B. | Al箔用砂紙打磨后,在空氣中受熱可以熔化,由于氧化膜被破壞,熔化的Al可以滴落 | |
| C. | 用鉑絲做焰色反應實驗,每次做完后都需要用鹽酸洗滌,再灼燒至跟酒精燈火焰顏色相同后再使用 | |
| D. | 實驗室制備Al(OH)3時,氨水不宜過量,因為Al(OH)3與過量的濃氨水反應生成NH4AlO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol固態焦炭與1mol水蒸氣反應產生1mol一氧化碳和1mol氫氣,吸收131.3 kJ的熱量 | |
| B. | 碳與水反應吸收131.3 kJ的熱量 | |
| C. | 1mol碳和1mol水反應吸收131.3 kJ的熱量 | |
| D. | 固態碳和氣態水各1mol反應,放出131.3 kJ的熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com