
【題目】(1)在現用周期表中氧族元素包括 ______________________(填元素名稱)五種元素,其中Se的基態原子的電子排布式為______________________,元素X與Se同周期,X元素原子核外未成對電子數最多,X為______________________(填元素符號)。
(2)與氧同周期的相鄰元素中,第一電離能有大到小的順序______________________。
(3)臭鼬排放的臭氣主要成分為3—MBT(3—甲基—2—丁烯硫醇,結構如圖)。1mol3—MBT中含有σ鍵數目為____________(NA為阿佛加德羅常數的值)。沸點:3—MBT____________(CH3)2C==CHCH2OH(填“>”“<”或“=”),主要原因是________________________。

(4)S有+4和+6兩種價態的氧化物。
①下列關于氣態SO3和SO2的說法正確的是__________(填序號)。
A.中心原子的價層電子對數不相等
B.都是極性分子
C.中心原子的核對電子數目不相等
D.都含有極性鍵
②SO3分子的空間構型為__________,與其互為等電子體的陰離子為__________(舉一例)。
(5)單質Po是有__________鍵形成的晶體;若已知Po的摩爾質量為Mg·mol-1,原子半徑為rpm,阿伏加德羅常數的值為NA,則釙晶體的密度的表達式為____________________g·cm-3。
【答案】氧、硫、硒、碲、釙 1s22s22p63s23p63d104s24p4 Cr F>N>O 15NA < (CH3)2C=CHCH2OH分子間存在氫鍵,使沸點增高 CD 平面三角形 NO3-或CO32- 金屬 ![]()
【解析】
根據原子的核外電子排布規律分析解答;根據元素周期表、元素周期律分析解答;根據價層電子對互斥理論分析解答。
(1)氧族元素即第VIA族元素,其中包括氧、硫、硒、碲、釙五種元素,其中Se是位于第四周期VIA族,Se的基態原子的電子排布式為1s22s22p63s23p63d104s24p4或[Ar]3d104s24p4,元素X與Se同周期,X元素原子核外未成對電子數最多,則X的d軌道和4s軌道呈半滿狀態時,原子核外未成對電子數最多,所以X為Cr;
故答案為:氧、硫、硒、碲、釙,1s22s22p63s23p63d104s24p4,Cr;
(2)與氧同周期的相鄰元素中有N元素和F元素,由于N原子2p軌道呈半滿狀態,較穩定,則N的第一電離能大于O原子的第一電離能,所以F、O、N的第一電離能由大到小的順序F>N>O;
故答案為:F>N>O;
(3)有圖片可知,一分子3—MBT(3—甲基—2—丁烯硫醇)含有9個C—H鍵,4個C—Cσ鍵,一個C—S鍵,一個S—H鍵,所以1mol3—MBT中含有σ鍵數目為15NA,由于(CH3)2C=CHCH2OH分子間存在氫鍵,使沸點增高沸點,所以(CH3)2C=CHCH2OH的沸點高于3—MBT;
故答案為:5NA,<,(CH3)2C=CHCH2OH分子間存在氫鍵,使沸點增高;
(4)①根據分析可知,二者中心原子的價層電子對數目相等,都是3對,故A正確;二氧化硫是極性分子,而三氧化硫為平面三角形,結構對稱,為非極性分子,故B錯誤;中心原子的孤對電子數目不等,二氧化硫分子中含有1對,三氧化硫不存在孤對電子,故C正確;二氧化硫和三氧化硫都含有S與O之間的極性鍵,故D正確;
故答案為:CD;
②SO3中心原子S原子價電子對數為3,即SO3為sp2雜化,所以SO3的空間構型為平面三角形,價電子數和原子數分別相等的是等電子體,則與SO3互為等電子體的離子為NO3-,CO32-;
故答案為:平面三角形,NO3-、CO32-;
(5)單質釙是由金屬鍵形成的晶體,屬于簡單立方堆積,一個晶胞中含有1個原子,當原子半徑為rpm時,晶胞邊長為2rpm,則釙晶體的密度ρ=![]() =
=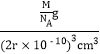 =
=![]() ,
,
故答案為:![]() 。
。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】現有下列十種物質:①蔗糖 ②熔融NaCl ③石墨 ④銅絲 ⑤NaOH固體 ⑥SO2 ⑦NaHSO4固體 ⑧K2O固體 ⑨液態H2SO4 ⑩飽和FeCl3溶液
(1)上述物質中可導電的是_____(填序號,下同);
(2)上述物質中不能導電,但屬于電解質的是_____。
(3)⑦在水溶液中的電離方程式為__________________________________。
(4)實驗室制備少量Fe(OH)3膠體所用的物質有______(填序號)和蒸餾水,反應的離子方程式為_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組向一定量的NaHSO3溶液(加入少量淀粉)中加入稍過量的KIO3 溶液,一段時![]() 間后,溶液突然變藍色。為進一步研究有關因素對反應速率的影響,探究如下。
間后,溶液突然變藍色。為進一步研究有關因素對反應速率的影響,探究如下。
(1)查閱資料 知NaHSO3與過量KIO3反應分為兩步進行,且其反應速率主要由第一步反應決定。已知第一步反應的離子方程式為IO3—+3HSO3—===3SO42—+I—+3H+,則第二步反應的離子方程式為________________。
(2)通過測定溶液變藍所用時間來探究外界條件對該反應速率的影響,記錄如下。
編號 | 0.01mol/LNaHSO3溶液/mL | 0.01mol/L KIO3 溶液/mL | H2O/mL | 反應溫度 /℃ | 溶液變藍所用時間t/s |
① | 6.0 | 10.0 | 4.0 | 15 | t1 |
② | 6.0 | 14.0 | 0 | 15 | t2 |
③ | 6.0 | a | b | 25 | t3 |
實驗①②是探究_______________對反應速率的影響,表中t1___________t2(填“>”、“=”或“<”);
實驗①③是探究溫度對反應速率的影響,表中a=_____________,b=_____________。、
(3)將NaHSO3溶液與KIO3溶液在恒溫條件下混合,用速率檢測儀檢測出起始階段反應速率 逐漸增大。該小組對其原因提出如下假設,請你完成假設二。
假設一:生成的SO42—對反應起催化作用;
假設二:___________________________;……
(4)請你設計實驗驗證上述假設一,完成下表中內容。
實驗步驟(不要求寫出具體操作過程) | 預期實驗現象和結論 |
在燒杯甲中將一定量的NaHSO3溶液與KIO3溶液混合,用速率檢測儀測定起始時的反應速率v(甲) 在燒杯乙中先加入少量①_____,其他條件與甲完全相同,用速率檢測儀測定起始時的反應速率v(乙) | ②若v(甲)___v(乙),則假設一不成立 ③若v(甲)___v(乙),則假設一成立 (填“>”、“=”或“<”) |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積為1L的密閉容器中充入2mol A和1![]() B,發生如下反應:
B,發生如下反應:![]() ,5min后反應達到平衡,這時C的濃度為1.2
,5min后反應達到平衡,這時C的濃度為1.2![]() ,請回答:
,請回答:
(1)5min內A消耗速率![]() ________________________________;
________________________________;
(2)能判斷該反應達到化學平衡狀態的依據是__________________;
A.混合氣體的壓強保持不變 B.單位時間內生成2molA的同時生成1mol B
C.混合氣體的密度保持不變 D.A、B、C的物質的量之比為![]()
(3)該反應的平衡常數表達為K=_______________________,該溫度下反應的平衡常數是_________;
(4)B在此條件下的轉化率為___________________;
(5)升高溫度,混合氣體的平均相對摩爾質量減小,則正反應為________(填“吸熱”或“放熱”)反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化鈉是家庭日常生活中必不可少的一種調味品,海水制鹽是氯化鈉來源的一種途徑。海水曬鹽工業流程中,得到的粗鹽常含有Mg2+、Ca2+、SO42-等雜質工業提純粗鹽的流程如圖所示:

(1)步驟④操作中需要用到玻璃棒,玻璃棒的作用是____________;步驟⑥中操作b實驗室用到的可直接加熱的儀器名稱叫____________。
(2)如果按以上操作步驟及順序進行了,則制得的精鹽不純。要獲得純凈的精鹽,還需添加的試劑是(填化學式)____________;該步驟作應該放在(填序號)____________之前。
(3)室溫下,電解1mol/L500mL的NaCl溶液,當溶液的pH=13時停止電解;寫出該電解過程的離子方程式(忽略溶液體積變化,惰性電極):________________________________________________________;
要使電解后的溶液恢復到原濃度,需加入(通入)____________mol____________(填物質名稱)。
(4)用氯堿工業的產物氫氧化鈉配制成0.1mol/L的標準溶液,滴定20mL未知濃度的鹽酸溶液,需用作____指示劑,判定要達到滴定終點的現象:_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴A是有機化學工業的基本原料,其產量可以用來衡量一個國家的石油化工發展水平,A還是一種植物生長調節劑,A可發生如圖所示的一系列化學反應,其中①②③屬于同種反應類型。

回答下列問題:
(1)寫出A、B、C、D的結構簡式:
A ____________,B____________C___________,D_____________。
(2)寫出①②兩步的化學方程式,并注明反應類型:
①__________________________________(反應類型________________)。
②_________________________________(反應類型________________)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】D、E、X、Y、Z是周期表中的前20號元素,且原子序號逐漸增大,它們的最簡單氫化物分子的空間結構依次是正四面體、三角錐形、直線形、折線形、直線形,回答下列問題:
(1)E的氫化物的電子式為_____,D的氫化物分子中鍵角為_____,Y的氫化物的結構式為_____,X的氫化物沸點_____Z的氫化物沸點(填“高于”或“低于”)。
(2)D和Y形成的化合物,其分子的電子式為_____,空間構型為_____形,為_____(填“極性”或“非極性”)分子。
(3)取上述五種氫化物中的兩種化合,能生成一種含有離子鍵、共價鍵和配位鍵的化合物,試寫出其中的任意一種的化學式_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 常溫常壓下,22.4L的37Cl2中所含的中子數為20NA
B. 標準狀況下,8.0g甲烷所含C一H鍵數目為2.0NA
C. 若將1mol氯化鐵完全轉化為氫氧化鐵膠體,則分散系中膠體微粒數為NA
D. 一定條件下,0.1molN2與足量H2充分反應,生成NH3分子數為0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有短周期A,B,C三種元素,原子序數依次增大,A元素的單質是密度最小的氣體,B獲得2個電子可達到穩定結構,C與A同主族。
(1)判斷A,B,C各為何種元素。A____,B____,C____。
(2)用電子式表示三種元素原子之間可能構成的化合物的形成過程,若含共價鍵請指出共價鍵是σ鍵還是π鍵,并標明該鍵的個數。
①A與B:___________________________________________________。
②A與C:___________________________________________________。
③B與C:___________________________________________________。
④A,B,C:___________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com