
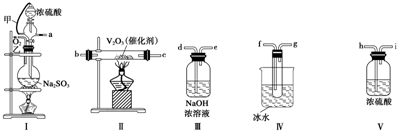
分析 (1)因從溶液中反應生成氣體中混有水蒸氣,所以產生的氣體首先經過干燥裝置Ⅲ,然后再進行二氧化硫氣體的催化氧化即經過裝置Ⅱ,然后是收集S03,S03的熔點是16.8℃,沸點是44.8℃,所以選擇裝置Ⅳ進行冷卻,使三氧化硫與二氧化硫分離,最后在Ⅴ中吸收未反應的SO2,依據各裝置作用排序:裝置Ⅰ為氣體發生裝置,裝置Ⅱ為二氧化硫催化氧化裝置,裝置Ⅲ為尾氣吸收裝置,裝置Ⅳ為收集裝置,裝置Ⅴ干燥裝置;
(2)反應在加熱條件下進行,為保證充分反應,應先加熱;
(3)Ⅱ中發生反應二氧化硫的催化氧化生成三氧化硫;
(4)大火加熱,生成二氧化硫較快,不能充分反應;生成三氧化硫,經冷卻可得到晶體;
(5)二氧化硫的轉化率=$\frac{二氧化硫變化量}{二氧化硫起始量}$×100%,根據硫元素守恒結合三氧化硫的量確定二氧化硫的變化量.
解答 解:(1)因從溶液中反應生成氣體中混有水蒸氣,所以產生的氣體首先經過干燥裝置Ⅲ,然后再進行二氧化硫氣體的催化氧化即經過裝置Ⅱ,然后是收集S03,S03的熔點是16.8℃,沸點是44.8℃,所以選擇裝置Ⅳ進行冷卻,使三氧化硫與二氧化硫分離,最后在Ⅴ中吸收未反應的SO2,要制備二氧化硫并檢驗二氧化硫的性質、收集二氧化硫,依次用到的裝置為:Ⅰ氣體發生裝置,Ⅴ干燥裝置,Ⅱ為二氧化硫催化氧化裝置,Ⅳ收集裝置,Ⅲ尾氣吸收裝置,所以正確的順序為:a h i b c f g d;
故答案為:a h i b c f g d;
(2)為保證產生的二氧化硫盡可能多的轉化為三氧化硫,應先加熱V2O5,后緩緩滴入濃硫酸,
故答案為:先加熱V2O5,后緩緩滴入濃硫酸;
(3)Ⅱ中發生反應的化學方程式:2SO2+O2 $\frac{\underline{催化劑}}{△}$2SO3,故答案為:2SO2+O2 $\frac{\underline{催化劑}}{△}$2SO3;
(4)大火加熱,生成二氧化硫較快,不能充分反應,則轉化率減小,裝置IV處是用來冷卻三氧化硫氣體,使之變成液態或固態,從而收集得到三氧化硫,所以可以在Ⅳ處看到有無色(或白色)晶體(或固體)生成,
故答案為:減小;有無色(或白色)晶體(或固體)生成;
(5)n mol Na2SO3粉末與足量濃硫酸反應生成nmol二氧化硫,當反應結束時,Ⅲ處增重的部分為未反應的二氧化硫,則轉化了的二氧化硫的質量為:64n-m,所以實驗中SO2的轉化率=$\frac{64n-m}{64n}$×100%,
故答案為:$\frac{64n-m}{64n}$×100%.
點評 本題考查物質的性質探究以及轉化率的測定,把握實驗的原理、物質的性質是解題關鍵,側重于學生的分析能力和實驗能力的考查,題目難度中等.


 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 煤的干餾是化學變化 | |
| B. | 煤液化后可以得到甲醇等液體燃料 | |
| C. | 煤中含有苯和甲苯,可以用蒸餾的方法把它們分離出來 | |
| D. | 從萃取分液后溴的四氯化碳溶液中提取溴可以用蒸餾的方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
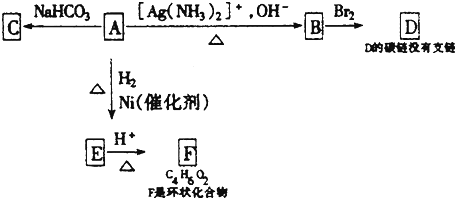
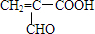 .
.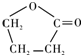 .由E生成F的反應類型是酯化反應.
.由E生成F的反應類型是酯化反應.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳的結構式:O-C-O | B. | 過氧化鈉的電子式: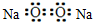 | ||
| C. | 丙烷分子的球棍模型: | D. | Cl-的結構示意圖: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C5H12屬于烷烴且有2種同分異構體 | |
| B. | 乙烯、氯乙烯、甲苯分子中的所有原子均共平面 | |
| C. | C4H10與Cl2在光照條件下反應,可生成4種一氯代烴 | |
| D. | 苯分子中不含碳碳雙鍵,所以不能發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
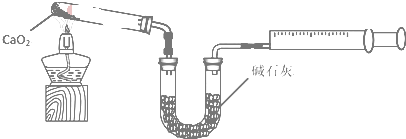
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18gH2O含有的氫原子數目為NA | |
| B. | 標準狀況下,22.4LCO2含有的分子數目為NA | |
| C. | 1L1mol•L-1K2SO4溶液中含有的鉀離子數目為NA | |
| D. | 1molH2在O2中完全燃燒轉移的電子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
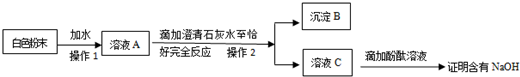
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com