

分析 高溫反應后,石墨中氧化物雜質均轉變為相應的氯化物,根據雜質的含量可知,氣體I中氯化物主要為SiCl4、AlCl3、FeCl3等,氣體I中碳氧化物主要為CO,SiCl4的沸點為57.6℃,金屬氯化物的沸點均高于150℃,80℃冷卻得到的氣體Ⅱ含有SiCl4及CO,SiCl4與氫氧化鈉溶液反應得到硅酸鈉與氯化鈉,固體Ⅲ存在AlCl3、FeCl3、MgCl2,其中FeCl3、MgCl2與過量的氫氧化鈉溶液反應得到沉淀,而氯化鋁與過量的氫氧化鈉溶液反應生成偏鋁酸鈉,過濾得到的溶液中含有偏鋁酸鈉、過量的氫氧化鈉,在溶液中加入乙酸乙酯,加熱,乙酸乙酯發生水解,消耗了氫氧化鈉,溶液堿性減弱,促進了偏鋁根水解,生成氫氧化鋁沉淀,據此分析解答.
解答 解:(1)石墨化學性質在常溫下穩定,而在高溫下可與氧氣發生反應,所以通入氮氣排盡裝置中的空氣,防止石墨發生氧化反應,減少石墨損失,
故答案為:排除裝置中的空氣;
(2)石墨過量高溫反應后,石墨中氧化物雜質均轉變為相應的氯化物,根據雜質的含量可知,氣體I中氯化物主要為SiCl4、AlCl3、FeCl3等,氣體I中碳氧化物主要為CO,SiCl4的沸點為57.6℃,金屬氯化物的沸點均高于150℃,80℃冷卻得到的氣體Ⅱ含有SiCl4及CO,SiCl4與氫氧化鈉溶液反應得到硅酸鈉與氯化鈉,化學反應方程式為:SiCl4+6NaOH=Na2SiO3+4NaCl+3H2O;
故答案為:CO;SiCl4+6NaOH═Na2SiO3+4NaCl+3H2O.
點評 本題考查混合物分離提純的綜合應用,為高頻考點,題目難度中等,把握物質的性質、流程中的反應及混合物分離方法為解答的關鍵,側重分析與實驗能力的考查.


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:選擇題
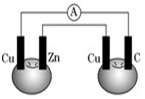 重慶市璧山中學校在化學興趣活動中,曾老師利用番茄做成電池(如圖所示),銅片和鋅片用導線連接后插入番茄里,則碳是( )
重慶市璧山中學校在化學興趣活動中,曾老師利用番茄做成電池(如圖所示),銅片和鋅片用導線連接后插入番茄里,則碳是( )| A. | 陽極 | B. | 正極 | C. | 陰極 | D. | 負極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,S2和S8的固體混合物共6.4g,其中所含硫原子數一定為0.2NA | |
| B. | 將1molFeCl3滴入足量沸水中,所分散系中粒子數目小于NA | |
| C. | 6.4g銅與硫反應時,銅失去的電子數為0.2NA | |
| D. | 標準狀況下,44.8L NO與22.4L O2混合后氣體中分子總數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SO4既不是氧化劑又不是還原劑 | |
| B. | 1molKClO3參加反應時有5mol電子轉移 | |
| C. | KClO3是氧化劑 | |
| D. | 被氧化與被還原的氯元素的質量比為1:5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
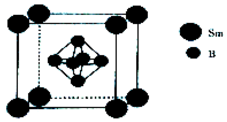 硼及其化合物在工農業生產中應用廣泛.
硼及其化合物在工農業生產中應用廣泛.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 化學性質 | 實際應用 |
| A | Na、K均是活潑金屬 | 鈉鉀合金用作原子反應堆導熱劑 |
| B | H2O2能使蛋白質變性 | 醫療上用于傷口消毒 |
| C | CH2=CH2能與H2O發生加成反應 | 乙烯用作果實的催熟劑 |
| D | NH3具有還原性 | 作食品加工的制冷劑 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com