
【題目】實驗室配制500mL 0.2mol/L的NaOH溶液。
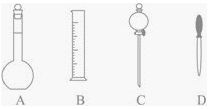
(1)在下圖所示儀器中,配制上述溶液肯定不需要的是_____________(填序號),除圖中已有儀器外,配制上述溶液還需要的玻璃儀器是__________、____________。
(2)填寫下述過程中的空白;
具體步驟如下:
①計算需要稱量NaOH固體的質量___________g;
②用托盤天平稱量NaOH固體;
③將稱好的NaOH固體放入燒杯中,加適量蒸餾水溶解、攪拌,并_________至室溫;
④將NaOH溶液沿玻璃棒注入____________中;
⑤用少量蒸餾水洗滌燒杯內壁2~3次,洗滌液也都注入容量瓶,輕輕晃動容量瓶,使溶液混合均勻;
⑥將蒸餾水注入容量瓶,液面離刻度線下_______cm時,改用____________滴加蒸餾水至液面于刻度線相切;
⑦蓋好瓶塞,反復上下顛倒,搖勻;
(3)經精確測量,最后所得溶液物質的量濃度為0.192mol/L,原因可能是_____________
A.使用濾紙稱量NaOH固體;
B.溶解NaOH后的燒杯未經多次洗滌;
C.容量瓶中原來有少量蒸餾水;
D.稱量時所用的砝碼生銹;
E.未冷卻直接轉移至容量瓶,立即配好。
【答案】C 燒杯 玻璃棒 4.0 冷卻 500mL容量瓶 1~2 膠頭滴管 AB
【解析】
(1)根據(jù)實驗操作的步驟(計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻等操作)以及每步操作需要儀器確定反應所需儀器;
(2)依據(jù)m=c·V·M計算需要溶質的質量;依據(jù)配制一定物質的量濃度溶液的一般步驟確定使用的儀器及方法、要求;
(3)分析操作對溶質的物質的量和溶液體積的影響,依據(jù)c=![]() 進行誤差分析。
進行誤差分析。
(1)配制一定體積一定物質的量濃度的溶液要在一定規(guī)格是容量瓶中進行,先用天平稱量物質,用量筒量取水,在燒杯中進行溶解,為促進物質溶解,要用玻璃棒攪拌,待溶液恢復至室溫后通過玻璃棒引流轉移至在容量瓶中,最后用膠頭滴管定容。故在如圖所示儀器中,配制上述溶液肯定不需要的是分液漏斗,序號是C;還需要使用的玻璃儀器有燒杯、玻璃棒;
(2)①配制500mL 0.2mol/LNaOH溶液需要氫氧化鈉的質量為:m(NaOH)= 0.2mol/L×0.5L ×40g/mol=4.0g;
②用托盤天平稱量NaOH固體;
③由于容量瓶要求配制的溶液的溫度是室溫,所以要將稱好的NaOH固體放入燒杯中,加適量蒸餾水溶解、攪拌,并冷卻至室溫;
④將NaOH溶液沿玻璃棒注入500mL容量瓶中;
⑤用少量蒸餾水洗滌燒杯內壁2~3次,洗滌液也都注入容量瓶,輕輕晃動容量瓶,使溶液混合均勻;
⑥將蒸餾水注入容量瓶,液面離刻度線下1~2cm時,改用膠頭滴管滴加蒸餾水至液面于刻度線相切;
⑦蓋好瓶塞,反復上下顛倒,搖勻,就得到500mL 0.2mol/LNaOH溶液。
(3)經精確測量,最后所得溶液物質的量濃度為0.192mol/L,小于0.2mol/L,
A.使用濾紙稱量NaOH固體,部分溶質由于NaOH潮解沾在濾紙上,導致溶質的質量偏少,稱取溶質中氫氧化鈉物質的量也就偏小,使所配溶液的濃度偏低,A符合題意;
B.溶解NaOH后的燒杯未經多次洗滌,導致溶質的質量減少,使所配溶液的濃度偏低,B符合題意;
C.容量瓶中原來有少量蒸餾水,不影響溶質的質量和溶液的體積,因此對配制的溶液濃度無影響,C不符合題意;
D.稱量時所用的砝碼生銹,使溶質的質量偏大,最后導致配制的溶液濃度偏高,D不符合題意;
E.未冷卻直接轉移至容量瓶,立即配好,待溶液恢復至室溫時,溶液的體積偏小,導致配制的溶液濃度偏高,E不符合題意;
故合理選項是AB。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】某一化工廠以廢鐵屑為原料制備FeCl3溶液,用作印刷電路銅板腐蝕劑,并對溶液B進行電解處理的實驗流程如圖:
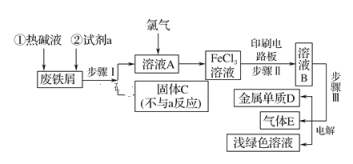
(1)熱堿液的作用_____________;
(2)試劑a應選用________(填寫名稱);
(3)步驟Ⅰ用到的主要玻璃儀器有漏斗、_____(填寫儀器名稱);
(4)寫出步驟Ⅱ中主要反應的化學方程式______;
(5)實驗室制取氣體E的離子方程式是____,欲對氣體E進行干燥和吸收,需選用下列裝置中的____(填寫序號);
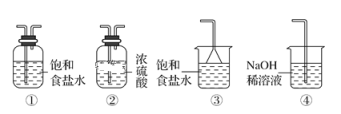
(6)如何用化學方法檢驗氣體E?_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一包固體粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三種物質組成,取樣品進行如圖實驗,從實驗可以判斷:( )

A.該固體粉末中一定不含有BaCl2
B.該固體粉末中一定含有KNO3
C.它的組成可能是CaCO3、BaCl2、Na2SO4
D.它的組成一定是CaCO3、Na2SO4、KNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,不屬于四大基本反應類型,但屬于氧化還原反應的是
A. 2Na+2H2O===2NaOH+H2↑
B. Cl2+H2O===HCl+HClO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. Ca(ClO)2+2HCl===CaCl2+2HClO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組以黃銅礦(主要成分CuFeS2)為原料進行如下實驗探究.為測定黃銅礦中硫元素的質量分數(shù),將m1g該黃銅礦樣品放入如圖所示裝置中,從a處不斷地緩緩通入空氣,高溫灼燒石英管中的黃銅礦樣品.

(1)錐形瓶A內所盛試劑是__________;裝置B的作用是__________;錐形瓶D內發(fā)生反應的離子方程式為__________。
(2)反應結束后將錐形瓶D中的溶液進行如下處理:

如圖則向錐形瓶D中加入過量H2O2溶液反應的離子方程式為__________;操作Ⅱ是洗滌、烘干、稱重,其中洗滌的具體方法__________;該黃銅礦中硫元素的質量分數(shù)為__________(用含m1、m2的代數(shù)式表示).
(3)反應后固體經熔煉、煅燒后得到泡銅(Cu、Cu2O)和熔渣(Fe2O3、FeO),要驗證熔渣中存在FeO,應選用的最佳試劑是__________
A.KSCN溶液、氯水B.稀鹽酸、KMnO4溶液
C.稀硫酸、KMnO4溶液D.NaOH溶液
(4)已知:Cu+在強酸性環(huán)境中會發(fā)生反應生成Cu和Cu2+.設計實驗方案驗證泡銅中是否含有Cu2O__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生欲配制6.0mol/L的H2SO4 1000 mL,實驗室有三種不同濃度的硫酸:
①480mL 0.5mol/L 的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。有三種規(guī)格的容量瓶:250mL、500mL、1000mL。老師要求把①②兩種硫酸全部用完,不足的部分由③來補充。
請回答下列問題:
(1)實驗所用25%的硫酸的物質的量濃度為______mol/L(保留1位小數(shù))。
(2)配制該硫酸溶液應選用容量瓶的規(guī)格為______mL。
(3)配制時,該同學的操作順序如下,請將操作步驟B、D補充完整。
A.將①②兩溶液全部在燒杯中混合均勻;
B.用量筒準確量取所需的18mol/L的濃硫酸____mL,沿玻璃棒倒入上述混合液中。并用玻璃棒攪拌,使其混合均勻;
C.將混合均勻的硫酸沿玻璃棒注入所選的容量瓶中;
D._________________________________________________________________________________________________________________________________
E.振蕩,繼續(xù)向容量瓶中加水,直到液面接近刻度線1~2cm處;
F.改用膠頭滴管加水,使溶液的凹液面恰好與刻度線相切;
G.將容量瓶蓋緊,振蕩,搖勻。
(4)如果省略操作D,對所配溶液濃度有何影響?________(填“偏大”、“偏小”或“無影響”)。
(5)進行操作C前還需注意____________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)根據(jù)有機化合物分子中所含官能團,可對其進行分類和性質預測。
①下列有機化合物屬于醇類物質的是____(填字母)。
a.CH3CH2OH b.CH3CHO c.![]()
②下列有機化合物中加入濃溴水能生成白色沉淀的是____(填字母)。
a.CH2=CH2 b.苯 c.![]()
③下列有機化合物能發(fā)生水解反應的是____(填字母)。
a.乙酸 b.油脂 c.葡萄糖
(2)有機物W(![]() )廣泛存在于肉桂類植物的果肉中。
)廣泛存在于肉桂類植物的果肉中。
①W分子中所含官能團的名稱為____和____。
②W分子中處于同一平面的碳原子最多有____個。
③1mol W分子最多能與____mol H2發(fā)生加成反應。
(3)對羥基苯甲酸乙酯( )是常用的食品防腐劑,可通過以下方法合成:
)是常用的食品防腐劑,可通過以下方法合成:
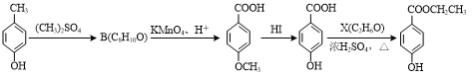
A C D E
①C→D的反應類型為____。
②B的結構簡式為____。
③D與碳酸氫鈉反應后所得有機物的結構簡式為____。
④D→E反應的化學方程式為____。
⑤寫出同時滿足下列條件的C的一種同分異構體的結構簡式:____。
Ⅰ.能和FeCl3溶液發(fā)生顯色反應;
Ⅱ.能發(fā)生銀鏡反應,不能發(fā)生水解反應;
Ⅲ.分子中含有4種不同化學環(huán)境的氫原子。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組設計實驗制備乙酸乙酯(如圖1):
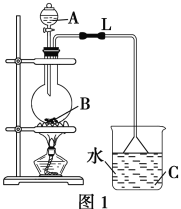
(1)實驗過程中,用酒精燈緩慢加熱,“緩慢加熱”目的是______________________。
(2)燒瓶B中加幾塊碎瓷片,其作用是__________。長導管L的作用是________________。
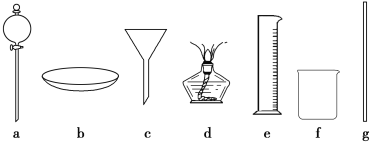
(3)圖1方案有明顯缺陷,請?zhí)岢龈倪M建議:_____________________________________。經改進后,實驗現(xiàn)象是____________________________________________________。簡述分離乙酸乙酯的操作方法:________________,需要用到的下列儀器有________(填代號)。
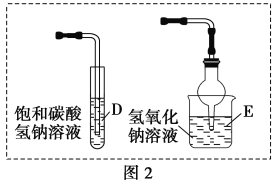
(4)①能否用圖2的D裝置替代圖1的C裝置?________(填“能”或“否”),理由是__________________________;
②能否用圖2的E裝置替代圖1的C裝置?________(填“能”或“否”),理由是___________________。
(5)實驗中,若濃硫酸量過多,會導致后果是______________________________________(答兩點即可)。經實驗證明,可以用硫酸氫鈉固體替代濃硫酸完成本實驗,硫酸氫鈉不溶于有機物,其優(yōu)點是____________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.6×10-39。常溫下,某酸性CuCl2溶液中含有少量的FeCl3,為了得到純凈的CuCl2·2H2O晶體,應加入___________(填氧化物的化學式),調節(jié)溶液的pH=4,使溶液中的Fe3+轉化為Fe(OH)3沉淀,此時溶液中的c(Fe3+)=________。過濾后,將所得濾液低溫蒸發(fā)、濃縮結晶,可得到CuCl2·2H2O晶體。
(2)某碳素鋼鍋爐內水垢的主要成分是碳酸鈣、硫酸鈣、氫氧化鎂、鐵銹、二氧化硅等。水垢需及時清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加熱,浸泡數(shù)小時;
Ⅱ.放出洗滌廢液,清水沖洗鍋爐,加入稀鹽酸和少量NaF溶液,浸泡;
Ⅲ.向洗滌液中加入Na2SO3溶液;
Ⅳ.清洗達標,用NaNO2溶液鈍化鍋爐。
①用稀鹽酸溶解碳酸鈣的離子方程式是_____________________________。
②已知:25 ℃時有關物質的溶度積
物質 | CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
Ksp | 2.8×10-9 | 9.1×10-6 | 1.8×10-11 | 6.8×10-6 |
根據(jù)數(shù)據(jù),結合化學平衡原理解釋清洗CaSO4的過程________________。(用溶解平衡表達式和必要的文字敘述加以說明);在步驟Ⅰ浸泡過程中還會發(fā)生反應MgCO3(s)+2OH-(aq)![]() Mg(OH)2(s)+CO32-(aq),該反應的平衡常數(shù)K=________(保留兩位有效數(shù)字)。
Mg(OH)2(s)+CO32-(aq),該反應的平衡常數(shù)K=________(保留兩位有效數(shù)字)。
③步驟Ⅲ中,加入Na2SO3溶液的目的是_______________________________。
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com