
【題目】向某NaOH溶液中通入CO2氣體后得到溶液M,因CO2通入的量不同,溶液M的組成也不同,若向M中逐滴加入鹽酸,產生的氣體體積V(CO2)與加入鹽酸的體積V(HCl)的關系如下圖所示。則下列分析與判斷正確的是(不計CO2的溶解)
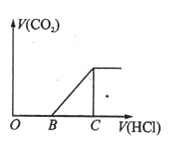
A.若OB=0,則溶液M為Na2CO3溶液
B.若OB=BC,則形成溶液M所發生的離子反應方程式為:OH-+CO2=HCO3-
C.若3OB=BC,則溶液M中c(NaHCO3)=2c(Na2CO3)
D.若OB>BC,則溶液M中大量存在的陰離子為CO32-和HCO3-
【答案】C
【解析】
試題分析:向Na2CO3溶液中逐滴加入鹽酸,反應原理為:Na2CO3 + HCl = NaCl + NaHCO3,NaHCO3 + HCl = NaCl + CO2↑ + H2O。A.若OB = 0,表明開始滴加鹽酸就有氣體生成,則M中的溶質NaHCO3,反應為CO2 + OH— = HCO3—,A項錯誤;B.若OB = BC,說明生成HCO3—消耗的H + 與HCO3—產生CO2消耗的H + 相等,則M中的溶質為Na2CO3,生成碳酸鈉發生的反應為2OH- + CO2 = CO32-,B項錯誤;C.3OB = BC,M中溶質為Na2CO3和NaHCO3,因為Na2CO3~NaHCO3,所以c(NaHCO3) = 2c(Na2CO3),C項正確;D.OB>BC,說明不產生CO2消耗H + 大于產生CO2消耗的H + 量,M中溶質應為NaOH和Na2CO3,若OB<BC,說明不產生CO2消耗H+小于產生CO2消耗的H+量,M中溶質應為Na2CO3和NaHCO3,D項錯誤;答案選C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】A、B、C、D代表原子序數依次增大的四種短周期非金屬元素,它們滿足以下條件:
①C的原子序數是A、B的原子序數之和,A、C、D的最外層電子數和為13; ②D的原子序數是C的2倍,D的最高價氧化物對應的水化物是二元強酸。
試根據以上敘述回答:
(1)B單質的結構式為________,畫出C元素的原子結構示意圖________________;
(2)下列環境問題與B與C形成的化合物有關的是________;
A.溫室效應 B.光化學煙霧 C.酸雨 D.PM2.5
II.現有下列短周期元素相關性質的數據:
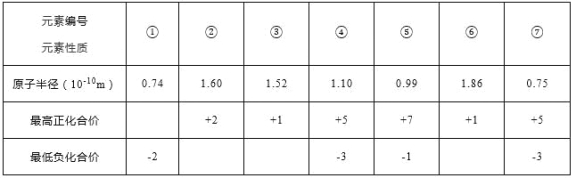
試回答下列問題:
(l)元素⑤在周期表中韻位置__________________;
(2)元素④與元素⑦相比較,氣態氫化物較穩定的是_____________(填結構式);
(3)元素④形成的+3和+5價的氯化物中,各原予均達到8電子穩定結構的化合物是___________(寫化學式);
(4)以下敘述正確的是____________。
A.氫化物的沸點為④<⑦
B.①與②形成的化合物具有兩性
C.與稀鹽酸反應單質②比單質⑥快
D.最高價氧化物對應水化物的堿性③>⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨是一種重要的化工產品,是氮肥工業、有機合成工業以及制造硝酸、銨鹽和純堿等的原料。
(1)在一定溫度下,在固定體積的密閉容器中進行可逆反應:N2+3H2![]() 2NH3。該可逆反應達到平衡的標志是________________。
2NH3。該可逆反應達到平衡的標志是________________。
A.3v(H2)正=2v(NH3)逆
B.單位時間生成m mol N2的同時消耗3m mol H2
C.容器內的總壓強不再隨時間而變化
D.混合氣體的密度不再隨時間變化
E.a molN≡N鍵斷裂的同時,有6amolN—H鍵斷裂
F.N2、H2、NH3的分子數之比為1∶3∶2
(2)某化學研究性學習小組模擬工業合成氨的反應。在容積固定為2L的密閉容器內充入1molN2和3molH2,加入合適催化劑(體積可以忽略不計)后在一定溫度壓強下開始反應,并用壓力計監測容器內壓強的變化如下:
反應時間/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
壓強/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
則從反應開始到25min時,以N2表示的平均反應速率= ;該溫度下平衡常數K= ;
(3) 利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,主要反應如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H=-99kJ·mol-1
CH3OH(g) △H=-99kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H
CO(g)+H2O(g) △H
圖1中能正確反映平衡常數K隨溫度變化關系的曲線是 ;反應③的△H= kJ·mol-1。
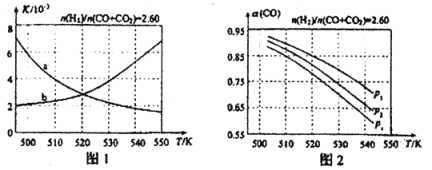
(4)合成氣的組成n(H2)/n(CO+CO2)=2.60時體系中的CO平衡轉化率α(CO)與溫度和壓強的關系如圖2所示。圖中的壓強p1、p2、p3由大到小的順序為 ;α(CO)隨溫度升高而減小,其原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,將甲、乙兩個裝有不同物質的針筒用導管連接起來,將甲針筒內的物質壓到乙針筒內,進行實驗,對乙針筒里的現象所作的判斷不正確的是( )
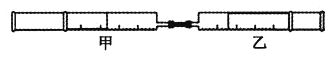
實驗序號 | 甲針筒內物質 | 乙針筒內物質 | 乙針筒里的現象 |
A | HCl | AgNO3溶液 | 產生白色沉淀 |
B | NH3 | FeCl3溶液 | 出現紅褐色沉淀 |
C | SO2 | BaCl2 | 產生白色沉淀 |
D | Cl2 | 紫色石蕊溶液 | 先變紅后褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】完全沉淀等物質的量濃度的NaCl、MgCl2、AlCl3溶液中的Cl—,消耗等物質的量濃度的AgNO3溶液的體積比為3:2:1,則上述溶液的體積比為( )
A. 1:1:1 B. 3:2:1
C. 6:3:2 D. 9:3:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組的同學用下圖所示裝置研究有關電化學的問題(甲、乙、丙三池中溶質足量),當閉合該裝置的電鍵K時,觀察到電流計的指針發生了偏轉.

請回答下列問題:
(1)甲池為 (填“原電池”、“電解池”或“電鍍池”),A電極的電極反應式為 .
(2)丙池中F電極為 (填“正極”、“負極”、“陰極”或“陽極”),該池的總反應方程式為 .
(3)當乙池中C極質量減輕10.8g時,甲池中B電極理論上消耗O2的體積為 mL(標準狀況).
(4)一段時間后,斷開電鍵K,下列物質能使乙池恢復到反應前濃度的是 (填選項字母).
A.Cu
B.CuO
C.Cu(OH)2
D.Cu2(OH)2CO3.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2CO2+2Na2O2=2Na2CO3+O2,在密閉容器中,將6.6gCO2與一定量的Na2O2固體充分反應后,氣體變為3.8g。下列說法正確的是()
A.3.8g氣體全部是O2
B.3.8g氣體通過足量NaOH溶液后,氣體減少2.2g
C.反應后的固體是混合物
D.生成Na2CO3的質量為15.9g
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com