
���}Ŀ����ˮ���}���dz�Ҋ(ji��n)�Ļ��W(xu��)ԇ�����Ɍ�������NH3�����Ȼ�����w�քe����ˮ�Ƶá�
��1������İl(f��)���b�ÿ����x���D�е�_______������(y��ng)�Ļ��W(xu��)����ʽ��__________________��
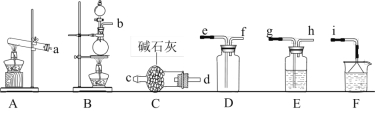
��2�����ռ�һƿ����İ��⣬�x���ψD�е��b�ã����B�����?y��n)飺�l(f��)���b����_______��������������С����ĸ��ʾ����
��3��С�A��̽����������ˮ�Ƿ�l(f��)�����W(xu��)����(y��ng)���O(sh��)Ӌ(j��)���������(sh��)�(y��n)������пհ���:
��(sh��)�(y��n)���� | ��(sh��)�(y��n)�F(xi��n)�Y(ji��)Փ |
�����з�̪��Һ�ĞV���������ʢ�и��ﰱ��ļ���ƿ�� | �o(w��)���@�F(xi��n)�� |
��4��С�������з�̪��ϡ��ˮ�ӟᣬ�^�쵽��Һ�ɫ׃�\��ԭ������� ��
��5��С��������ʯ���ϡ�}��ӟᣬ��Һ�ɫ�o(w��)���@׃�������M(j��n)һ���о���ȡϡ�}��ֳ�2�ݣ���δ��(j��ng)�ӟ���ӟ����һ�Εr(sh��)�g����s���քe�к͵����Ě������c�����Ķ��ߵ��|(zh��)�����٩������tϡ�}�Ὓ(j��ng)�ӟ���к��� �����������������pС��������׃���������ȥ�Ȼ��c��Һ�е�̼���c��С���O(sh��)Ӌ(j��)�����·�����

���J(r��n)���������� ����������������������������Ո(q��ng)������ ����������f(shu��)��ԭ���粻�������f(shu��)��ԭ���O(sh��)Ӌ(j��)���M(j��n)��������
��6�����о������߀ԭ�ԣ�С�m����һ��(sh��)�(y��n)������2���ռ�����NH3����ע����X�У�Ӳ�|(zh��)������Y�м�����������������NO2���ɶ��ÊA��K1��K2�A��������һ���ض��°��Dʾ�b���M(j��n)�Ќ�(sh��)�(y��n)��
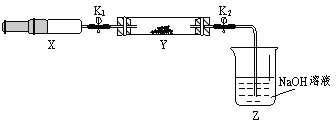
�������E | ��(sh��)�(y��n)�F(xi��n)�� | ���ԭ�� |
���_(k��i)K1���Ƅ�(d��ng)ע����������ʹX�еĚ��w��������Y���� | ��Y����___________ | ������(y��ng)�Ļ��W(xu��)����ʽ ______________________ |
��ע���������˻�ԭ̎���̶������b�û֏�(f��)���Ҝ� | Y����������ˮ�� | ���ɵĚ�B(t��i)ˮ���� |
���_(k��i)K2 | ��___________________ | ��____________________ |
���𰸡�
��1�� A��2NH4Cl+Ca��OH��2![]() CaCl2+2NH3��+2H2O������B��NH3��H2O
CaCl2+2NH3��+2H2O������B��NH3��H2O ![]() NH3��+H2O
NH3��+H2O
��2��d��c��f��e��i��
��3�� �����з�̪��Һ�ĞV����(r��n)����ʢ�иɲٰ���ļ���ƿ�У��V��׃�t���f(shu��)��������ˮ��Һ�ʉA�ԣ�
��4����ˮ�ܟ�ֽ⣬�S�ض����߰����ܽ�ȜpС����(d��o)�°�ˮ��Ƚ����������𰸼�����
��5�� �pС��������̼���c�cϡ�}�ᷴ��(y��ng)�����Ȼ��c��������̼��ˮ�����Լ���ϡ�}��ɰ�̼���c�D(zhu��n)�����Ȼ��c����ȥ������(y��ng)�����Һ�ӟ���У��}����Г]�l(f��)�ԣ����Եõ��������Ȼ��c���ʺ�����
��6�����t��ɫ���w����׃�\������ʞ�o(w��)ɫ����8NH3+6NO2![]() 7N2 +12H2O����Z�е�NaOH��Һ������Y��������ԓ����(y��ng)�ǚ��w�w�e�pС�ķ���(y��ng)��Y�܃�(n��i)����(qi��ng)���ͣ��ڴ�≺�������°l(f��)��������
7N2 +12H2O����Z�е�NaOH��Һ������Y��������ԓ����(y��ng)�ǚ��w�w�e�pС�ķ���(y��ng)��Y�܃�(n��i)����(qi��ng)���ͣ��ڴ�≺�������°l(f��)��������
��������
ԇ�}��������1������(sh��)�(y��n)���üӟ���w�Ȼ��@�͚������}�ķ����Ƃ䰱�⣬����(y��ng)���B(t��i)����w�c���w������(y��ng)�l����ӟᣬ�����x��A��l(f��)���b�ã�����(y��ng)����ʽ��Ca��OH��2+2NH4Cl![]() CaCl2+2NH3��+2H2O���ʴ𰸞飺A��Ca��OH��2+2NH4Cl
CaCl2+2NH3��+2H2O���ʴ𰸞飺A��Ca��OH��2+2NH4Cl![]() CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��
��2����(sh��)�(y��n)���üӟ���w�Ȼ��@�͚������}�ķ����Ƃ䰱�⣬�Ƃ�Ě��w�к���ˮ���⣬�����A�Ԛ��w����(y��ng)�x��ʢ�ЉAʯ�Ҹ���ܸ�����w������O������ˮ���ܶ�С�ڿ՚��ܶ����ԑ�(y��ng)�x�������ſ՚ⷨ�ռ����w������O������ˮ��β�������ˮ���գ�ע���ֹ�����İl(f��)�����������_���B�����?y��n)飺�l(f��)���b����d��c��f��e��i���ʴ𰸞飺d��c��f��e��i��
��3�������з�̪��Һ�ĞV����(r��n)����ʢ�иɲٰ���ļ���ƿ�У��V��׃�t���f(shu��)��������ˮ��Һ�ʉA�ԣ��ʴ𰸞飺�����з�̪��Һ�ĞV����(r��n)����ʢ�иɲٰ���ļ���ƿ�У��V��׃�t���f(shu��)��������ˮ��Һ�ʉA����
��4��С�������з�̪��ϡ��ˮ�ӟᣬ�^�쵽��Һ�tɫ׃�\��ԭ������ǰ�ˮ����(w��n)���ܟ��ֽ����ɰ����ˮ����(d��o)����Һ�A�Ԝp�����t��Һ�ɫ׃�\�ʴ𰸞飺��ˮ�ܟ�ֽ⣬�S�ض����߰����ܽ�ȜpС����(d��o)�°�ˮ��Ƚ��ͣ�
��5��ȡϡ�}��ֳ�2�ݣ���δ��(j��ng)�ӟ���ӟ����һ�Εr(sh��)�g����s���քe�к͵����Ě������c�����Ķ��ߵ��������������tϡ�}�Ὓ(j��ng)�ӟ���к���׃С�����}����Г]�l(f��)�ԣ����|(zh��)׃�٣����ĵĚ������c�٣�̼���c�cϡ�}�ᷴ��(y��ng)�����Ȼ��c��������̼��ˮ�����Լ���ϡ�}��ɰ�̼���c�D(zhu��n)�����Ȼ��c����ȥ������(y��ng)�����Һ�ӟ���У��}����Г]�l(f��)�ԣ����Եõ��������Ȼ��c���ʺ������ʴ𰸞飺�pС��������̼���c�cϡ�}�ᷴ��(y��ng)�����Ȼ��c��������̼��ˮ�����Լ���ϡ�}��ɰ�̼���c�D(zhu��n)�����Ȼ��c����ȥ������(y��ng)�����Һ�ӟ���У��}����Г]�l(f��)�ԣ����Եõ��������Ȼ��c���ʺ�����
��6�����_(k��i)K1���Ƅ�(d��ng)ע����������ʹX�еĚ��w��������Y���У��t�����c���������l(f��)���w�з���(y��ng) ���ɟo(w��)ɫ��?d��)⣬���Կ����F(xi��n)��飺�t��ɫ���w����׃�\������(j��)����(y��ng)8NH3+6NO2![]() 7N2+12H2O�Լ��b�û֏�(f��)���Ҝغ��B(t��i)ˮ���ۿ��Д෴��(y��ng)����w���Ӕ�(sh��)�p�٣��b�Ã�(n��i)����(qi��ng)���ͣ����Դ��_(k��i)K2�ڴ�≺�������°l(f��)���������ʴ𰸞飺���t��ɫ���w����׃�\������ʞ�o(w��)ɫ����8NH3+6NO2
7N2+12H2O�Լ��b�û֏�(f��)���Ҝغ��B(t��i)ˮ���ۿ��Д෴��(y��ng)����w���Ӕ�(sh��)�p�٣��b�Ã�(n��i)����(qi��ng)���ͣ����Դ��_(k��i)K2�ڴ�≺�������°l(f��)���������ʴ𰸞飺���t��ɫ���w����׃�\������ʞ�o(w��)ɫ����8NH3+6NO2![]() 7N2 +12H2O����Z�е�NaOH��Һ������Y���У���ԓ����(y��ng)�ǚ��w�w�e�pС�ķ���(y��ng)��Y�܃�(n��i)����(qi��ng)���ͣ��ڴ�≺�������°l(f��)��������
7N2 +12H2O����Z�е�NaOH��Һ������Y���У���ԓ����(y��ng)�ǚ��w�w�e�pС�ķ���(y��ng)��Y�܃�(n��i)����(qi��ng)���ͣ��ڴ�≺�������°l(f��)��������


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ����1���������҂���Ϥ�����|(zh��)������̖(h��o)����
��O2��SO2��CaCl2��HNO3��NaOH��NH4Cl
�@Щ���|(zh��)�У����ڹ��r(ji��)���������___________�������x�ӻ��������___________��ֻ���x���I����___________��
��2�����������քe��ʾԪ�ص�ij�N���|(zh��)�c��늺ɔ�(sh��)���P(gu��n)ϵ(Z���늺ɔ�(sh��)��Y��Ԫ�ص����P(gu��n)���|(zh��))��
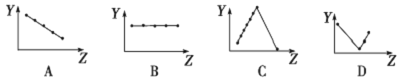
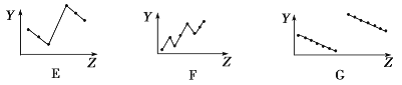
���c�����Ԫ�����P(gu��n)���|(zh��)����������Ę�(bi��o)̖(h��o)��������(y��ng)��̖(h��o)�У�
�ٵڢ�A��Ԫ�ص��������Ӕ�(sh��)________________��
�ڵڶ�������������Ԫ���Sԭ����(sh��)�f��ԭ�Ӱ돽��׃��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����҈D��ʾ���׳صĿ�����(y��ng)ʽ�飺N2H4��O2=N2+2H2O�������P(gu��n)��ԓ늳ع����r(sh��)���f(shu��)�����_����

A. ԓ�b�ù����r(sh��)��Ag늘O���К��w����
B. �׳غ��ҳ��е���Һ��pH���pС
C. �׳���ؓ(f��)�O����(y��ng)��N2H4-4e-=N2+4H+
D. ��(d��ng)�׳�������0.1molN2H4�r(sh��)���ҳ�����S�����a(ch��n)��6.4g���w
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����л��W(xu��)���|(zh��)�У���N���߂���ǣ� ��
A.һ���l���°l(f��)���ֽⷴ��(y��ng)
B.�����ڿ՚���ȼ��
C.�cCl2�l(f��)��ȡ������(y��ng)
D.��ʹ���i���������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�������x�ӽM�ϣ��ܴ����������
A��������Һ�У�Al3+��Fe3+��SO32-��Cl-
B������Һ�У�MnO4-��K+��Na+��NO3-
C����(qi��ng)�A����Һ�У�Na+��NO3-��SO32-��HCO3-
D����(qi��ng)������Һ�У�Na+��Fe2+��SO42-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ��bXn����aYm+���x�ӵ���ӌӽY(ji��)��(g��u)��ͬ���ta���ڣ�������
A. b��m��n B. b+m+n C. b��m+n D. m��n+b
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����з����У��Ⱥ��Ц��I�ֺ��Ц��I���ǣ� ��
A. CH4 B. HCl C. CH2=CH2 D. F2
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ���״���һ�N��(y��u)�|(zh��)ȼ�ϣ��ڹ��I(y��)�ϳ���CO��H2�ϳɼ״�������(y��ng)����ʽ��CO (g)+H2(g)![]() CH3OH(g)����֪����CO(g)+1/2O2(g)=CO2(g) ��H1=��283.0 kJ/mol����H2(g)+1/2O2(g)=H2O(g) ��H2=��241.8 kJ/mol����CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ��H3=��192.2 kJ/mol���ش����І�(w��n)�}��
CH3OH(g)����֪����CO(g)+1/2O2(g)=CO2(g) ��H1=��283.0 kJ/mol����H2(g)+1/2O2(g)=H2O(g) ��H2=��241.8 kJ/mol����CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ��H3=��192.2 kJ/mol���ش����І�(w��n)�}��
��1��Ӌ(j��)��CO(g)+2H2(g)![]() CH3OH(g)�ķ���(y��ng)����H4=_________________��
CH3OH(g)�ķ���(y��ng)����H4=_________________��
��2�����ڽ^�ᡢ���ݵ����]�����г���1 mol CO��2 mol H2���l(f��)������(y��ng)CO(g)+2H2(g)![]() CH3OH(g)������ʾ��D���_�����f(shu��)�����M(j��n)�е�t1�r(sh��)�̞�ƽ���B(t��i)����________�����x�(xi��ng)��ĸ����
CH3OH(g)������ʾ��D���_�����f(shu��)�����M(j��n)�е�t1�r(sh��)�̞�ƽ���B(t��i)����________�����x�(xi��ng)��ĸ����

��3��T1��r(sh��)����һ��(g��)�w�e��5 L�ĺ��������г���1 mol CO��2 mol H2����(j��ng)�^(gu��)5 min�_(d��)��ƽ�⣬CO���D(zhu��n)���ʞ�0.8��T1��r(sh��)������һ�w�e��׃�����]������Ҳ����1 mol CO��2 mol H2���_(d��)��ƽ��r(sh��)CO���D(zhu��n)���ʞ�0.7���tԓ�������w�e______5 L�����������=������T1��r(sh��)��CO(g)+2H2(g)![]() CH3OH(g)��ƽ�ⳣ��(sh��)K=____________��
CH3OH(g)��ƽ�ⳣ��(sh��)K=____________��
��4����T1��r(sh��)�����w�e��5 L�ĺ��������г���һ������H2��CO������(y��ng)�_(d��)��ƽ��r(sh��)CH3OH���w�e��?j��n)?sh��)�cn(H2)/n(CO)���P(gu��n)ϵ��D��ʾ���ضȲ�׃����(d��ng)n(H2)/n(CO)=2.5�r(sh��)���_(d��)��ƽ���B(t��i)��CH3OH���w�e��?j��n)?sh��)�����LjD���е�________�c(di��n)��

��5���������ȼ�ϵ������ʿ��Ԍ��״��O(sh��)Ӌ(j��)��ȼ��늳أ�����KOH��늽��|(zh��)��Һ�r(sh��)���״�ȼ��늳ص�ؓ(f��)�O����(y��ng)ʽ________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ���Q������(x��)���к���DNA�������������D(zhu��n)�Q���ܵĽY(ji��)��(g��u)�ǣ� ��
A. �����wB. �~�G�wC. �����wD. �����w���~�G�w
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com