正極材料為LiCoO2的鋰離子電池已被廣泛用作便攜式電源。但鈷的資源匱乏限制了其進一步發展。
(1)橄欖石型LiFePO4是一種潛在的鋰離子電池正極材料,它可以通過(NH4)2Fe(SO4)2、H3PO4與LiOH溶液發生共沉淀反應,所得沉淀經80℃真空干燥、高溫成型而制得。
①共沉淀反應投料時,不將(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是________________。
②共沉淀反應的化學方程式為____________________。
③高溫成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的導電性能外,還能___________________。
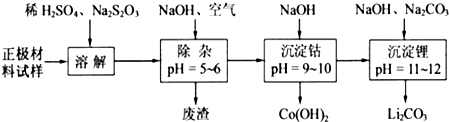
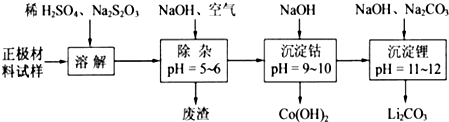
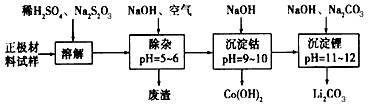
(2)廢舊鋰離子電池的正極材料試樣(主要含有LiCoO2及少量Al、Fe等)可通過下列實驗方法回收鈷、鋰。
①在上述溶解過程中,S2O32-被氧化成SO42-,LiCoO2在溶解過程中反應的化學方程式為____________________
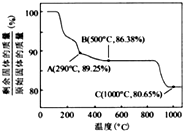
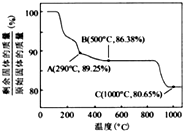
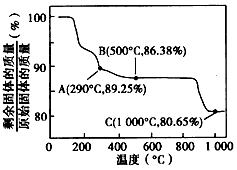
②Co(OH)2在空氣中加熱時,固體殘留率隨溫度的變化如上圖所示。已知鈷的氫氧化物加熱至290℃時已完全脫水,則1000℃時,剩余固體的成分為___________(填化學式);在350-400℃范圍內,剩余固體的成分為_______(填化學式)。