
(10分)工業(yè)上常用天然氣作為制備 的原料。已知:
的原料。已知:
①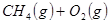
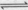
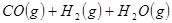

②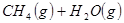
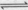
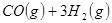
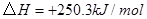
③
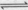
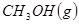
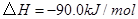
(1)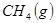 與
與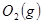 反應生成
反應生成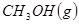 的熱化學方程式為
。
的熱化學方程式為
。
(2)向VL恒容密閉容器中充入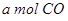 與
與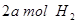 ,在不同壓強下合成甲醇。
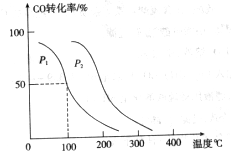
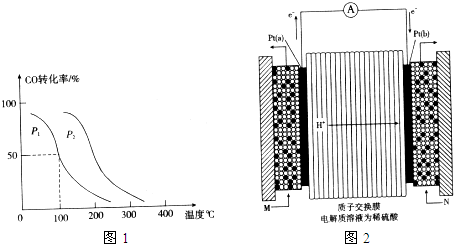
,在不同壓強下合成甲醇。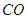 的平衡轉(zhuǎn)化率與溫度、壓強的關(guān)系如下圖所示:
的平衡轉(zhuǎn)化率與溫度、壓強的關(guān)系如下圖所示:
①壓強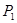
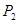 (填“<”、“>”或“=”)
(填“<”、“>”或“=”)
②在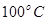 、
、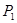 壓強時,平衡常數(shù)為
(用含
壓強時,平衡常數(shù)為
(用含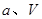 的代數(shù)式表示)。
的代數(shù)式表示)。
(3)下圖是甲醇燃料電池(電解質(zhì)溶液為稀硫酸)結(jié)構(gòu)示意圖,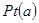 電極通入的
電極通入的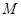 為
,電極反應式是
。
為
,電極反應式是
。
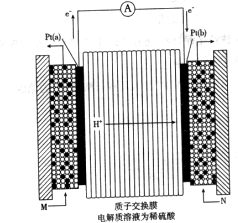
若用該電池電解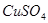 溶液,當?shù)玫?img src="http://thumb.zyjl.cn/pic6/res/gzhx/web/STSource/2012082515565637533077/SYS201208251557403559418079_ST.files/image026.png">銅時,參加反應的氣體
溶液,當?shù)玫?img src="http://thumb.zyjl.cn/pic6/res/gzhx/web/STSource/2012082515565637533077/SYS201208251557403559418079_ST.files/image026.png">銅時,參加反應的氣體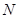 的體積應為
的體積應為
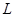 (標準狀況)。
(標準狀況)。
(1)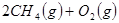
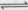
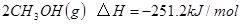 2分
2分
(2)① < 1分
②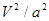 2分
2分
(3)甲醇(或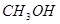 ) 1分
) 1分
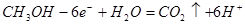 2分
2分
0.56L 2分
【解析】(1)考查蓋斯定律的應用。根據(jù)已知可知,①+②+③×2即得到
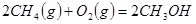 ,所以反應熱是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。
,所以反應熱是-321.5kJ/mol+250.3 kJ/mol-90 kJ/mol×2=-251.2 kJ/mol。
(2)①反應③是體積減小的可逆反應,所以壓強越大,轉(zhuǎn)化率越高,因此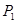 <
<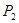 。
。
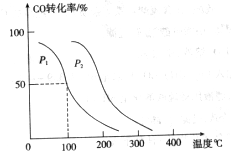
②根據(jù)圖像可知,平衡時CO的轉(zhuǎn)化率是50%,所以平衡時生成甲醇0.5amol,剩余CO和氫氣分別是0.5amol和amol,因此平衡常數(shù)為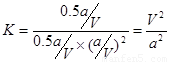 。
。
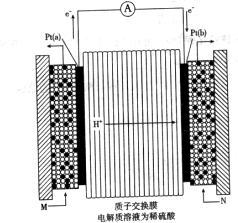
(3)根據(jù)裝置圖中電子的流向可知,左側(cè)是原電池的負極,失去電子,所以左側(cè)通入的是甲醇。應用電解質(zhì)是稀硫酸,且只能允許質(zhì)子通過,所以負極反應式為
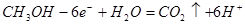 。
。


科目:高中化學 來源: 題型:
| V2 |
| a2 |
| V2 |
| a2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 能源是制約國家發(fā)展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業(yè)上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.
能源是制約國家發(fā)展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業(yè)上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北武漢市武昌區(qū)高三上學期期末考試理綜化學試卷(解析版) 題型:填空題
能源是制約國家發(fā)展進程的因素之一。甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業(yè)上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚。
(1)工業(yè)上,可以分離合成氣中的氫氣,用于合成氨,常用醋酸二氨合亞銅
[Cu(NH3)2Ac]溶液(Ac=CH3COO-)(來吸收合成氣中的一氧化碳,其反虛原理為:
[Cu(NH3)2Ac](aq)+CO+NH3 [Cu(NH3)3]Ac•CO(aq)(△H<0)
[Cu(NH3)3]Ac•CO(aq)(△H<0)
常壓下,將吸收一氧化碳的溶液處理重新獲得[Cu(NH3)2]AC溶液的措施是 ;
(2)工業(yè)上一般采用下列兩種反應合成甲醇:
反應a:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
反應b:CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
①對于反應a,某溫度下,將4.0 mol CO2(g)和12.0 mol H2(g)充入容積為2L的密閉容器中,反應到達平衡時,測得甲醇蒸氣的體積分數(shù)為30%,則該溫度下反應的平衡常數(shù)為 ;
②對于反應b,某溫度下,將1.0mol CO(g)和2.0 mol H2(曲充入固定容積的密閉容器中,反應到達平衡時,改變溫度和壓強,平衡體系中CH3OH的物質(zhì)的量分數(shù)變化情況如圖所示,溫度和壓強的關(guān)系判斷正確的是 ;(填字母代號)

A.p3>p2,T3>T2
B.p2>p4,T4>T2
C.p1>p3,T1>T3
D.p1>p4,T2>T3
(3)CO可以合成二甲醚,二甲醚可以作為燃料電池的原料,化學反應原理為:
CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H<0
CH3OCH3(g)+H2O(g) △H<0
①在恒容密閉容器里按體積比為1:4充入一氧化碳和氫氣,一定條件下反應達到平衡狀態(tài)。當改變反應的某一個條件后,下列變化能說明平衡一定向正反應方向移動的是 ;
A.逆反應速率先增大后減小
B.正反應速率先增大后減小
C.反應物的體積百分含量減小
D.化學平衡常數(shù)K值增大
②寫出二甲醚堿性燃料電池的負極電極反應式 ;
③己知參與電極反應的電極材料單位質(zhì)量放出電能的大小稱為該電池的比能量。關(guān)于二甲醚堿性燃料電池與乙醇堿性燃料電池,下列說法正確的是 (填字母)
A.兩種燃料互為同分異構(gòu)體,分子式和摩爾質(zhì)量相同,比能量相同
B.兩種燃料所含共價鍵數(shù)目相同,斷鍵時所需能量相同,比能量相同
C.兩種燃料所含共價鍵類型不同,斷鍵時所需能量不同,比能量不同
(4)已知l g二甲醚氣體完全燃燒生成穩(wěn)定的氧化物放出的熱量為31.63 kJ,請寫出表示二甲醚燃燒熱的熱化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
工業(yè)上常用天然氣作為制備![]() 的原料。已知:
的原料。已知:
①![]()
![]()
![]()
![]()
②![]()
![]()
![]()
![]()
③![]()
![]()
![]()
![]()
(1)![]() 與
與![]() 反應生成
反應生成![]() 的熱化學方程式為 。
的熱化學方程式為 。
(2)向VL恒容密閉容器中充入![]() 與
與![]() ,在不同壓強下合成甲醇。
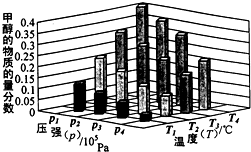
,在不同壓強下合成甲醇。![]() 的平衡轉(zhuǎn)化率與溫度、壓強的關(guān)系如下圖所示:
的平衡轉(zhuǎn)化率與溫度、壓強的關(guān)系如下圖所示:
①壓強![]()
![]() (填“<”、“>”或“=”)
(填“<”、“>”或“=”)
②在![]() 、
、![]() 壓強時,平衡常數(shù)為 (用含
壓強時,平衡常數(shù)為 (用含![]() 的代數(shù)式表示)。
的代數(shù)式表示)。
(3)下圖是甲醇燃料電池(電解質(zhì)溶液為稀硫酸)結(jié)構(gòu)示意圖,![]() 電極通入的
電極通入的![]() 為 ,電極反應式是 。
為 ,電極反應式是 。
若用該電池電解![]() 溶液,當?shù)玫?sub>
溶液,當?shù)玫?sub>![]() 銅時,參加反應的氣體
銅時,參加反應的氣體![]() 的體積應為
的體積應為
![]() (標準狀況)。
(標準狀況)。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com