
氯酸鉀和亞硫酸氫鈉發(fā)生氧化還原反應(yīng)生成Cl(-1價)和S(+6價)的速率如圖所示,已知這個反應(yīng)速率隨著溶液中c(H+)增大而加快。
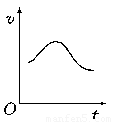
(1)反應(yīng)開始進(jìn)行時,反應(yīng)速率加快的原因是(要求寫出化學(xué)方程式)
;
(2)反應(yīng)后期,反應(yīng)速率下降的原因是
。
(1)2KCl O3+6NaHSO3==3Na2SO4+2KCl+3H2SO4,溶液中c(H+)增大,化學(xué)反應(yīng)速率加快。
(2)隨著反應(yīng)的進(jìn)行,KClO3和NaHSO3濃度明顯減小,后期化學(xué)反應(yīng)速率減慢。
【解析】
試題分析:(1)反應(yīng)起始階段,根據(jù)反應(yīng)的化學(xué)方程式2KClO3+6NaHSO3=3Na2SO4+2KCl+3H2SO4可知,溶液中c(H+)逐漸增大,所以化學(xué)反應(yīng)速率加快。
(2)隨著反應(yīng)的進(jìn)行,KClO3和NaHSO3濃度明顯減小,即反應(yīng)物的濃度降低,從而導(dǎo)致后期化學(xué)反應(yīng)速率減慢。
考點(diǎn):考查外界條件對反應(yīng)速率的影響
點(diǎn)評:該題是高考中的常見題型,試題基礎(chǔ)性強(qiáng),側(cè)重對稀釋能力的考查,屬于中等難度的試題。該題有利于培養(yǎng)學(xué)生的靈活應(yīng)變能力,也有利于培養(yǎng)學(xué)生的知識遷移能力。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學(xué)生10分鐘應(yīng)用題系列答案
小學(xué)生10分鐘應(yīng)用題系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:

(1)反應(yīng)開始時,反應(yīng)速率加快的原因是_____________________________________________。
(2)反應(yīng)后期,反應(yīng)速率又下降的原因是_____________________________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:

(1)寫出該反應(yīng)的離子方程式____________________________;
(2)為什么反應(yīng)開始時速率加快____________________________;
為什么后期反應(yīng)速率下降____________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:

(1)反應(yīng)開始反應(yīng)速率加快的原因是________________________________________。
(2)反應(yīng)后期反應(yīng)速率下降的原因是________________________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:

圖9-4?
(1)為什么反應(yīng)開始一段時間內(nèi)速率逐漸加快? 。?
(2)為什么后期反應(yīng)速率逐漸減慢? 。?
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
氯酸鉀和亞硫酸氫鈉發(fā)生氧化還原反應(yīng)生成Cl(-1價)和S(+6價)的速率如圖曲線所示,已知ClO3-的氧化性隨c(H+)的增大而增強(qiáng),有關(guān)方程式為:
ClO3-+3 HSO3-![]() Cl-+3 H+ +3 SO42-
Cl-+3 H+ +3 SO42-
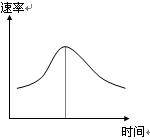
(1)反應(yīng)開始時反應(yīng)速率加快的原因是 ![]() ;
;
(2)反應(yīng)后期反應(yīng)速率下降的原因是 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com