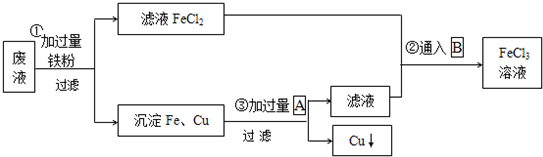
分析:由流程圖可知廢液的處理過程為:利用過量的飽和氯化鐵溶液與鍍銅電路板上金屬銅反應,然后用過量鐵粉把生成的氯化銅置換得到金屬銅,同時把過量的氯化鐵溶液轉變為氯化亞鐵溶液,過濾所得沉淀用鹽酸分離銅和鐵,最后,進行過濾分離出金屬銅而回收銅,并把濾液氯化亞鐵與氯氣反應而轉化為氯化鐵溶液循環利用.
解答:解:(1)分離Cu和Fe,可加入鹽酸,得到FeCl2和Cu,反應后的濾液為FeCl2,可與Cl2反應生成FeCl3,故答案為:HCl;Cl2;
(2)CuCl2和FeCl3中加入鐵粉,分別發生:Fe+2FeCl3=3FeCl2,Fe+CuCl2=Cu+FeCl2,氯化亞鐵與氯氣反應而轉化為氯化鐵,反應的化學方程式為2FeCl2+Cl2 =2FeCl3,
故答案為:Fe+2FeCl3=3FeCl2;Fe+CuCl2=Cu+FeCl2;2FeCl2+Cl2 =2FeCl3;
(3)Fe比Cu活潑,可與鹽酸反應生成而分離出Cu,反應的離子方程式為Fe+2H+=Fe2++H2↑,故答案為:Fe+2H+=Fe2++H2↑.
點評:本題考查物質的分離,題目難度中等,注意根據流程結合物質的性質解答該題.